
科目: 来源: 题型:
【题目】[化学―选修5: 有机化学基础]
某塑化剂DEHP的结构简式如右图所示,其合成路线如下:


已知:① A 的核磁共振氢谱有三组峰。
② 
回答下列问题:
(1)A的结构简式为_____,B的结构简式为_________。
(2)C的化学方名称为_______,反应分两步进行,其反应类型分别为_____、_____。
(3)DEHP在稀硫酸催化下水解的化学方程式为____________。
(4)写出DEHP酸性水解产物中满足下列条件的所有同分异构体的结构简式(不考虑立体异构)_______。
a.属于芳香族化合物 b.核磁共振氢谱有两组峰
(5)写出以D和乙烯为原料(其他无机试剂任选)制备聚邻笨二甲酸乙二醇酯的合成路线___。
查看答案和解析>>
科目: 来源: 题型:
【题目】
周期表前四周期元素R、X、Y、Z原子序效依次增大,RO2是红棕色气体:X位于元素周期表ⅣB族:同周期元素的基态原子中,Y的未成对电子最多;基态Z+最外层有18个电子。请回答下列问题:
(l)基态Y原子的价层电子轨道示意图为__________。
(2) RO3-的立体构型是______________,写出两个与RO3- 其有相同空间构型和键合形式的分子或离子____________。
(3) R及与R相邻的同周期元素中,第一电离能最大的是____(填元素符号), 原因是_____。
(4)若过渡金属离子具有未成对d电子,容易吸收可见光而发生d-d跃迁,因而它们的水合离子常常具有颜色;若过渡金属离子无未成对d电子,则其水合离子是无色的。下列水合离子为无色的是_____
A. X2+ B.X4+ C. Y3+ D. Z2+
(5)右图是Z与金的一种合金晶体的立方晶胞:
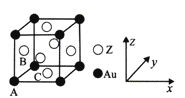
① 该晶体中,Z与Au的原子个数比为_________;
② 原子坐标参数可表示晶胞内各原子的相对位置。图示晶胞中,原子坐标参数A为(0, 0,0 );
B为(0,1/2,1/2)则C原子(底心)的坐标参数为__________。
③ 已知该立方晶胞的密度为dg/cm3 ,NA为阿伏伽德罗常数的值,则晶胞参数(描述晶胞的大小和形状)a=_______nm。(列出表达式即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关颜色变化的叙述不正确的是 ( )
A.淀粉溶液中滴入碘水﹣﹣变蓝色
B.溴化银见光分解﹣﹣变黑色
C.苯酚溶液中滴入Fe 3+﹣﹣变紫色
D.胆矾空气中久置﹣﹣变白色
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g) + 3H2(g) ![]() 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=______________.
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量______________.
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=_____________.
(4)达到平衡时,N2和H2的转化率之比,α(N2):α(H2)=______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(1)海水淡化的方法有_______(填一种)。
(2)写出氯化钠的形成过程:_____________。
(3)从海水中提取镁的流程如下图所示:
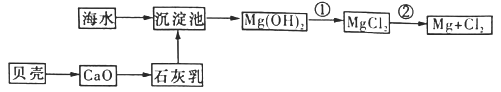
反应②的化学方程式为_______________。
从海水中提取溴的主要步骤是向浓缩的海水中通人氯气,将溴离子氧化,该反应的离子方程式为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置:
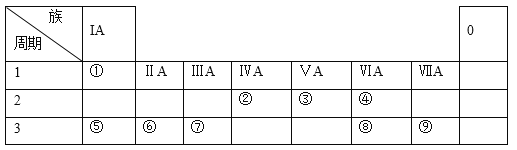
回答下列问题:
(1)写出②,③,④的气态氢化物的稳定性强弱_______________________;
(2)⑤-⑨的简单离子半径由大到小的顺序为:_______________________;(填离子符号)
(3)用电子式表示②的最高价氧化物的形成过程:____________;
(4)请设计实验比较元素⑥与⑦金属性的相对强弱:_________________;
(5) X、Y由①②④中的两种或三种元素组成。X的溶液能与小苏打反应产生Y,若X是其所属系列中最简单的分子,且相对分子质量为46,则X的名称为_________,写出X溶液与小苏打反应的离子方程式为___________________。
(6)用由①、②两种元素组成的空间构型为正四面体结构的有机物A与④元素的单质可以制成电池,电池中装有KOH浓溶液,将多孔的惰性电极甲和乙浸入KOH溶液中,在甲极通入A,乙极通入④的单质,则甲极的电极反应式为:_________________________________,一段时间后KOH的浓度将___(填“变大”、“变小”、“不变”或“无法确定”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图1是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,铁架台等已省略.)按下图连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…
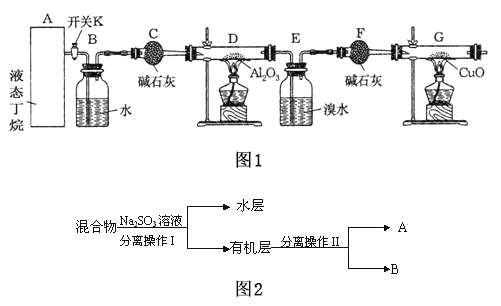
(1)这三步操作的先后顺序依次是_________________;
(2)B装置所起的作用是________________;
(3)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为 ____________________(假定流经D、G装置中的气体能完全反应)。
(4)若对E装置中的混合物再按图2流程实验:
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ ______________,分液Ⅱ_____________;
Na2SO3溶液的作用是____________(用离子方程式表示)。
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小 的,其核外电子排布式为______,价电子构型为______,属________区元素。
(2)某元素原子的价电子构型为4s24p1,它属于第________周期________族,最高正化合价为________,元素符号是________。
(3)原子序数为24的元素原子中有________个电子层,________个能级,________个未成对电子。
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计如下图所示装置,用电解法把Na2CrO4溶液转变为Na2Cr2O7溶液(2CrO42-+2H+=Cr2O72-+H2O)。下列说法正确的是
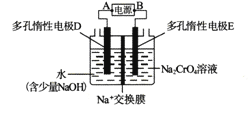
A. A为正极,B为负极
B. 电解过程中,电解槽左侧溶液pH增大
C. 电解过程中,Na+在电解槽中自左向右迁移
D. 当电路中通过lmol电子时,阴极生成0.5mol Na2Cr2O7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com