
【题目】
周期表前四周期元素R、X、Y、Z原子序效依次增大,RO2是红棕色气体:X位于元素周期表ⅣB族:同周期元素的基态原子中,Y的未成对电子最多;基态Z+最外层有18个电子。请回答下列问题:
(l)基态Y原子的价层电子轨道示意图为__________。
(2) RO3-的立体构型是______________,写出两个与RO3- 其有相同空间构型和键合形式的分子或离子____________。
(3) R及与R相邻的同周期元素中,第一电离能最大的是____(填元素符号), 原因是_____。
(4)若过渡金属离子具有未成对d电子,容易吸收可见光而发生d-d跃迁,因而它们的水合离子常常具有颜色;若过渡金属离子无未成对d电子,则其水合离子是无色的。下列水合离子为无色的是_____
A. X2+ B.X4+ C. Y3+ D. Z2+
(5)右图是Z与金的一种合金晶体的立方晶胞:
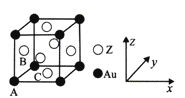
① 该晶体中,Z与Au的原子个数比为_________;
② 原子坐标参数可表示晶胞内各原子的相对位置。图示晶胞中,原子坐标参数A为(0, 0,0 );
B为(0,1/2,1/2)则C原子(底心)的坐标参数为__________。
③ 已知该立方晶胞的密度为dg/cm3 ,NA为阿伏伽德罗常数的值,则晶胞参数(描述晶胞的大小和形状)a=_______nm。(列出表达式即可)
【答案】 ![]() (2分) 平面三角形 CO32- SO3(或SeO3)(2分) N N原子3p轨道为半充满状态,相对稳定(2分) B(1分) 3:1 (1/2,1/2,0)
(2分) 平面三角形 CO32- SO3(或SeO3)(2分) N N原子3p轨道为半充满状态,相对稳定(2分) B(1分) 3:1 (1/2,1/2,0) ![]()
【解析】试题分析:由题给的条件可知, RO2是红棕色气体,R是N元素;基态Z+最外层有18个电子,Z是Cu元素;前四周期元素Y的未成对电子最多,Y价电子排布为3d54s1,Y是Cr元素;R、X、Y、Z原子序效依次增大,X位于元素周期表ⅣB族,X是Ti元素。
解析:(1)基态Cr原子的价电子排布为3d54s1,价层电子轨道示意图为![]() ; SO32-中S原子的孤电子对数=
; SO32-中S原子的孤电子对数=![]() 、价层电子对数=3+1=4,其空间构型为三角锥形,CO32- SO3与SO32-其有相同空间构型和键合形式;(3)同周期元素从左到右第一电离能逐渐增大,但N元素2p轨道为半充满状态,相对稳定,所以与N相邻的同周期元素C、N、O中,第一电离能最大的是N;(4)A.Ti2+ d 轨道有未成对电子,有颜色; B.X4+ d 轨道没有电子,所以没有颜色; C. Cr3+ d 轨道有未成对电子,有颜色; D. Cu2+ d 轨道有未成对电子,有颜色;(5)
、价层电子对数=3+1=4,其空间构型为三角锥形,CO32- SO3与SO32-其有相同空间构型和键合形式;(3)同周期元素从左到右第一电离能逐渐增大,但N元素2p轨道为半充满状态,相对稳定,所以与N相邻的同周期元素C、N、O中,第一电离能最大的是N;(4)A.Ti2+ d 轨道有未成对电子,有颜色; B.X4+ d 轨道没有电子,所以没有颜色; C. Cr3+ d 轨道有未成对电子,有颜色; D. Cu2+ d 轨道有未成对电子,有颜色;(5)
根据均摊原则,Z原子数6![]() =3,Au原子数
=3,Au原子数![]() =1,该晶体中,Z与Au的原子个数比为3:1;② 原子坐标参数可表示晶胞内各原子的相对位置。图示晶胞中,原子坐标参数A为(0, 0,0 );
=1,该晶体中,Z与Au的原子个数比为3:1;② 原子坐标参数可表示晶胞内各原子的相对位置。图示晶胞中,原子坐标参数A为(0, 0,0 );
B为(0,1/2,1/2),C原子(底心)的坐标参数为(1/2,1/2,0);③ 1 mol晶胞的质量为389g,1mol晶胞的体积为![]() ,则
,则![]() a=
a=![]() nm
nm


科目:高中化学 来源: 题型:
【题目】用A、B、C三个装置都可以制取溴苯,其中A是最基本的制备装置,B、C是改进后的装置,请仔细分析、对比三套装置,然后回答以下问题:

(1)写出三个装置中都发生的发应的化学方程式:__________、___________。
(2)装置A和C中均采用了长玻璃导管,其作用是_____________________________。
(3)装置B和C较好地解决了装置A中存在的加药品和及时密封的矛盾,方便了操作。装置A中这一问题在实验中易造成的不良后果是________________________________。
(4)装置B中采用了洗气瓶吸收装置,其作用是_______________________。
(5)装置B中也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是
___________________________、________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,铁架台等已省略.)按下图连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…
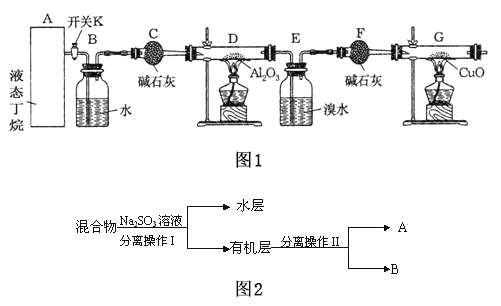
(1)这三步操作的先后顺序依次是_________________;
(2)B装置所起的作用是________________;
(3)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为 ____________________(假定流经D、G装置中的气体能完全反应)。
(4)若对E装置中的混合物再按图2流程实验:
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ ______________,分液Ⅱ_____________;
Na2SO3溶液的作用是____________(用离子方程式表示)。
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6分子结构中只存在S﹣F键,是一种优良的绝缘气体,制备原理:S(s)+3F2(g)→SF6(g)+Q.已知:1mol S(s)转化为气态硫原子吸收能量280kJ,断裂1mol F﹣F、S﹣F键需吸收的能量分别为160kJ、330kJ.则反应热效应Q的值为(单位:kJ)( )
A.178 0
B.1220
C.﹣1220
D.﹣1780
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿是铜矿的主要品种之一传统的火法冶炼在资源的综合利用、环境保护等方面会遇到困难。辉铜矿的湿法冶炼目前国内外都处于探索阶段。自氧化还氨氮分离法是一种较为理想的湿法冶炼方法,工艺流程如下图所示:
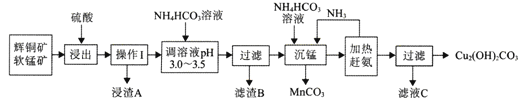
已知:
① 辉铜矿的主要成分是Cu2S,含有较多的Fe2O3、SiO2等。
② 软锰矿的主要成分是MnO2,含有较多的SiO2等。
③ 浸出时,生成一种非金属单质。
④ 室温下,Kap[Fe(OH)3]=4.0×10-38mol/L,Kap[Fe(OH)2]=8.0×10-16mol/L
完成下列填空:
(l)浸出前需要先将矿石粉碎,其目的是__________。
(2)写山浸出时主要反应的离子方程式_____________。
(3)浸渣A的主要成分为_______;调溶液pH 3.0-3.5的目的是除去______离子;室温下,若该离子的浓度为4.0×10-8mol/L,则溶液的pH=__________。
(4) 工业上可将MnCO3、在300℃左右氧化来制取具有较好催化性能的MnO2,则MnCO3在空气中受热制取MnO2的化学方程式为_________________。
(5)从滤液C中提取硫酸氨晶体的步骤为_______、_______、过滤、洗涤、干操。
(6)与火法冶炼辉铜矿相比,用图中方法冶炼辉铜矿的优点有________、_____。(列举其中2条)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2气体分别通入下列四种溶液中,有关现象及结论的说法正确的是
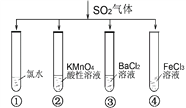
A. 试管①中有淡黄色沉淀生成,说明SO2有氧化性
B. 试管②中溶液褪色,说明SO2有漂白性
C. 试管③中能产生白色沉淀,说明SO2有酸性
D. 试管④中溶液颜色变浅,说明SO2有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是( )
A. 植物油不能使溴的四氯化碳溶液褪色
B. 淀粉水解的最终产物是葡萄糖
C. 糖类都能发生氧化反应和水解反应
D. 蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com