
科目: 来源: 题型:
【题目】下列关于苯酚的叙述中,不正确的是
A. 其浓溶液如果不慎沾在皮肤上,应立即用酒精擦洗
B. 其水溶液显强酸性,俗称石炭酸
C. 超过65℃可以与水以任意比互溶
D. 纯净的苯酚是无色晶体,在空气中易被氧化而呈粉红色
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. 钠和冷水反应 2Na+2H2O=2Na++2OH-+H2↑
B. 石灰石与醋酸溶液反应 CaCO3+2H+=Ca2++H2O+CO2↑
C. 溴化亚铁溶液中通入少量氯气 2Br -+ Cl2=Br2+2C1-
D. NH4HCO3 溶液中加入足量的 NaOH 溶液:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】苯乙烯是重要的基础有机化工原料.工业中以乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:C6H5-CH2CH3(g)![]() C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
(1)向体积为VL的密闭容器中充入n mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:
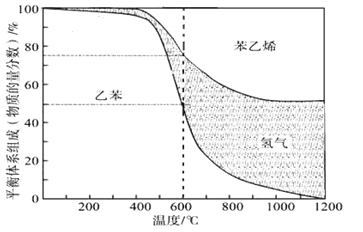
600℃时,该反应的平衡常数_____________。
(2)乙苯在特定催化剂下发生氧化脱氢:
C6H5-CH2CH3(g)+1/2O2(g)![]() C6H5-CH=CH2(g)+H2O(g) ΔH1
C6H5-CH=CH2(g)+H2O(g) ΔH1
已知 H2的燃烧热ΔH= b kJ/mol,水的汽化热为c J/g,则 ΔH1=____________。
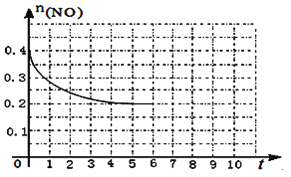
(3)在汽车上安装三元催化转化器可实现反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。
N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。
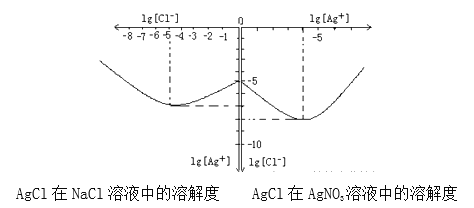
(4)沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。已知AgCl+Cl-═[AgCl2]-,如图是某温度下AgCl在NaCl溶液中的溶解情况.
由以上信息可知:
①由图知该温度下AgCl的溶度积常数为_________。
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:_______________。
查看答案和解析>>
科目: 来源: 题型:
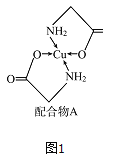
【题目】已知铜的配合物A结构如图图1。请回答下列问题:
(1)写出基态Cu的外围电子排布式________
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和x键数目之比是___;N2O与CO2互为等电子体,则N2O的电子式为_______。
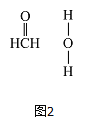
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醇分子中HCO的键角____(选填“大于”、“等于”或“小于”) l20°;甲醛能与水形成氢健,请在如图2中表示出来____。
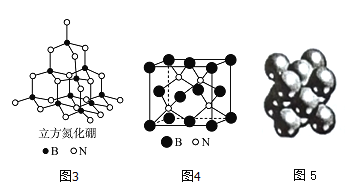
(4)立方氮化硼如图3、图4与金刚石结构相似,是超硬材料。立方氮化硼晶体内B一N键数与硼原子数之比为__________;
(5)Cu晶体的堆积方式如图5所示,设Cu原子半径为a,晶体中Cu原子的配位数为_____,晶体的空间利用率为_________。(已知:![]() ,列式并计算出结果)
,列式并计算出结果)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的分离和鉴别方法正确的是( )
A.用分液法分离碘酒和CCl4
B.用饱和碳酸钠溶液萃取乙醇中的乙酸
C.用银氨溶液鉴别甲酸乙酯和乙醛
D.用浓溴水鉴别苯和环己烯
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(l)ClO2的制备:(已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4)

①装置A中反应的化学方程式为_______________。
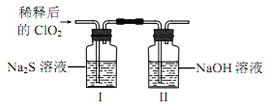
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为 a→_________(按气流方向,用小写字母表示)
③装置D的作用是_________。
(2)ClO2与 Na2S 的反应
将上述收集到的ClO2用 N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
操作步骤 | 实验现象 | 结论 |
取少量Ⅰ中溶液于试管甲中, 加入Ba(OH)2溶液,振荡 | ①_________ | 有硫酸根离子生成 |
另取少量Ⅰ中溶液于试管乙中, 滴加品红溶液和盐酸 | 品红溶液不翅色 | ② 无_____生成 |
若在试管甲中继续加Ba(OH)2溶液至 过量,静置,取上层清液于试管丙③______ | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S反应的离子方程式为__________。用于处理含硫废水时,ClO2相对于Cl2的优点是____________(任写2条)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
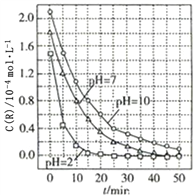
A. 在20~25min之间,pH=10时R的平均降解速率为0.04molL-1min-1
B. 溶液酸性越强,R的降解速率越小
C. R的起始浓度越小,降解速率越大
D. 50min时,pH=2和pH=7时R的降解百分率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是:①金属先熔化;②在空气中燃烧,放出黄色火花;③燃烧后得白色固体;④燃烧时火焰为黄色;⑤燃烧后生成浅黄色固体物质 ( )
A.①② B.①②③ C.①④⑤ D.④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com