
科目: 来源: 题型:
【题目】低碳经济是以低能耗、低污染、低排放为基础的经济模式。低碳经济的概念在中国正迅速从高端概念演变成全社会的行为,在新能源汽车、工业节能等多个领域都大有作为。 请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)工业上可利用CO或CO2来制备清洁液体燃料甲醇。已知:800℃时,化学反应①、反应②对应的平衡常数分别为2.5、1.0。
反应①:2H2(g)+CO(g)![]() CH3OH(g) △H = -90.8kJ mol-1
CH3OH(g) △H = -90.8kJ mol-1
反应②:H2(g)+CO2(g)![]() H2O(g)+CO(g) △H= +41.2kJ mol-1
H2O(g)+CO(g) △H= +41.2kJ mol-1
写出用CO2与H2反应制备甲醇的热化学方程式________________________,800℃时该反应的化学平衡常数K的数值为_______________。
现将不同量的CO2 (g)和H2(g)分别通入到容积为2L恒容密闭容器中进行反应②,得到如下二组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO2 (g) | H2(g) | H2(g) | CO2 (g) | |||
1 | 900 | 4 | 6 | 1.6 | 2.4 | 2 |
2 | 900 | a | b | c | d | t |
实验2中,若平衡吋,CO2 (g)的转化率小于H2(g),则a、b必须满足的关系是_________。
若在900℃时,另做一组实验,在此容器中加入10mol CO2,5mol H2,2 mol CO,5 mol H2O (g),则此时v正___v逆(填“>”、“>”或“=”)。
(2)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为:CH3OH(g)+CO(g) ![]() HCOOCH3(g) △H=-29.1KJ·mol-1 ,科研人员对该反应进行了研究,部分研究结果如下:
HCOOCH3(g) △H=-29.1KJ·mol-1 ,科研人员对该反应进行了研究,部分研究结果如下:
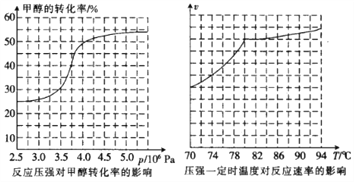
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是____(填“3.5×106 Pa”“4.0×106 Pa”或“5.0×106Pa”)。
②实际工业生产中采用的温度是80℃,其理由是______________________。
(3)已知常温下NH3H2O的电离平衡常数K= 1.75×10-5,H2CO3的电离平衡常数K1=4.4×10-7,K2 =4. 7×10-11。常温下,用氮水吸收CO2可得到NH4HCO3溶液,NH4HCO3溶液呈_____(填“酸性”“中性”或“碱性”),溶液中离子浓度由大到小的顺序为:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机物的说法不正确的是
A. 用碳酸钠溶液可一次性鉴别乙酸、苯和乙醇三种无色液体
B. ![]() 中所有原子可能共平面
中所有原子可能共平面
C. 1 mol苹果酸(HOOCCHOHCH2COOH)可与3mol NaHCO3发生反应
D. —C3H7和—C2H5O各取代苯分子中的一个氢原子形成的二元取代物的同分异构体有24种
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃。某小组在实验室中拟用下图所示装置制取并收集C1O2。冋答下列问题:
(1)C1O2的制备
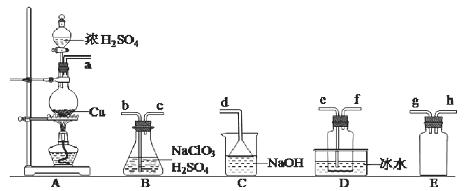
已知:SO2 +2NaClO3 +H2SO4 =2C1O2↑+2NaHSO4
①装置A中反应的化学方程式为_________________________。
②欲收集干燥的C1O2,选择上图中的装罝,其连接顺序为a→____________(按气流方向,用小写字母表示)。
③装置D的作用是_________________。
④若没有E装置,会造成的严重后果是____________________。
(2)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样;量取V1mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol/LNa2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知2Na2S2O3+I2=Na2S4O6+2NaI)
①步骤2的反应中氧化产物的电子式为______。
②滴定终点的实验现象是_________________。
③原C1O2溶液的浓度为____g/L(用少骤中的字母代数式表示)。
④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_______;若滴定开始仰视读数,滴定终点时正确读数,则测定结果_____。(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】Q、W、X、Y、Z是原子序数依次增大的短周期元素,Q和Y均满足主族序数与周期序数相等,Q与X、W与Z同主族,Q和W能形成原子个数之比为1:1和2:1的常见化合物。下列说法正确的是
A. 原子半径:Z>Y>X>W>Q
B. Q、X形成的化合物的电子式为:![]()
C. 最简单氢化物的稳定性:Z>W
D. 工业上常用电解的方法制备X、Y的单质
查看答案和解析>>
科目: 来源: 题型:
【题目】用漂白粉溶液浸泡过的有色布条,如晾晒在空气中,过一段时间,其漂白效果更好的原因是:
A. 漂白粉被氧化了
B. 漂白粉和空气中的二氧化碳充分反应生成了次氯酸
C. 有色布条被空气中的氧气氧化
D. 漂白粉溶液失去了部分水分,浓度增大了
查看答案和解析>>
科目: 来源: 题型:
【题目】膳食纤维具有突出的保健功能,人体的“第七营养素”木质索是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是

A. 芥子醇的分子式是C11H14O4,属于芳香烃
B. 1mol芥子醇最多可与3molH2加成
C. 芥子醇分子中可能所有原子都共面
D. 芥子醇能发生的反应类型有氧化、取代、加成、加聚
查看答案和解析>>
科目: 来源: 题型:
【题目】在己经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种但与生产生活有密切的联
系。
(1)为了提高煤的利用率,常将其气化为可燃性气体,主要反应是碳和水蒸气反应生成水煤气,化学反应方程式为_________________。
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g) ![]() 2NH3(g)
2NH3(g)
①合成氨的反应中的能量变化如图所示.该反应是__________反应 (填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量__________(填“大于”或“小于”)生成物化学键形成放出的总能量。
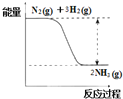
②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是_____________(填序号)。
A. 容器中混合气体的密度不随时间变化 B. 断裂3molH-H键的同时断裂6molN-H键
C.N2、H2、NH3的物质的量之比为1:3:2 D.容器中的压强不随时间变化
(3)键性电池具有容量大、放电电流大的特点,固而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)
则该电池的负极反应是_________,放电时,外电路中每通过0.2mol电子,锌的质量理论上减小______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com