
科目: 来源: 题型:
【题目】氢能是理想的清洁能源,资源丰富。以太阳能为热源分解 Fe3O4 ,经由热化学铁氧化合物循环分解水制H2 的过程如下:
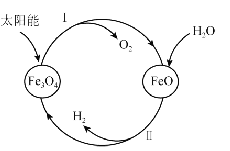
(1)过程Ⅰ:![]()
①将O2分离出去,目的是提高Fe3O4的 。
②平衡常数K 随温度变化的关系是 。
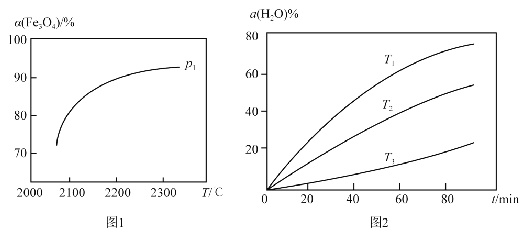
③在压强 p1下, Fe3O4的平衡转化率随温度变化的![]() (Fe3O4) ~ T 曲线如图 1 所示。若将压强由p1增大到p2 ,在图1 中画出 p2 的
(Fe3O4) ~ T 曲线如图 1 所示。若将压强由p1增大到p2 ,在图1 中画出 p2 的![]() (Fe3O4) ~ T 曲线示意图。
(Fe3O4) ~ T 曲线示意图。
(2)过程Ⅱ的化学方程式是 。
(3)其他条件不变时,过程Ⅱ在不同温度下, H2O的转化率随时间的变化![]() (H2 O) ~ t曲线如图2 所示。比较温度T1 、T2 、T3的大小关系是 ,判断依据是 。
(H2 O) ~ t曲线如图2 所示。比较温度T1 、T2 、T3的大小关系是 ,判断依据是 。
(4)科研人员研制出透氧膜(OTM) ,它允许电子、O2-同时透过,可实现水连续分解制H2。工作时,CO、H 2O分别在透氧膜的两侧反应。工作原理示意图如下:
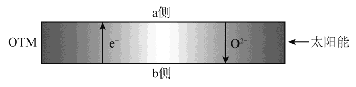
H2O在 侧反应(填“ a ”或“ b ”),在该侧H2O释放出H2的反应式是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学实验兴趣小组探究实验室中制备Cl2的过程,为证明过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如下图所示的实验装置,按要求回答问题。
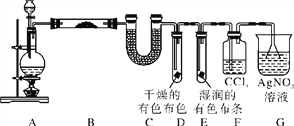
(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是________________________。
(2)①装置B中盛放的试剂名称为_______,作用是___________,现象是___________。
②装置D和E中出现的不同现象说明的问题是_______________________________。
③装置F的作用是____________________。
④写出装置G中发生反应的离子方程式:__________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应加入________(填写试剂或用品名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定质量的钠、钾投入一定量的稀盐酸中,产生气体随时间变化的曲线如下图所示,则下列说法中正确的是
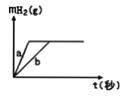
A. 投入的Na、K一定等质量
B. 投入的Na的质量大于K的质量
C. 曲线a为K,b为Na
D. 稀盐酸的量一定是不足量的
查看答案和解析>>
科目: 来源: 题型:
【题目】我国药学家屠呦呦因发现植物黄花蒿叶中含有抗疟疾的物质—青蒿素而荣获2015年诺贝尔奖。科学家对青蒿素的结构进行进一步改良,合成药效更佳的双氢青蒿素、蒿甲醚。下列说法正确的是
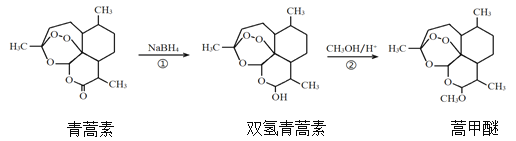
A.利用黄花蒿叶研究青蒿素结构的基本步骤为:元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式
B.①、②的反应类型分别为还原反应、酯化反应
C.双氢青蒿素在水中的溶解性大于青蒿素
D.双氢青蒿素与蒿甲醚组成上相差-CH2-,二者互为同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】右图是利用微生物燃料电池处理工业含酚废水的原理示意图,下列说法不正确的是
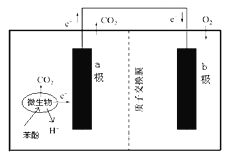
A.该装置可将化学能转化为电能
B.溶液中H+由a极移向b极
C.电极b 附近的pH降低
D.电极a附近发生的反应是C6H6O-28e- + 11H2O![]() 6CO2 + 28H+
6CO2 + 28H+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关碱金属元素的说法正确的是( )
A. 锂与过量氧气反应,生成过氧化锂
B. 从锂到铯,密度由小到大
C. 从锂到铯,熔沸点依次升高
D. 钠与水反应不如钾与水反应剧烈
查看答案和解析>>
科目: 来源: 题型:
【题目】用HCl的质量分数为36.5%的浓盐酸(密度为1.20g/cm3) 配置1L 1mol/L的稀盐酸。回答下列有关问题。完成下述操作步骤:
(1)计算:需量取36.5%的浓盐酸的体积为________毫升。
(2)量取:用量筒量取所需浓盐酸并注入到250mL烧杯中;
(3)溶解:___________________________________________________并冷却。
(4)转移(移液):_________________________________________________。
(5)洗涤:__________________________________________________________。
(6)定容:__________________________________________________________。
(7)摇匀:盖好容量瓶塞,反复颠倒、摇匀;
(8)储藏:将配置好的稀盐酸倒入试剂瓶中,并贴好标签。标签上要注明______________。
(9)误差分析:以下操作造成配得的盐酸浓度是“偏高”、“相等”还是“偏低”?
①用量筒量取浓盐酸后,用蒸馏水洗涤筒量后的溶液转入容量瓶中;____________。
②容量瓶中有少量的蒸馏水;__________________。
③没有将洗涤烧杯和玻璃棒的溶液转入容量瓶中;___________。
④定容读数时,府视容量瓶的刻度线;________________。
⑤定容摇匀后发现容量瓶中液面低于刻度线,又加水;________________。
⑥未冷却就转移定容;_____________________。
⑦润洗了容量瓶;_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。

有关上述两种化合物的说法正确的是
A. 常温下,1mol丁香酚只能与1molBr2反应
B. 丁香酚不能使FeCl3溶液发生显色反应
C. 1mol香兰素最多能与3mol氢气发生加成反应
D. 香兰素分子中至少有12个原子共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com