
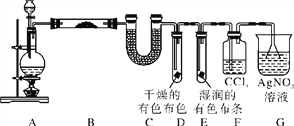
【题目】某校化学实验兴趣小组探究实验室中制备Cl2的过程,为证明过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如下图所示的实验装置,按要求回答问题。
(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是________________________。
(2)①装置B中盛放的试剂名称为_______,作用是___________,现象是___________。
②装置D和E中出现的不同现象说明的问题是_______________________________。
③装置F的作用是____________________。
④写出装置G中发生反应的离子方程式:__________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应加入________(填写试剂或用品名称)。
【答案】 浓盐酸的浓度随着反应的进行逐渐变稀,变稀以后将不再与MnO2反应;加热时浓盐酸因挥发而损失 无水硫酸铜 证明有水蒸气产生 白色固体变为蓝色晶体 干燥的Cl2无漂白性,HClO有漂白性 吸收Cl2 Ag++Cl-===AgCl↓ F G 湿润的淀粉KI试纸(或湿润的有色布条)
【解析】(1)随着反应的进行盐酸的浓度会逐渐降低,而二氧化锰是不能氧化稀盐酸的,所以实际生成的氯气总是小于理论值。
(2)①无水硫酸铜常用来检验水的存在,因为硫酸铜吸水即变成蓝色的胆矾。②氯气的漂白是靠次氯酸实现的,所以氯气不能使干燥的有色布条褪色,这说明氯气是没有漂白性的,次氯酸才具有漂白性。③由于G是用来检验氯化氢的,而氯气也能和硝酸银反应产生白色沉淀,所以在通入硝酸银溶液之前要先除去氯气,利用氯气易溶于有机溶剂中,除去氯气。④氯化氢溶于水和硝酸银反应生成氯化银白色沉淀,方程式为Ag-+Cl-=AgCl↓。
(3)氯气能溶解在四氯化碳中,但无法确定是否完全被吸收,所以需要在F和G之间连接1个装置,用来检验氯气是否完全被吸收;可利用氯气的氧化性,能把碘化钾氧化生成单质碘,而单质碘能和淀粉发生显色反应,使溶液显蓝色,所以可选用湿润的淀粉KI试纸(也可以通过漂白性来检验,因此也可以选择湿润的有色布条)。


科目:高中化学 来源: 题型:
【题目】浓度为0.50mol·L-1的某金属阳离子Mn+的溶液10.00mL,与0.40mol·L-1的NaOH溶液12.50mL完全反应,生成沉淀,则n等于
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是 ( )
A. BF3是三角锥形分子
B. NH![]() 的电子式:
的电子式: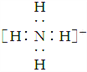 ,离子呈平面形结构
,离子呈平面形结构
C. CH4分子中的4个C—H键都是氢原子的1s轨道与碳原子的p轨道形成的sp σ键
D. 正三价阳离子的电子排布式为1s2 2s2 2p6 3s2 3p6 3d5的元素周期表中位于第Ⅷ族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开犮和应用前景。工业上通过媒的气化生成的CO和H2合成甲醇,反应原理为:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
(1)在一容积可变的密闭容器中充有10 mol CO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(a)与温度(T)、压强(p)的关系如图1所示。
①合成甲醇的反应为_____(填“放热”或“吸热”)反应。判断理由是_________。平衡常数KA_____KC(填“>”、“<”或“=”)。
②下列有关该反应的说法正确的是_____(填字母序号)。
A.当v(CO)生成=2v消耗(H2) 时该反应达到平衡状态
B.其它条件不变,只改变CO和H2的投料量,该反应的焓变发生改变
C.在反应过程中混合气体的密度和相对平均分子质量均不发生变化
D.使用催化剂可以减小反应的活化能
(2)下列措施可以提高甲醇产率的是________。
A.压缩容器体积
B.恒容条件下充入He,使体系总压强增大
C.将CH3OH (g)从体系中分离
D.恒压条件下再充入10mol CO和20mol H2
(3)甲醇一一空气燃料电池装置如图2所示。
①该电池甲电极的电极反应式为_________。
②若用此甲醇燃料电池电解200mL —定浓度NaCl与CuSO4的混合溶液(电极为惰性电极,不参与反应),电极产生气体体积(标况下)与电解时间的关系图如图3所示,此溶液中硫酸铜的浓度为______mol/L。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. 以石墨为电极电解MgCl2溶液:2Cl—+2H2O![]() Cl2+H2↑+2OH—
Cl2+H2↑+2OH—
B. CuC12溶液中加入氨水:Cu2++2OH- Cu(OH)2↓
C. KI溶液中滴入稀硫酸,空气中振荡:4H++4I-+O2 2I2+2H2O
D. 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中各组离子一定能大量共存的是
A.加入铝粉有氢气生成的溶液中:Mg2+,Cl-,NO3-,K+
B.常温下,c(H+) =0.1 mol/L的溶液中:Na+, AlO2-、S2-、 SO32-
C.含有0.1 mol/LHCO3-的溶液:Na+,Fe3+,NO3-, SCN-
D.![]() =0.1 mol/L的溶液:Na+, K+ , CO32-, NO3-
=0.1 mol/L的溶液:Na+, K+ , CO32-, NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在托盘天平的两盘,放上质量相等的A、B两烧杯,调至平衡,然后分别倒入质量相等的足量盐酸,继而在AB两烧杯中放入下述各组物质,结果天平仍保持平衡的是()
A. 0.5molNa和0.5molMg B. 0.1molZn和0.1molAl
C. 8.4gMgCO3和8.4gNaHCO3 D. 10gCaCO3和10gMgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长期以来,天文学家认为,茫茫宇宙空间,除了恒星、恒星集团、行星、星云之类的天体物质,再没有什么别的物质了。直到20世纪初,人们还认为星际空间是一片真空。后来终于发现,在星际空间充满了各种微小的星际尘埃、稀薄的星际气体、各种宇宙射线以及粒子流。60年代在星际空间发现了大量有机分子云,云中含有各种复杂的有机分子。其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键、三键等,颜色相同的球表示同一种原子)。

下列对该物质的说法中正确的是 ( )
A. 此星际分子属于烃类 B. ①处的化学键表示碳碳双键
C. ②处的化学键表示碳碳单键 D. ③处的原子可能是氯原子或氟原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com