
【题目】下列离子方程式书写正确的是 ( )
A. 以石墨为电极电解MgCl2溶液:2Cl—+2H2O![]() Cl2+H2↑+2OH—
Cl2+H2↑+2OH—
B. CuC12溶液中加入氨水:Cu2++2OH- Cu(OH)2↓
C. KI溶液中滴入稀硫酸,空气中振荡:4H++4I-+O2 2I2+2H2O
D. 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
科目:高中化学 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视________,直到因加入一滴盐酸后,溶液由黄色变为橙色,并___________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是________(填序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如右图所示,所用盐酸溶液的体积为________mL。
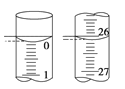
(4)某学生根据3次实验分别记录有关数据如下表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果在中国已有两千多年的栽培历史, 有“ 智慧果” 的美称。
(1) 未成熟的苹果肉变蓝色的原因是______。
(2)苹果中也有少量脂肪。脂肪对人体所起的作用是_____。( 写一条)
(3)英国是苹果酒人均消费量最大的国家。苹果酒是由成熟度高的苹果在果胶、酶、酵母菌等的作用下。经一系列变化而制得的低度酒, 其中果胶酶、酵母菌都起作用_________ ; 由 葡 萄 糖 生 成 酒 精 的 反 应________________![]() 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。

有关上述两种化合物的说法正确的是
A. 常温下,1mol丁香酚只能与1molBr2反应
B. 丁香酚不能使FeCl3溶液发生显色反应
C. 1mol香兰素最多能与3mol氢气发生加成反应
D. 香兰素分子中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组探究实验室中制备Cl2的过程,为证明过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如下图所示的实验装置,按要求回答问题。
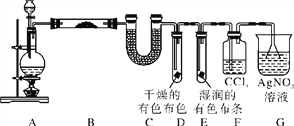
(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是________________________。
(2)①装置B中盛放的试剂名称为_______,作用是___________,现象是___________。
②装置D和E中出现的不同现象说明的问题是_______________________________。
③装置F的作用是____________________。
④写出装置G中发生反应的离子方程式:__________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应加入________(填写试剂或用品名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z和W代表原子序数依次增大的四种短周期主族元素.它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17。下列说法错误的是
A. X、Y、Z既能形成离子化合物.又能形成共价化合物
B. Y和Z元素的原子半径大小顺序为Y>Z
C. X与Y、Z之问形成的核外电子总数为10的微粒只有YX3和X2Z
D. Z、W元索的最简单氢化物的沸点和稳定性均为H2Z>H2W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )

A.曲线①代表的粒子是HC2O4-
B.0.1 molL-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4)
C.pH=5时,溶液中主要含碳物种浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-)
D.一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用O2将HCl转化为Cl2,可提高效益,减少污染。
(1)传统上该转化通过如下图所示的催化剂循环实现,其中,反应①为:2HCl(g) + CuO(s)![]() H2O(g)+CuCl2(g) △H1,反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为_____________________, (反应热用△H1和△H2表示)。
H2O(g)+CuCl2(g) △H1,反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为_____________________, (反应热用△H1和△H2表示)。
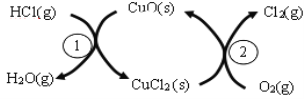
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性。

①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的αHCl—T(HCl的转化率与温度的关系)曲线如右图,则总反应的△H__________0,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是____________________。
②在上述实验中若压缩体积使压强增大,画出相应αHCl—T曲线__________,(在图中画出)并简要说明理由______________________。
③一定温度下,若该反应在某恒容容器中进行,下列能说明该反应已经达到化学平衡的是_________________________。
A、体系的压强不再改变
B、各反应物和生成物的浓度相等
C、混合气体的密度不再改变
D、混合气体的平均摩尔质量不再改变
(3)Cl2用途广泛,写出用Cl2制备漂白粉的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鲜花可以蒸制芳香油,油的主要成分为左旋香芳醇,含量最高可达千分之六,供食用及化妆品用,花瓣可以制饼馅、玫瑰酒、玫瑰糖浆,干制后可以泡茶,花蕾入药治肝、胃气痛、胸腹胀满。果实含丰富的维生素C、葡萄糖、果糖、蔗糖、枸橼酸、苹果酸及胡萝卜素等.β—紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是( )
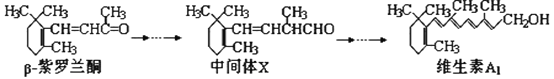
A. β—紫罗兰酮与中间体X互为同分异构体
B. 1mol维生素A1最多能与5molH2发生加成反应
C. 维生素A1易溶于NaOH溶液
D. β—紫罗兰酮不可使酸性KMnO4溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com