
科目: 来源: 题型:
【题目】氮化钠(Na3N)固体是一种重要的化合物,它与水反应可产生NH3。回答下列问题:
(1)Na3N属于________(填“共价”或“离子”)化合物,Na3N的电子式为________。
(2)Na3N与足量盐酸反应的化学方程式为________。
(3)比较Na3N中两种粒子的半径:r(Na+)________r(N3-)(填“>”“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】石油裂解可获得A。已知A在通常状况下是一种相对分子质量为28的气体,A通过加聚反应可以得到F,F常作为食品包装袋的材料。有机物A、B、C、D、E、F有如下图所示的关系。
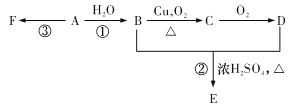
(1)A的分子式为________。
(2)写出反应①的化学方程式________;该反应的类型是________。写出反应③的化学方程式________。
(3)G是E的同分异构体,且G能与NaHCO3反应,则G的可能结构简式分别为________。
(4)标准状况下,将A与某烃混合共11.2L,该混合烃在足量的氧气中充分燃烧,生成CO2的体积为17.92L,生成H2O18.0g,则该烃的结构式为________;A与该烃的体积比为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家在-100 ℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键)。下列说法正确的是

A.X既能使溴的四氯化碳溶液褪色,又能使酸性KMnO4溶液褪色
B.X是一种常温下能稳定存在的液态烃
C.X和乙烷类似,都容易发生取代反应
D.充分燃烧等质量的X和甲烷,X消耗氧气较多
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。其中A为气体,A~F 都含有相同的元素。
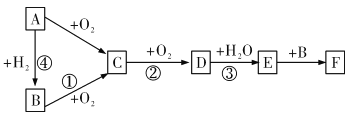
试回答下列问题:
(1)写出下列物质的化学式:C_______、F_______。
(2)在反应①中,34gB发生反应后放出452.9kJ的热量,请写出该反应的热化学方程式________。
(3)③的化学方程式为__________,该反应氧化剂与还原剂的物质的量之比为______。
(4)铜与E的浓溶液反应的离子方程式为__________ 。
(5)25.6g铜与含有1.4molE的浓溶液恰好完全反应,最终得到气体的体积为(标准状况下)__________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是
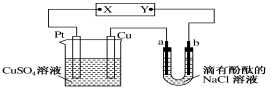
A.X极是电源负极,Y极是电源正极
B.Cu电极上增重6.4 g时,b极产生1.12 L(标准状况)气体
C.电解过程中CuSO4溶液的pH逐渐增大
D.a极的电极反应式为2Cl--2e-=Cl2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图所示。
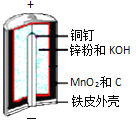
放电时总反应为:Zn + 2H2O + 2MnO2![]() Zn(OH)2 + 2MnOOH
Zn(OH)2 + 2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如下:
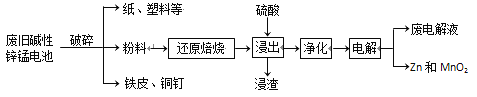
回答下列问题:
(1)MnOOH中,Mn元素的化合价为________。
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有________。
(3)“净化”是为了除去浸出液中的Fe2+,方法是:加入________(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀。(离子浓度小于1×10-5mol·L-1即为沉淀完全)已知浸出液中Mn2+、Zn2+的浓度约为0.1 mol·L-1,根据下列数据计算调节pH的合
理范围是________至________。
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
KSP近似值 | 10-13 | 10-17 | 10-38 |
(4)“电解”时,阳极的电极反应式为_____。本工艺中应循环利用的物质是_____(填化学式)。
(5)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为________。
(6)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80分钟即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有________%的金属锌未参加反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于 的表述不正确的是( )
的表述不正确的是( )
A. 该物质能发生缩聚反应
B. 该物质有7种不同化学环境的氢原子
C. 该物质遇FeCl3溶液显色,1 mol该物质最多能与含1 mol Br2的溴水发生取代反应
D. 1 mol该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为2∶2∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以烃A为原料生产人造羊毛的合成路线。

下列说法正确的是 ( )
A.合成人造羊毛的反应属于缩聚反应
B.A生成C的反应属于加成反应
C.A生成D的反应属于取代反应
D.烃A的结构简式为CH2===CH2
查看答案和解析>>
科目: 来源: 题型:
【题目】T℃时,在20.00 mL 0.10 mol·L-1CH3COOH溶液中滴入0.10 mol·L-1 NaOH溶液,溶液pH与NaOH溶液体积关系如图所示。下列说法正确的是

A. T℃时,CH3COOH电离平衡常数Ka=1.0×10-3
B. M点对应的NaOH溶液体积为20.0 mL
C. N点与Q点所示溶液中水的电离程度:N>Q
D. N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com