
科目: 来源: 题型:
【题目】某同学设计如下实验方案,以分离混合溶液中的AlCl3和FeCl2。

(1)沉淀A的化学式为________________ 。
(2)写出AlCl3溶液与过量NaOH溶液反应的离子方程式:___________________________。
(3)写出沉淀A转化为沉淀B反应的化学方程式:___________________。
(4)写出检验溶液A中是否含有Fe2+时的方法:________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关实验操作的叙述正确的是
A. 过滤操作中,漏斗的尖端不可接触烧杯内壁
B. 滴加试剂时,滴管的尖嘴不可接触试管内壁
C. 滴定接近终点时,滴定管的尖嘴不可接触锥形瓶内壁
D. 向容量瓶转移液体时,引流用玻璃棒不可接触容量瓶内壁
查看答案和解析>>
科目: 来源: 题型:
【题目】当今世界,能源的发展日益成为全世界、全人类共同关注的问题,乙烷、二甲醚的燃烧热较大,可用作燃料。如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
(1)乙烷的燃烧热ΔH= kJ·mol-1。
(2)等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量 (填“多”或“少”)。
(3)根据题图写出二甲醚完全燃烧时的热化学方程式 。
(4)二氧化碳是温室气体,从环保角度分析,放出相同的热量时选择 (填“乙烷”或“二甲醚”)作为燃料产生的CO2较少。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知还原性Cl-<Fe2+<H2O2<I-<SO2,下列反应不能发生的是
A. 2Fe3++SO2+2H2O===SO42-+4H++2Fe2+
B. I2+SO2+2H2O===H2SO4+2HI
C. H2O2+2H++SO42-===SO2↑+O2↑+2H2O
D. Cl2+2Fe2+===2Fe3++2Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】[2017北京节选]TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:
![]()
(1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2Cl2(g)TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol1
2C(s)+O2(g)2CO(g) ΔH2=220.9 kJ·mol1
① 沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:_______________________。
② 氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的ΔH_____0(填“>”“<”或“=”),判断依据:________________________________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJmol1。若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q1 kJ、Q2 kJ、Q3 kJ。则三者的由小到大关系是________(用Q1、Q2、Q3表示)。
(2)如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是_____________________; 若实验中不加盖泡沫塑料板,则求得的中和热数值______(填偏大、偏小、无影响)。

(3)实验室用50 mL 0.50 molL1盐酸、50 mL 0.55 molL1 NaOH溶液利用上图装置,进行测定中和热的实验。假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c=4.18 J/(g℃)。为了计算中和热,实验时还需测量的数据有(填序号)________。
A.反应前盐酸的温度 B.反应前盐酸的质量
C.反应前氢氧化钠溶液的温度 D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.4 |
2 | 20.2 | 20.4 | 23.6 |
3 | 20.5 | 20.6 | 23.8 |
依据该学生的实验数据计算,该实验测得的中和热ΔH为________。(保留三位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)=4Na+O2↑+2H2O;后来盖· 吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:Na++e-=Na
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数比为2:l
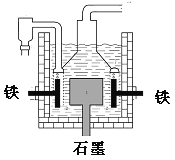
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关NO的说法不正确的是( )
A. NO可看作亚硝酸(HNO2)的酸酐 B. NO任意排放会造成大气污染
C. 实验室制取NO气体可用排水法收集 D. 氨催化氧化可生成NO
查看答案和解析>>
科目: 来源: 题型:
【题目】生物质资源是一种污染小的可再生能源。生物质的主要转化途径及主要产物如图所示。

(1)下列有关生物质能的说法正确的是_________。
a.生物质能本质上来源于太阳能
b.纤维素水解获得的产物中含有丰富的生物质能
c.生物质“热裂”获得的汽油、柴油等属于纯净物
d.将杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,可作家庭燃气
(2)由生物质能可获得CO和H2。等物质的量的CO与H2反应时,其原子利用率可达100%,则该反应合成的物质可能是_________。
a.汽油 b.甲醇(CH4O) c.甲醛(CH2O) d.乙酸(C2H4O2)
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列物质在水溶液中的电离方程式:
HCl:____________________;Ca(OH)2:_________________;
NH3·H2O:_________________;NH4NO3:_________________;
H2CO3:______________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com