
科目: 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是
①FeS2 ![]() SO2
SO2![]() H2SO4 ②SiO2
H2SO4 ②SiO2![]() SiCl4
SiCl4![]() Si
Si
③饱和NaCl![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
④Al![]() NaAlO2
NaAlO2![]() AlCl3(aq)
AlCl3(aq) ![]() AlCl3(s)
AlCl3(s)
⑤CuSO4(aq)![]() Cu(OH)2
Cu(OH)2![]() Cu2O
Cu2O
A. ①③⑤ B. ②③④ C. ②④⑤ D. ①④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】已知3.6 g碳在6.4 g氧气中燃烧,至反应物耗尽,测得放出热量a kJ。又知12.0 g碳完全燃烧,放出热量为 b kJ。则热化学方程式C(s)+![]() O2(g)===CO(g) ΔH=Q 中Q等于( )
O2(g)===CO(g) ΔH=Q 中Q等于( )
A. -(a-b) kJ·mol-1 B. -(a+b) kJ·mol-1
C. -(5a-0.5b) kJ·mol-1 D. -(10a-b) kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= +49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H= -192.9 kJ·mol-1
下列说法正确的是
A. CH3OH的燃烧热为192.9 kJ·mol-1
B. 反应①中的能量变化如图所示

C. CO2和H2转变成CH3OH的过程不一定要吸收能量
D. 根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H<-192.9kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组热化学方程式中化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)=CO2(g) ΔH1 C(s)+![]() O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)=SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+![]() O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO+H2O(l)===Ca(OH)2(s) ΔH8
A. ①③④ B. ②③④ C. ①④ D. ①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关金属腐蚀及防腐的叙述中,不正确的是( )
A.燃料电池电解质溶液显酸性时的正极反应为:2H2O+O2+4e-=4OH-
B.钢铁发生析氢腐蚀时,负极反应是 Fe-2e-=Fe2+
C.水中的钢闸门连接电源的负极是外加电流的阴极保护法
D.镀锌铁制品的镀锌层破损后对铁制品仍有保护作用,该保护法称为牺牲阳极的阴极保护法
查看答案和解析>>
科目: 来源: 题型:
【题目】水中Cl-的测定常用硝酸银滴定法,实验步骤及测定原理如下:
I.水样的预处理。
(1)如果水样带有颜色,则需要加入氢氧化铝胶体处理,利用了该胶体的_______性。
(2)如果水样耗氧量过高,则需要加入高锰酸钾晶体,煮沸后再加入少量乙醇处理,过程中高锰酸钾表现了______性,加入乙醇的目的是:______。
II.样品的测定。
将经过处理的水样置于锥形瓶中,加入少量的稀K2CrO4溶液做指示剂,用AgNO3 标准溶液滴定至砖红色沉淀(Ag2CrO4)刚好出现,且半分钟不消失时,即为滴定终点。已知Ksp(AgCl)=1.6 ×10-10,Ksp(Ag2CrO4)=9.0×10-12,Ksp(AgOH)=2.0×10-8。
(3)AgNO3 标准溶液置于棕色_______式滴定管中。
(4)实验中需严格控制水样的pH及指示剂的用量,如果pH过高,会使测定结果_____(填偏高、偏低或不变,下同),如果pH 过低,会使指示剂转化为 Cr2O72-而失效,如果指示剂过多会使测定结果________。
(5)取50.00mL水样,用浓度为cmol/ AgNO3标准溶液滴定,到达滴定终点时消耗的体积为VmL,则样品中Cl-的含量为_____mg/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】自然界氮的循环过程如图.回答下列问题。
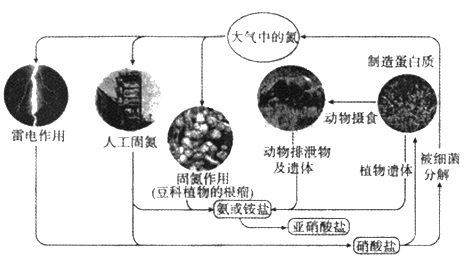
(1)上图中包含了_____种氮的固定方式,写出属于雷电作用固氮的化学方程式________。
(2)合成氮反应常用铁触媒催化剂,下列关于催化剂的说法不正确的是______。
A.可以加快反应速率 B.可以改变反应热
C.可以减少反应中的能耗 D.可以增加活化分子的数目
(3)氮的循环中,亚硝酸盐是重要的一环,利用化合价可推知亚硝酸盐具有_____性和_____性,亚硝酸盐和酸性高锰酸钾反应的离子方程式为__________________。
(4)某同学加热Fe(NO3)2时,发现得到了红色固体和红色气体,且所得气体被水充分吸收后体积少于原体积的l/3,Fe(NO3)2热分解的化学方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属Mg及其化合物有重要的用途,请回答下列问题
(1)MgO的重要用途有_______。(写出一种)
(2)井水中含有较多的Ca2+、Mg2+、HCO3-等离子,可以通过煮沸的方式将Mg2+转化为Mg(OH)2,发生的离子方程式是:__________________。
(3)金属Mg可以用来冶炼Ti:2Mg+TiCl4![]() Ti+2MgCl2。可以用作该反应保护气的是_______。
Ti+2MgCl2。可以用作该反应保护气的是_______。
A. He B. C02 C.N2 D.HCl
(4)在蒸发皿中放人研细的碘和镁粉,无现象,滴入几滴水后立即产生大量的紫烟,紫烟的成分是_________(填分子式);对于实验中水的作用,甲同学认为是水溶解了I2,增大了I2与Mg的接触面积,导致了反应加快,乙同学认为是I2与H2O反应生成了酸,是酸与Mg反应放出热量,加快了I2与Mg的反应,请利用供选试剂:0.01mol/L I2的CCl4溶液、0.01 mol/L I2水、I2粉、Mg粉、蒸馏水,设计实验证明哪位同学的说法合理:____________。(包括实验过程、现象和结论)
(5)一种新型的Mg-H2O2酸性介质电池工作原理如图,正极发生的电极方程式为:__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com