
科目: 来源: 题型:
【题目】常温下,物质的量浓度均为0.1mol·L-1的下列溶液:①Na2CO3溶液②NaOH溶液③NaHSO4溶液④NH4Cl溶液⑤NaNO3,溶液的pH由小到大的排列顺序是( )
A. ③<④<⑤<①<② B. ④<③<⑤<①<②
C. ④<③<①<⑤<② D. ①<④<③<⑤<②
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物. 请回答下列问题:;
(1)B的原子结构示意图;
(2)C、D、E三种原子对应的离子半径由大到小的顺序是(填具体离子);由A、B、C三种元素按4:2:3组成的化合物所含的化学键类型属于 .
(3)在100mL18mol/L的浓的A、C、E 组成酸溶液中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是;(填序号) a.7.32L b.6.72L c.20.16L d.30.24L
若使上述反应中剩余的铜片继续溶解,可向其中加入硝酸钠,反应的离子方程式为: .
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空: ,

(1)上述第一级分类标准(分成A、B组所依据)是______。
(2)C组物质为______________(填化学式)。
(3)D组物质中,与水反应时氧化剂和还原剂的物质的量之比为1:1的物质是_________(填化学式)。
(4)若E组和F组均有两种物质,则其分类依据是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式己配平): Cu+2H2SO4(浓)![]() CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成,则A应该属于______(填序号)
a.电解质 b.非电解质 c.硫化物 d.酸性氧化物 e.碱性氧化物
(2)A物质可以使酸性KMnO4溶液褪色,此反应中______(填写化学式,下同)失去电子,还原产物是______。
(3)一定量的铜片与100mL18mol/L的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的质量为______g,发生还原反应的硫酸的物质的量为___________mol。
(4)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。请写出此过程发生的反应的离子方程式:______、_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】N2H4是一种高效清洁的火箭燃料。8g N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是( )
A. ![]() N2H4(g)+O2(g)=== N2(g)+H2O(g) ΔH=267 kJ·mol-1
N2H4(g)+O2(g)=== N2(g)+H2O(g) ΔH=267 kJ·mol-1
B. N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
C. N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=534 kJ·mol-1
D. N2H4(g)+O2(g)===N2(g)+2H2O(l) ΔH=-133.5 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂对工业污泥中的Cr元素回收与再利用的工艺如下(己知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3* | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时 的pH | 1.9 | 7.0 | — | 一 | — |
沉淀完全时 的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(1)实验室用98% (密度为1.84 g·cm-3)的浓硫酸配制200mL4.8 mol·L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为_________mL (保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒外,还需__________________________________。
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏小的操作是____________________(填序号)
a.定容时俯视刻度线 b.量取浓硫酸时,俯视刻度线
c.当容置瓶中液体占容积2/3左右时,未振荡摇匀 d.转移溶液时,没有等溶液冷却至室温
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是_____________________________。(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是___________________。
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是_____________________。
(6)通SO2气体时,还原过程发生以下反应(填写缺项物质并配平)
____________________________________________________________Na2SO4.
查看答案和解析>>
科目: 来源: 题型:
【题目】炼丹是古人为追求长生而炼制丹药的方术。晋人葛洪《抱朴子·金丹篇》记载:“凡草木烧之即烬,而丹砂(硫化汞)烧之成水银,积变又还成丹砂”。其中未涉及到的反应类型
A. 化合反应B. 分解反应C. 氧化还原反应D. 置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】氢能源是21世纪极具开发前景的新能源之一,它既是绿色能源,又可循环使用。如图是氢能源循环体系图(X是H2O;Y是H2、O2)。回答下列问题:
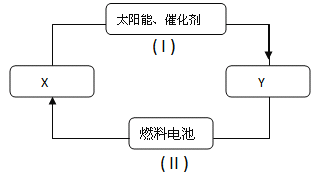
(1)从能量转换的角度看,过程II主要是将___能转化为____ 能。
(2)在该燃料电池中,H2所在的一极为_____极;若电解质溶液为碱性的KOH溶液,试写出两极的电极方程式:正极_______负极______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com