
科目: 来源: 题型:
【题目】有A、B、C、D、E五种烃,具有下列性质:
①各取0.1mol分别充分燃烧,其中B、C、E燃烧所得的CO2均为4.48L(标准状况),A和D燃烧所得的CO2都是前三者的3倍;
②在适宜条件下,A、B、C都能跟氢气发生加成反应,其中A可以转化为D、B可以转化为C,C可以转化为E;
③B和C都能使溴水或酸性KmnO4溶液褪色,而A、D、E无此性质;
④用铁屑作催化剂时,A可与溴发生取代反应.
判断A、B、C、D、E各是什么物质,写出结构简式ABCDE .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于元素周期表的叙述正确的是
A. 元素周期表中有18列,即18个族
B. 目前使用的元素周期表中,最长的周期含有32种元素
C. 短周期元素是指1~20号元素
D. 原子的种类和元素的种类一样多
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物;E的阳离子与A的阴离子核外电子层结构相同.请回答下列问题: 
(1)A在元素周期表中的位置 .
B的最高价氧化物化学式为 .
写出C元素气态氢化物的电子式 .
(2)D的单质与水反应的化学方程式为 .
(3)五种元素中原子半径最小的是(填元素符号),这些元素的最高价氧化物的对应水化物中酸性最强.
(4)C的一种氧化物是常见的大气污染物.为防止大气污染,某化工厂用NaOH溶液、石灰和O2处理含C的上述氧化物的尾气,使其转化为石膏(CaSO42H2O).假设在转化过程中C元素不损失,每天处理1120m3(标准状况下)含2%(体积分数)上述氧化物的尾气,理论上可以得到多少千克石膏(请写出计算过程).
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上制取氯酸钾的主要步骤为:
I.将Cl2通入石灰浆,在75℃左右充分反应,然后过滤;
II.向滤液中加入稍过量的KCl固体,进行适当操作可析出KClO3固体。
请回答下列问题:
(1)步骤I中总反应的化学方程式为6Ca(OH)2+ 6Cl2=Ca(ClO3)2+5CaCl2+ 6H2O 。
①标出反应中电子转移的方向和数目______________。
②滤液中Ca(ClO3)2与CaC12的物质的量之比n[Ca(ClO3)2]:n [CaCl2]____l∶5 (填“> ”“< ”、或“=” ) ,理由是___________。
(2)下图是有关物质的溶解度曲线。步骤II中,若溶液中KClO3的含量为147g·L-1,则KClO3得物质的量浓度为_______________。从该溶液中尽可能多地析出KClO3 固体的方法是______________。

查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某溶液中Ca2+的含量,某冋学设计了如下实验:量取100 mL该溶液于烧杯中,加入足量的(NH4)2C2O4溶液使Ca2+转化为CaC2O4沉淀(假设其他离子均不生成沉淀),过滤、洗涤后,往沉淀中加入足量稀硫酸,然后用0.1000molL-1的KMnO4标准溶液滴定。
(1)配平KMnO4氧化H2C2O4的化学方程式:____________________
(2)如图所示的仪器中,配制0.1000molL-1的KMnO4标准溶液时肯定不需要的是___(填标号),除此之外还需用到的玻璃仪器是___(填仪器名称)。
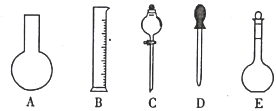
(3)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___0.1000molL-1(填“>”、“<”或“=”,下同);若KMnO4标准溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___0.1000molL-1。
(4)若滴定过程中消耗KMnO4标准溶液20.00mL,则原溶液中Ca2+的质量浓度为___gL-1。
(5)下图为草酸钙固体在受热分解过程中所得固体产物的质量随温度变化的曲线,图中A、B、C分别代表三种固体,写出固体A到B的化学方程式:_________________________。
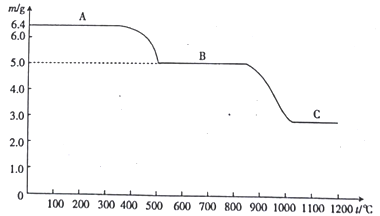
查看答案和解析>>
科目: 来源: 题型:
【题目】在带有活塞的密闭容器中发生反应:Fe2O3(s)+3H2(g)=2Fe(s)+3H2O(g),采用下列措施不能改变反应速率的是
A. 加热 B. 保持容器体积不变,增加通入H2的量
C. 充入N2,保持容器内压强不变 D. 充入N2,保持容器内体积不变
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,H2O2在水溶液中发生分解反应:2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
反应过程中,测得不同时间H2O2的物质的量浓度如表:
t/min | 0 | 20 | 40 | 60 | 80 |
c(H2O2)/molL﹣1 | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |
(1)H2O2的分解反应氧化还原反应(填“是”或“不是”).要加快该反应的速率,可采取的方法有 .
(2)该分解反应0─20min的平均反应速率v(H2O2)为molL﹣1 min﹣1 .
(3)如果反应所用的H2O2溶液为100mL,则共产生O2g.
A.0.08
B.0.16
C.1.2
D.2.4.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com