
科目: 来源: 题型:
【题目】氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。回答下列问题:
(1)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表:
t/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
在200℃时,当测得NH3和N2、H2的物质的量分别为1mol和0.5mol、1mol时,则该反应的v(N2)正____v(N2)逆(填写“>”、“=”或“<”)。
(2)结合表中给出的电离常数回答下列问题:
酸或碱 | CH3COOH | HNO2 | HCN | HClO |
电离平衡常数(Ka或Kb) | 1.8×10-5 | 4.6×10-4 | 5×10-10 | 3×10-8 |
①上述四种酸中,酸性最弱、最强的酸分别是_______、____(用化学式表示)。
②下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是____(填序号)。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸 E.加氢氧化钠固体
③依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。

①作负极的物质是__________。
②正极的电极反应式是__________。
(2)将足量铁粉投入水体中,经 24小时测定 NO3-的去除率和pH,结果如下:
初始 pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近 100% | <50% |
24 小时 pH | 接近中性 | 接近中性 |
铁的最终物质 形态 |
|
|
pH=4.5 时,NO3-的去除率低,其原因是_____________。
(3)实验发现:在初始 pH=4.5 的水体中投入足量铁粉的同时,补充一定量的 Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏 FeO(OH)氧化层。
①做对比实验,结果如图所示,可得到的结论是________。

②同位素示踪法证实 Fe2+能与 FeO(OH)反应生成 Fe3O4。结合该反应的离子方程式,解释加入 Fe2+提高NO3-去除率的原因:_____________。
(4) 其他条件与(2)相同,经 1小时测定NO3-的去除率和 pH,结果如下:
初始 pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始 pH不同时,NO3-去除率和铁的最终物质形态不同的原因:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】用50mL 0.25mol/LH2SO4溶液与50mL 0.55mol/LNaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:

(1)①烧杯间填满碎泡沫塑料的作用是_____________。
②若大烧杯上改为盖薄铁板,求得的反应热数值:_______(填“偏大”、“偏小”或“无影响”)。
③若通过测定计算产生的热量为1.42kJ,请写出表示中和热的热化学方程式:____________。
(2)上述实验数值与57.3 kJ/mol有偏差,产生偏差的原因可能是______(填字母)。
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液例入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(3)①已知:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2 kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4 kJ/mol
则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:____________。
②由气态基态原子形成1 mol化学键释放的最低能量叫键能。已知表中所列键能数据,则NH3(g)![]() l/2N2(g)+3/2H2(g) △H=_________kJ/mol。
l/2N2(g)+3/2H2(g) △H=_________kJ/mol。
化学键 | H-H | N-H | N≡N |
键能kJ/mol | 436 | 391 | 945 |
查看答案和解析>>
科目: 来源: 题型:
【题目】以下物质间的每步转化通过一步反应能实现的是( )
A.Al→Al2O3→Al(OH)3→NaAlO2
B.Si→SiO2→H2SiO3→Na2SiO3
C.N2→NO→NO2→HNO3
D.S→SO3→H2SO4→MgSO4
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂综合处理含 NH4+废水和工业废气(主要含 N2、CO2、SO2、NO、CO,不考虑其他成分),设计的流程如下图,回答下列问题:
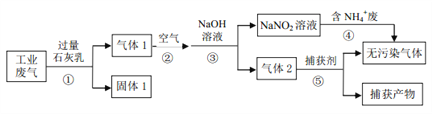
(1)固体 1的主要成分有______(填化学式)。
(2)反应①需控制反应的温度和气体的流速,其共同目的是______。
(3)反应④的离子方程式为______。
(4)已知:2NO2+2NaOH=NaNO3+NaNO2+H2O,NO2+NO+2NaOH=2NaNO2+H2O
在同温同压下,当反应②中NO与空气的体积比为______,经反应③,气体中NOx被完全吸收且仅生成 NaNO2。(设空气中氧气所占体积分数为 0.2)
(5)CuCl 的氨溶液常用作反应⑤的捕获剂。将(NH4)2SO3、NH4Cl与CuSO4 3种溶液相混可制得难溶物 CuCl。
① 理论上,(NH4)2SO3与CuSO4恰好反应时,n(SO32-):n(Cu2+)=______。
② 实际上, (NH4)2SO3的用量与 Cu2+的沉淀率关系如图所示,显然Cu2+沉淀率最高时,(NH4)2SO3的用量高于理论值其原因是______。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.甲酸乙酯和食用植物油均可水解
B.蛋白质、乙酸和糖类均属电解质
C.溴乙烷与NaOH水溶液共热生成乙烯
D.乙醇和乙醛都可以发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 1 mol氯含有6.02×1023个微粒
B. 阿伏加德罗常数的数值约等于6.02×1023
C. 钠的摩尔质量等于它的相对原子质量
D. H2O的摩尔质量是18 g
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关金属的说法正确的是( )
A. 生铁与钢的区别在于生铁含碳杂质,而钢不含
B. 铜在自然界中的含量高,所以铜是人类最早使用的金属
C. 黑色金属材料包括铁、铬、锰及其化合物
D. 金属一般都具有导电性、导热性、延展性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com