
科目: 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g·100mL-1)。
Ⅰ.实验步骤
(1)配制100ml待测白醋溶液:用 (填仪器名称)量取10.00 mL食用白醋,在烧杯中用水稀释后转移到 (填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴 作指示剂。
![]()
(3)读取盛装0.1000 mol·L-1 NaOH 溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________mL。
(4)滴定。当___________________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00[ | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(1)按实验所得数据,可得c(市售白醋)= mol·L-1;
市售白醋总酸量= g·100 mL-1。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是________填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
科目: 来源: 题型:
【题目】我国的“神州七号”载人飞船已发射成功,“嫦娥”探月工程已正式启动.据科学家预测,月球的土壤中吸附着数百万吨的 ![]() He,每百吨
He,每百吨 ![]() He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以
He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以 ![]() He的形式存在.下列说法正确的是( )
He的形式存在.下列说法正确的是( )
A.![]() He原子核内含有4个质子
He原子核内含有4个质子
B.![]() He和
He和 ![]() He互为同位素
He互为同位素
C.![]() He原子核内含有3个中子
He原子核内含有3个中子
D.![]() He的最外层电子数为2,所以
He的最外层电子数为2,所以 ![]() He的化学性质活泼
He的化学性质活泼
查看答案和解析>>
科目: 来源: 题型:
【题目】“保护环境”是我国的基本国策.下列做法不应该提倡的是( )
A. 化石燃料脱硫、脱硝处理 B. 工业废水经处理达标排放
C. 废电子产品统一回收处理 D. 农作物秸秆就地露天焚烧
查看答案和解析>>
科目: 来源: 题型:
【题目】关于石油化工的说法不正确的是( )
A.通过石油分馏得到石蜡、沥青等重油
B.石油分馏所得的各种馏分是纯净物
C.石油是各种碳氢化合物组成的混合物
D.通过重油裂化得到相对分子量较小、沸点较低的轻质燃料油
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.2LNaCl、MgCl2的混合溶液中,部分离子浓度大小如图所示,回答下列问题: 
(1)该混合溶液中,Na+的物质的量为mol,MgCl2的物质的量为mol,Cl﹣的物质的量为mol.
(2)该混合溶液中含溶质的总质量为g.
(3)将该混合溶液加水稀释至体积为 1L,稀释后溶液中Cl﹣的物质的量浓度为molL﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】NH4Al(SO4)2·12H2O (铵明矾) 可用作泡沫灭火器的内留剂、石油脱色剂等。用氧化铁和铝粉等物质做铝热反应后的铝灰及硫酸铵等为原料制备铵明矾的实验步骤如下:
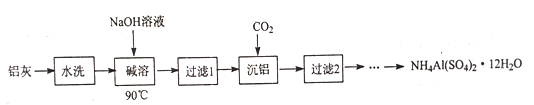
(1) 铝灰用“水洗”的目的是______碱溶时,需在约90℃条件下进行,适宜的加热方式为_____。
(2)“过滤1”所得滤渣主要成分为_________。
(3)用下图左边装置制备CO2时,适宜的药品A 为________、B 为__________;“沉铝”时,通入过量CO2 发生反应的离子方程式为________。
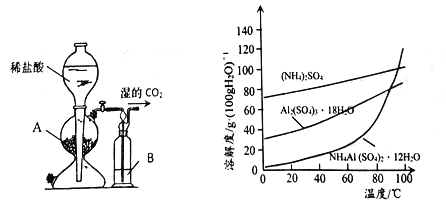
(4)请设计从“过滤2”所得滤渣制取铵明矾的实验方案: 称取一定质量“过滤2”的滤渣,放入烧杯中,____,静置,过滤、洗涤、晾干,得到NH4Al(SO4)2·12H2O [实验中须使用到3mol/L硫酸、(NH4)2SO4、蒸馏水、氨水、pH 试纸; 已知: NH4Al(SO4)2饱和溶液的pH约为1.5,几种物质的溶解度曲线见右上图]。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com