
科目: 来源: 题型:
【题目】在无色透明溶液中,能大量共存的离子组是
A. Mg2+、Na+、SO42- B. K+、H+、HCO3-
C. Cu2+、NO3-、SO42- D. Ba2+、NO3-、CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).B和C的相对分子质量相差16,化合物D是重要的工业原料.
I.单质A的名称 .
II.写出D的浓溶液与Cu加热反应生成B的化学方程式 . 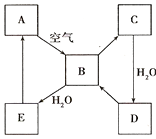
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的用途与利用的性质对应关系不正确的是( )
A | B | C | D | |
物质 | 漂白液 | 碱石灰 | 铁红 | 单晶硅 |
主要成份 | NaClO | 氧化钙与氢氧化钠 | Fe2O3 | Si |
用途 | 消毒剂 | 干燥剂 | 红色油漆或涂料 | 光导纤维 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】有如图所示装置,为实现下列实验目的,其中Y端适合于作入口的是 .
A.瓶内盛液体干燥剂,用以干燥气体
B.瓶内盛液体洗涤剂,用以除去某气体中的杂质
C.瓶内盛水,用以测量某难溶于水的气体的体积
D.瓶内贮存气体,加水时气体可被排出
E.收集密度比空气大的气体
F.收集密度比空气小的气体.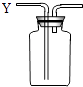
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钛性能优越,被称为继铁、铝之后的“第三金属”,工业上用钛矿石(主要成分:FeO、TiO2、SiO2等)为原料制取钛并得到副产物绿矾(FeSO4·7H2O),工艺流程如下,回答下列问题:

己知:①TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O(l)
②TiO2+易水解,只能存在于强酸性溶液中
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是_____________。
(2)加入过量铁粉的目的是_____________。
(3)固体2的主要成分是_____________。
(4)请用化学平衡移动原理解释溶液2加热煮沸的目的_____________。
(5)在高温下,TiO2和焦炭的混合物中通入Cl2得到TiC14和一种可燃性气体,请写出反应的化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组用下图装置制取并探究氯气的性质。[A装置中发生反应的化学方程式:2KMnO4+16HCl(浓) == 2KCl+2MnCl2 + 5Cl2↑+ 8H2O ]

【实验探究】
(1)A装置中a仪器的名称是_____________。
(2)制取氯气反应中KMnO4所起的作用是_____(填“氧化剂”或“还原剂”)。
(3)实验进行一段时间后,可观察到______(填“B”或“C”)装置中有色布条褪色,其褪色原因是______________________________________。
(4)当氯气进入D装置后,可观察到溶液颜色变为_______(填“红色”或“蓝色”),写出相关反应的化学方程式___________________________________。
(5)E装置中NaOH溶液的作用是_____________________________________。
(6)用31.6 g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下_____L氯气。(KMnO4的摩尔质量为158 g·mol—1)
【知识拓展】
(7)近年来,某些含氯的化合物(如ClO2、NaClO等)在生产、生活中应用广泛。
①高效净水剂ClO2中氯元素的化合价为_____________。
②NaClO是一种强氧化剂。某种家用洗涤剂含有NaClO,请写出NaClO在洗涤过程中的一种作用___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化硅属于酸性氧化物,理由是
A. Si是非金属元素 B. SiO2对应的水化物是可溶性弱酸
C. SiO2与强碱反应生成盐和水 D. SiO2不能与酸反应
查看答案和解析>>
科目: 来源: 题型:
【题目】H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了图1、图2两种实验装置. 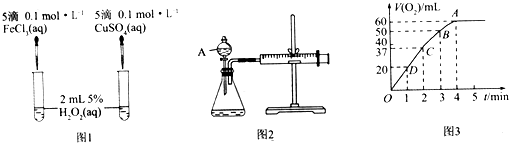
(1)若利用图1实验,可通过观察产生气泡的快慢定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是 , 写出H2O2在二氧化锰催化作用下发生反应的化学方程式: . 若利用图2实验可进行定理分析,图中仪器A的名称为 , 实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是 .
(2)将0.1mol MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示,解释反应速率变化的原因: , H2O2初始物质的量浓度为(保留两位有效数字).
(3)为了加深同学们对影响反应速率因素的认识,老师让同学完成如下实验:
在上述实验装置的锥形瓶内加入6.5g锌粒,通过分液漏斗加入40mL 2.5molL﹣1的硫酸,10s时收集到产生的H2的体积为44.8mL(标准状况),用硫酸表示10s内该反应的速率为molL﹣1s﹣1(假设反应前后溶液的体积不变).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com