
科目: 来源: 题型:
【题目】中国是瓷器的故乡,钧瓷是宋代五大名窑瓷器之一,以“入窑一色出窑万彩”的神奇窑变著称。下列关于陶瓷的说法正确的是( )
A.高品质的白瓷晶莹剔透,属于纯净物
B.瓷器中含有大量的金属元素,因此陶瓷属于金属材料
C.氮化硅陶瓷属于传统无机非金属材料
D."窑变"是高温下釉料中的金属化合物发生氧化还原反应导致颜色的变化
查看答案和解析>>
科目: 来源: 题型:
【题目】H2O2作为氧化剂在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题:
(1)定性分析:图甲可通过观察________________定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是_______________________。

(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为_______,检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看__________,实验中需要测量的数据是__________。
(3)加入MnO2粉末于H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

由D到A过程中,随着反应的进行反应速率逐渐_________。(填 “加快”或“减慢”),其变化的原因是_____________。(选填字母编号)
A.改变了反应的活化能 B.改变活化分子百分比
C.改变了反应途径 D.改变单位体积内的分子总数
(4)另一小组同学为了研究浓度对反应速率的影响,设计了如下实验设计方案,请帮助完成(所有空均需填满)。
实验编号 | T/K | 催化剂 | 浓度 |
实验1 | 298 | 3滴FeCl3溶液 | 10ml 2%H2O2 |
实验2 | 298 |
① 在实验2中依次填_______________、________________。
② 可得到的结论是浓度越大,H2O2 分解速率__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】磷是人体含量较多的元素之一,磷的化合物在药物生产和农药制造等方面用途非常广泛。回答下列问题:
(1)基态磷原子的核外电子排布式为____________________。
(2)P4S3可用于制造火柴,其分子结构如图甲所示。

①第一电离能:磷_____________硫;电负性:磷_____________硫(填“>”或“<”)。
②P4S3分子中硫原子的杂化轨道类型为_____________。
③每个P4S3分子中含孤电子对的数目为______________。
(3)N、P、As、Sb均是第VA族的元素。
①上述元素的氢化物的佛点关系如图乙所示,沸点:PH3<NH3,其原因是____________;沸点:PH3<AsH3<SbH3,其原因是______________________________________。

②某种磁性氮化铁的晶胞结构如图丙所示,该化合物的化学式为______。
(4)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图丁所示。
①磷化铝晶体中磷与铝微粒间的作用力为_____________________。
②图中A点和B点的原子坐标参数如图丁所示,则C点的原子坐标参数为________。
③磷化铝晶体的密度为ρg·cm-3,用NA表示阿伏加德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为___________cm。
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年以来我国北方的“雾霾”污染日益严重。中科院“大气灰霾追因与控制”项目针对北京强霾过程进行分析,强霾过程中,出现了大量有毒有害的含氮有机颗粒物。燃煤和机动年尾气是氮氧化物的主要来源。现在对其中的一些气体进行了一定的研究:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1
②OCH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ·mol-1
③H2O(g)=H2O(1)△H=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式_________________________。
(2)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程中NO的物质的量随时间变化如下图所示。

①写出该反应的化学方程式:________________________________。
②10min内该反应的速率v(N2)=___________;该反应达平衡时CO的转化率为___________;T℃时该化学反应的平衡常数K=___________。
③若该反应△H<0,在恒容的密闭容器中,反应达平衡后,改变某一条件,下列示意图正确的是________。

④一定温度下,在恒容密闭容器中充入一定量NO和CO进行该反应,能判断反应已达到化学平衡状态的是____________。
a.容器中压强不再变化 b.CO2的浓度不再改变
c.2v正(NO)=v逆(N2) d.气体的密度保持不变
(3)以燃料电池为代表的新能源的推广“使用能大大降低污染物的排放。如图是一种甲醚燃料电池结构,请写出该电池负极的电极反应式:________________________________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应:2Na2O2 + 2H2O === 4NaOH + O2,下列说法中正确的是 ( )
A. Na2O2是氧化剂,H2O是还原剂
B. Na2O2既是氧化剂,又是还原剂
C. 该反应中电子转移的数目为4e-
D. O2既是氧化产物,又是还原产物
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物H是合成抗心律失常药物决奈达隆的一种中间体,可通过以下方法合成:
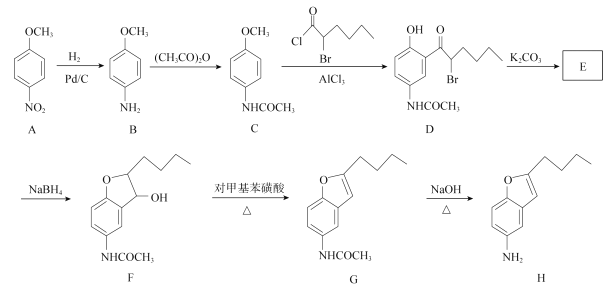
(1))D中的含氧官能团名称为________________(写三种)。
(2)F→G的反应类型为____________。
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:_______________________。
①能发生银镜反应
②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应
③分子中只有4种不同化学环境的氢。
(4)E经还原得到F,E的分子式为C14H17O3N,写出E的结构简式:________________________。
(5)已知:
①苯胺(![]() )易被氧化。
)易被氧化。
②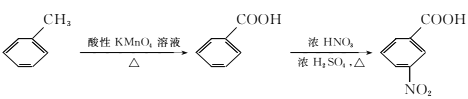
请以甲苯和(CH3CO)2O为原料制备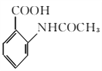 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。 ______________________
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。 ______________________
查看答案和解析>>
科目: 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。
请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
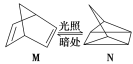 ΔH=+88.6 kJ·mol-1
ΔH=+88.6 kJ·mol-1
则M、N相比,较稳定的是 。
(2)已知CH3OH(l)的燃烧热为238.6 kJ·mol-1,CH3OH(l)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a 238.6(填“>”、“<”或“=”)。
O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a 238.6(填“>”、“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式: 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com