
科目: 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如右图所示,图中有机废水中有机物可用C6Hl0O5表示。下列有关说法正确的是( )

A. 电解精炼铜应将粗铜连接在a电极上
B. b电极附近溶液的pH减小
C. 中间室:Na+移向左室,Cl-移向右室
D. a电极反应式C6H10O5-24e-+7H2O=6CO2↑+24H+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A. 溶于水能导电的化合物一定是离子化合物
B. 在共价化合物中一定含有共价键
C. 含有共价键的化合物不一定是共价化合物
D. 离子化合物中不一定都含有金属元素
查看答案和解析>>
科目: 来源: 题型:
【题目】同温同压下,四个等体积的干燥圆底烧瓶中分别充满:①NH3②HCl(混有少量空气),③NO2 , ④NO2和O2(4:1)的混合气体,进行喷泉实验,经充分反应后,圆底瓶内溶液的物质的量浓度为(设溶质不扩散)( )
A.①>②>③>④
B.①=②=③=④
C.①=②=③>④
D.①>②>③=④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关图示说法不正确的是( )

A. 某温度将n mol/L醋酸溶液滴入10mL 1.0mol/L NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化如图甲,则n> 1.0
B. 恒容密闭容器中充入一定量NO和足量碳反应.C(s)+2NO(g)![]() CO2(g)+N2(g),平衡时c(NO)与温度关系如图乙,则B、
CO2(g)+N2(g),平衡时c(NO)与温度关系如图乙,则B、
C. D点压强为PC=PD>PB
C. 25℃时向100mL0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液的pH与NaOH溶液体积关系曲线如图丙,则a点到b点过程中,溶液导电能力减弱
D. 图丁装置(电极均为惰性电极)可吸收SO2,其阴极反应式为2HSO3-+2e-+2H+=S2O42-+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应及其应用在化学中占有重要地位。回答下列各题。
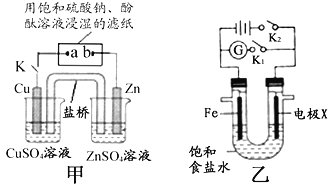
(1)写出铝与氢氧化钠溶液反应的离子方程式____________________;若将镁条、铝条和灵敏电流计用导线相连,使镁条、铝条浸入氢氧化钠溶液中,电流计指针发生偏转时,负极材料为________。
(2)当闭合K时,甲装置中Zn极的电极反应式为____;电子流动的方向为______;若盐桥中填充KCl琼脂,K+离子移动的方向为______;a极的电极反式为________;一段时间后,b极附近的现象为____________________。
(3)装置乙中。
①断开K2,接通K1。当X为石墨电极,Fe极的电极反应式为_________;当X为锌电极,Fe极的电极反应式为_____________。
②断开K1,接通K2。若X为石墨电极,X极的电极名称为_____;装置反应的离子方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】近期发现,H2S是继NO、CO之后第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)在密闭容器中充入一定量的H2S,发生反应2H2S(g)![]() 2H2(g)+S2 (g) 如图为H2S的转化率与温度、压强的关系。
2H2(g)+S2 (g) 如图为H2S的转化率与温度、压强的关系。
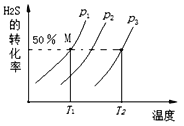
①该反应的ΔH__________0(填“>”、“=”或“<”);
②图中压强(p1、p2、p3)由小到大的顺序为_____________________;
③图中M点的平衡常数KP=_______________(KP是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)羰基硫(COS)是一种粮食熏蒸剂,能有效防止粮食被某些昆虫、线虫和真菌危害。在2 L的密闭容器中,保持温度T不变,将CO和H2S混合,并达下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.2。开始投入9 molH2S和a mol CO,经10 min达到平衡。
COS(g)+H2(g) K=0.2。开始投入9 molH2S和a mol CO,经10 min达到平衡。
①若达平衡时n(H2S)=5mol,a 为_______。平衡时CO的转化率为________。
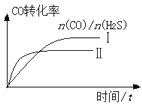
②曲线Ⅰ和Ⅱ表示该温度下,CO和H2S投料比[n(CO)/ n(H2S)]不同时,CO转化率随时间变化图像。则曲线Ⅰ和Ⅱ中a值的大小关系为:Ⅰ___Ⅱ(填“大于”“等于”“小于”),理由是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com