
科目: 来源: 题型:
【题目】(1)为测定一种气态烃A的化学式,取标准状况下一定体积的A置于密闭容器中,再通入一定体积的O2,用电火花引燃,定性实验表明产物是CO2、CO和水蒸气。相关方案如下:(箭头表示气体流向,实验前系统内空气已排除)
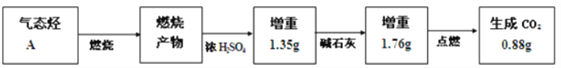
试回答(不要求写计算过程):A的实验式(最简式)是____________,根据所学知识,气态烃A的分子式为___________。
(2)质子核磁共振(PMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中,每一个结构中的等性氢原子的PMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中的等性氢原子数成正比。现有某有机物,化学式为C6H12。已知该物质可能存在多种结构,a、b、c是其中的三种,请根据下列要求填空:
①a与氢气加成生成2―甲基戊烷,则a的可能结构有___________种。
②b能使溴水和酸性高锰酸钾褪色,PMR谱中只有一个信号,则b的结构简式为:__________________,其命名为:______________。
③c不能使酸性高锰酸钾溶液褪色,不能与溴水加成褪色,可萃取溴水中的溴;PMR谱中也只有一个信号,则c的结构简式为:___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现通过以下步骤由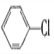 制备
制备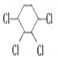
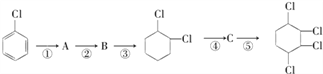
(1)写出A、B的结构简式:A_________, B________。
(2)从左到右依次填写每步反应所属的反应类型____________(a.取代反应;b.加成反应;c.消去反应。只填字母代号)。
(3)写出反应A→B所需的试剂和条件:_____________。
(4)写出④和⑤的化学方程式___________________,________________。
查看答案和解析>>
科目: 来源: 题型:
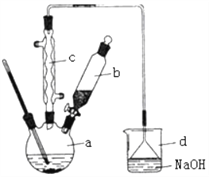
【题目】Ⅰ.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按以下步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL 液态溴。向a中滴入几滴溴,a中液体立即沸腾,并有红棕色蒸气出现;a中发生的化学方程式为_______________________;继续滴加至液溴滴完。仪器a的名称是___________装置d中的作用是_______________________。仪器c为冷凝管,其进水口为__________________(填“上”或“下”)口。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_______________________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_______________________。
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为____,要进一步提纯,下列操作中必须的是____。
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列空白。
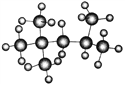
(1)“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,右图是异辛烷的球棍模型,则异辛烷的系统命名为_____________。
(2)写出下列反应的化学方程式
① 2,5-二甲基-2,4-己二烯与足量氢气加成:_____________________________
② 2-甲基-2-丁烯加聚反应___________________
③ 甲苯在一定条件下生成三硝基甲苯:________________________________
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3 + HBr → CH3CHBrCH3 + CH3CH2CH2Br
(主要产物) (次要产物)
A是一种不对称烯烃,与HBr加成时,生成的主要产物为B,且B中仅含有4个碳原子、1个溴原子、1种氢原子。则B的结构简式为 ___________,A的结构简式_______________
查看答案和解析>>
科目: 来源: 题型:
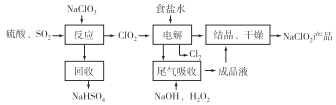
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其中一种生产工艺如下图所示,回答下列问题:
(1)NaClO2中Cl元素的化合价为_______。
(2)ClO2的沸点为11℃,纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下更安全。写出“反应”步骤中生成ClO2的化学方程式:___________________。
(3)“电解”过程中阴极的主要电极反应式为__________________。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。
①此吸收反应中,还原剂与氧化剂的物质的量之比为________。(填字母代号)。
②提高尾气的吸收效率的可行措施有_______________。
A.“尾气吸收”时充分搅拌吸收液 B.适当加快尾气的通入速率
C.将温度控制在20C以下 D.加水稀释尾气吸收液
③在“尾气吸收”过程中,可代替H2O2的最佳试剂是______(填字母代号)。
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
(5)ClO2和H+结合为HClO2,HClO2是唯一的亚卤酸,不稳定,易分解产生Cl2、ClO2和H2O,写出HClO2分解的化学方程式:___________________。
(6)已知NaClO2的溶解度随温度升高而增大,NaClO2饱和溶液在38℃以上60℃以下会析出NaClO2,在NaClO2析出过程中可能混有的杂质是________(任写一种,填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( ) 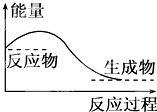
A.任何化学反应都伴随着能量的变化
B.H2O(g)═H2O(l)该过程放出大量的热,所以该过程是化学变化
C.化学反应中能量的变化都表现为热量的变化
D.对于如图所示的过程,是吸收能量的过程
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 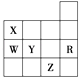
A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物还原性小于Y的氢化物
D.Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com