
科目: 来源: 题型:
【题目】现有下列九种物质:①H2 ②铝 ③CuO ④CO2⑤H2SO4 ⑥Ba(OH)2固体⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)上述状态下可导电的是;
属于电解质的是;
属于非电解质的是 .
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为 .
(3)⑨在水中的电离方程式为 , 34.2g ⑨溶于水配成250mL溶液,SO42﹣的物质的量浓度为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1 160 kJ·mol-1
下列说法不正确的是( )
A. 反应①②均为放热反应
B. 等物质的量的甲烷分别发生反应①②,转移电子数相同
C. 由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ·mol-1,a<574
D. 若用标准状况下4.48 L CH4还原NO2至N2,放出的热量为173.4 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】图1表示酶和催化剂改变化学反应速率的原理,图2表示加入抑制剂对起始反应速率的影响。酶的抑制剂是与酶结合并降低酶活性的分子。竞争性抑制剂与底物竞争酶的活性部位,非竞争性抑制剂和酶活性部位以外的其他位点结合,从而抑制酶的活性。请回答下列问题。
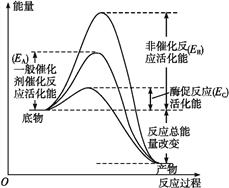 图1
图1 图2
图2
(1)由图1可知,该酶降低的活化能是______(用图中字母表示),与无机催化剂相比______________________,因而催化效率更高。
(2)活细胞产生酶的场所有________,需要的原料是________。
(3)图2中对照组是____曲线的结果,其中b为加入_____抑制剂的曲线,判断理由是_________________。请在图2中画出加入该酶的激活剂的曲线。________________
(4)信号肽假说认为,编码分泌蛋白的mRNA在翻译时首先合成的是N末端带有疏水氨基酸残基的信号肽,它被内质网膜上的受体识别并与之相结合。信号肽经由膜中蛋白质形成的孔道到达内质网内腔,但蛋白质转到高尔基体加工时却没有了该信号肽序列。据此我们可以推断内质网中可能存在的酶及作用是_______________。
(5)蛙的红细胞合成酶所需要的ATP主要由_______(过程)产生。
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2既是温室气体,也是重要的化工原料。以CO2为原料可合成多种物质。
(1)利用CO2和CH4重整可制合成气(主要成分CO、H2),重整过程中部分反应的热化学方程式为:
①CH4(g) = C(s) + 2H2(g) △H = +75.0 kJ·mol1
②CO2(g) + H2(g) = CO(g) + H2O(g) △H = +41.0 kJ·mol1
③CO(g) + H2(g) = C(s) + H2O(g) △H = -131.0 kJ·mol1
反应CO2(g) + CH4(g) = 2CO(g) + 2H2(g)的△H= ____。
(2)在一定温度下,向2L固定容积的密闭容器中通入2 mol CO2和6 mol H2发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。
CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。
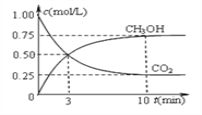
①前10 min内的平均反应速率υ(H2)=____ mol∕(L·min)。
②能说明该反应已达平衡状态的是____。
A.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
B.混合气体的平均摩尔质量保持不变
C.CH3OH的体积分数在混合气体中保持不变
D.混合气体的密度不随时间变化
③下列措施能使n(CH3OH) ∕n(CO2) 增大的是____。
A.升高温度 B.恒温恒容充入He(g)
C.使用高效催化剂 D.恒温恒容下,再充入1mol CO2、3mol H2
④该温度下的平衡常数K=____(L∕mol)2。
(3)用100mL 0.25 mol∕L Na2CO3溶液吸收标准状况下336mL的CO2气体(溶液体积变化忽略不计),所得溶液中:c(HCO3)+c(CO32)+c(H2CO3)=____ mol∕L(填数字)。
(4)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图所示。

① b电极的名称是____。
② 请写出电解时生成乙烯的电极反应式____。
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨反应:N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1 , 在反应过程中,正反应速率的变化如图.下列说法正确的是( ) 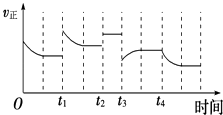
A.t1时升高了温度
B.t2时使用了催化剂
C.t3时增大了压强
D.t4时降低了温度
查看答案和解析>>
科目: 来源: 题型:
【题目】现在人们已能合成自然界并不存在的许多性能优良的有机高分子材料,如由氯乙烯合成聚氯乙烯,则适合于合成聚氯乙烯的原料是( )
A.CH4、Cl2
B.CH3CH3、HCl
C.CH≡CH、HCl
D.CH2=CH2、HCl
查看答案和解析>>
科目: 来源: 题型:
【题目】砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再变化
d. c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某蓄电池放电、充电时的反应为
Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2下列推断中正确的是
Fe(OH)2+2Ni(OH)2下列推断中正确的是
①放电时,Fe为正极,Ni2O3为负极
②充电时,阴极上的电极反应式是Fe(OH)2+2e-==Fe+2OH-
③充电时,Ni(OH)2为阳极
④蓄电池的电极必须是浸在某种碱性电解质溶液中
A. ①②③ B. ①②④ C. ①③④ D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com