
科目: 来源: 题型:
【题目】下列叙述正确的是
A.摩尔是国际单位制中七个基本物理量之一
B.固体氯化钠不能导电,但氯化钠是电解质
C.6.02×1023个12C原子数就是阿伏伽德罗常数
D.1mol一氧化碳的质量为28g/mol
E.Na2CO3和NaHCO3的电离方程式分别是Na2CO3═2Na++CO ![]() 、NaHCO3═Na++H++CO
、NaHCO3═Na++H++CO ![]()
F.金刚石不能导电,所以金刚石是非电解质
G.氧化物只能分为酸性、碱性、两性三类
H.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA .
查看答案和解析>>
科目: 来源: 题型:
【题目】某种食用精制盐包装袋上有如表说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)KIO3+KI+H2SO4═K2SO4+I2+H2O
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是 .
②某学生设计回收四氯化碳的操作为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体d.将分液漏斗充分振荡后静置
其中分液漏斗使用前须进行的操作是 , 上述操作正确的顺序是:(填序号)
(3)已知:I2+2S2O32﹣═2I﹣+S4O62﹣ . 某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10﹣3molL﹣1的Na2S2O3溶液10.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是 .
②b中反应所产生的I2的物质的量是mol.
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)mg/kg.
查看答案和解析>>
科目: 来源: 题型:
【题目】已知Ksp[Fe(OH)3]=2.6×10-39,回答下列问题:
(1)FeCl3溶液可用做净水剂,其净水原理为(用离子方程式表示):______________________。
(2)某酸性MgCl2溶液中含有少量FeCl3,为得到纯净的MgCl2溶液,可加入___________调节溶液的pH=4,使溶液中的Fe3+变为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_________________。
(3)由FeCl3·6H2O晶体得到纯的无水FeCl3的合理方法是:______________________________。
(4)草酸亚铁是制备高纯度活性铁粉的原料,其样品纯度测定步骤如下:准确称取草酸亚铁(FeC2O4)样品wg,将其研成粉末后溶于适量的稀硫酸中(假设杂质不反应)配成250omL溶液。准确量取20mL该溶液于锥形瓶中,用cmol/L的K2Cr2O7酸性溶液(用稀硫酸酸化)滴定至终点,消耗滴定液VmL(还原产物为Cr3+,氧化产物为Fe3+和CO2)。
①滴定时反应的离子方程式为____________________________________。
②该草酸亚铁样品的纯度为___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式为:
①2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=﹣890.3kJmol﹣1
②2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1
③C(s)+O2(g)═CO2(g)△H=﹣393.5Kjmol﹣1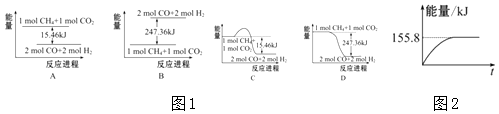
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷气体与O2作用而产生的能量存活,甲烷细菌使1mol甲烷生成CO2气体与液态水,放出的能量(填“>”、“<”或“=”)890.3kJ.
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2═2CO+2H2 , 1g CH4完全反应可释放15.46kJ的热量,则:
①图1(所有物质均为气态)能表示该反应过程中能量变化的是(填字母).
②若将物质的量均为1mol的CH4与CO2充入某恒容密闭容器中,体系放出的热量随时间的变化如图2所示,则CH4的转化率为 .
(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)═CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)═CH4(g)的反应热△H= .
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是(填字母).
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2 , 并放出热量
B.将固态碳合成为C60 , 以C60作为燃料
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
查看答案和解析>>
科目: 来源: 题型:
【题目】向27.2g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2 . 在所得溶液中加入1.0molL﹣1的NaOH溶液1.0L,此时溶液呈中性,金属铜离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
A.Cu与Cu2O的物质的量之比为2:1
B.沉淀为氢氧化铜
C.产生的NO在标准状况下的体积为4.48 L
D.Cu、Cu2O与硝酸恰好完全反应
查看答案和解析>>
科目: 来源: 题型:
【题目】碳及其化合物应用广泛.I.工业上利用CO和水在沸石分子筛表面反应制氢气,CO(g)+H2O(g)CO2(g)+H2(g)
(1)向1L恒容密闭容器中注入CO和H2O(g),830°C时,测得部分数据如下表.
t/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(CO)/mol | 0.200 | 0.160 | 0.125 | 0.099 | 0.080 | 0.080 |
n(H2O)/mol | 0.300 | 0.260 | 0.225 | 0.199 | 0.180 | 0.180 |
则该温度下反应的平衡常数K=
(2)相同条件下,向 1L恒容密闭容器中,同时注入1molCO、1molH2O(g)、2molCO2和2molH2 , 此时v(正)v(逆)(填“>”“=”或“<”);II.已知:CO(g)+ ![]() O2(g)=CO2(g)△H1=﹣141kJmol﹣1
O2(g)=CO2(g)△H1=﹣141kJmol﹣1
2H2(g)+O2(g)=2H2O(g)△H2=﹣484kJmol﹣1
CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(g)△H3=﹣726kJmol﹣1
O2(g)=CO2(g)+2H2O(g)△H3=﹣726kJmol﹣1
(3)利用CO、H2化合制得液态甲醇的热化学方程式为
(4)Ⅲ.一种新型氢氧燃料电池工作原理如图所示.
写出电极A的电极反应式放电过程中,溶液中的CO32﹣将移向电极(填A或B)
(5)以上述电池电解饱和食盐水,若生成0.2mol Cl2 , 则至少需通入O2的体积为L(标准状况)
查看答案和解析>>
科目: 来源: 题型:
【题目】固体氧化物燃料电池是以固体氧化锆﹣氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2﹣)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,下列判断正确的是( ) 
A.有O2参加反应的a极为电池的负极
B.b极的电极反应式为H2+O2﹣﹣2e﹣═H2O
C.a极对应的电极反应式为O2+2H2O+4e﹣═4OH﹣
D.氧化锆的作用是让电子在电池内部通过
查看答案和解析>>
科目: 来源: 题型:
【题目】现用质量分数为98%、密度为1.84gcm﹣3的浓H2SO4来配制500mL0.25mol/L的稀H2SO4 . 可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒⑥容量瓶 ⑦托盘天平 ⑧药匙.请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号).
(2)经计算,需浓H2SO4的体积为 . 现有①10mL ②50mL ③100mL三种规格的量筒,应选用的量筒是(填代号).
(3)将浓H2SO4加适量蒸馏水稀释,冷却片刻,随后全部转移到mL的容量瓶中,转移时应用玻璃棒 . 转移完毕,用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀.然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度1~2cm处.改用加蒸馏水到瓶颈刻度的地方,使溶液的凹液面正好与刻度线相切.振荡、摇匀后,装瓶、贴签.
(4)在配制过程中,其他操作都准确,下列操作中:能引起误差偏高的有(填代号).①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com