
科目: 来源: 题型:
【题目】硫酸亚铁晶体(FeSO47H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下: 
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有(填离子符号),检验滤液中还存在Fe2+的方法为(注明试剂、现象).
(2)步骤②加入过量H2O2的目的是 .
(3)步骤③中反应的离子方程式为 .
(4)步骤④中一系列处理的操作步骤包括:过滤、、灼烧、、称量.
(5)若实验无损耗,则每片补血剂含铁元素的质量为g.
查看答案和解析>>
科目: 来源: 题型:
【题目】利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。该电池工作时,有关说法正确的是( )

A. 该电池工作一段时间后炭棒和炭粒的质量会减轻
B. 炭粒和炭棒上发生的反应为 O2+4e-=2O2-
C. 炭棒应与玩具电机的负极相连
D. 铝罐将逐渐被腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】NA代表阿伏加德罗常数,下列说法正确的是( )
A.1molFe与足量的Cl2反应转移的电子数为2NA
B.标准状况下,22.4L水中含有的水分子数为NA
C.常温、常压下,22gCO2中含有的氧原子数为NA
D.0.11mol/LCaCl2溶液中含氧离子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室有密度为1.8g/m3、质簠分数为98%的“化学纯”硫酸.
(1)取该浓硫酸1L加蒸馏水稀释至18L,稀释后硫酸的物质的量浓度为
(2)现有Na2CO3、NaHCO3组成的混合物,加热到质量不再减少为止,放出标准状况下气体2.24L,取稀释后硫酸200mL恰好与剩余的残渣完全反应,又放出标准状况下气体AL,试计算①原混合物的质量
②原混合物Na2CO3与NaHCO3物质的量之比
③A= .
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是生活中的一种常见金属,用途非常广泛.
(1)FeCl3溶液用于腐蚀印刷线路板,反应的离子方程式为
(2)用废铁皮制取铁红粉的局部流程图如下:
①步骤I温度不能太高的原因是
②步骤Ⅱ中发生反应:
4Fe(NO3)2+O2+(2n+4)H2O═24Fe2O3H2O+8HNO3
4Fe+10HNO3═4Fe(NO3)2+NH4NO3+3H2O
第一个反应的氧化剂是
笫二个反应每生成1molNH4NO3 , 转移的电子数是
③铁红可用于焊接钢轨,其反应的化学方程式为
④上述生产结束后,流程中氮元素最主要的存在形式为(填字母)
a.氮氧化物 b.硝酸按 c.硝酸亚铁 d.硝酸.
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应式为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是
A. 放电时负极的反应为:Zn-2e-+2OH-![]() Zn(OH)2
Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3-3e-+5OH-![]() FeO42-+4H2O
FeO42-+4H2O
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被还原
D. 放电时正极附近溶液的碱性减弱
查看答案和解析>>
科目: 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得: 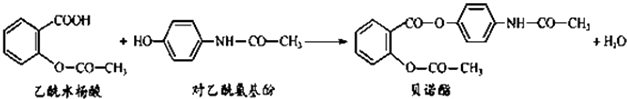
下列有关叙述正确的是( )
A.贝诺酯分子中有三种含氧官能团
B.对乙酰氨基酚核磁共振氢谱中共有四个峰
C.乙酰水杨酸和对乙酰氨基酚均能与Na2CO3 溶液反应
D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目: 来源: 题型:
【题目】四种常见元素的性质或结构信息如下表.试根据信息回答有关问题.
元素 | A | B | C | D |
性质 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx , 有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为(用元素符号表示);
(2)B元素的低价氧化物分子中心原子的杂化方式为 , B元素与D元素形成分子空间构型为;
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点(填“高”或“低”),其原因是;
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为;
(5)C晶体的堆积方式如图所示,设C原子半径为r cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为 , C晶体的密度为gcm﹣3(要求写表达式,可以不化简).
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对于“摩尔”的理解正确的是
A. 摩尔是国际科学界建议采用的一种物理量
B. 摩尔是物质的量的单位,简称摩,符号为mol
C. 1摩尔任何集体都含有6.02×1023个分子
D. 1mol氧含6.02×1023个O2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 1mol H2SO4的质量为98gmol-1 B. SO3的摩尔质量为80gmol-1
C. 1molO就是1mol 氧气 D. SO2 的摩尔质量与其相对分子质量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com