
科目: 来源: 题型:
【题目】含有0.20mol碳酸钠的溶液250mL和100mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
A.2.0mol/L
B.0.24mol/L
C.0.19 mol/L
D.3 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取少量溴乙烷的装置如下图所示.根据题意完成下列填空: 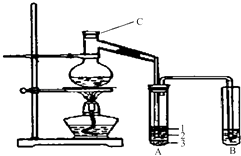
(1)装置图中C仪器的名称为,向C中加入的反应物是溴化钠、和1:1的硫酸.配制体积比1:1的硫酸所用的定量仪器为(选填编号).
a.天平 b.量筒 c.容量瓶 d.滴定管
(2)写出加热时烧瓶中发生的主要反应的化学方程式 .
(3)将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是 .
如图所示试管A中的物质分为三层,产物在第层.
(4)试管A中除了产物和水之外,还可能存在、(写出化学式).
(5)用浓的硫酸进行实验,若试管A中获得的有机物呈橙红色,除去其中杂质的最合理的方法是(选填编号).
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称应该是 .
(6)实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是: .
查看答案和解析>>
科目: 来源: 题型:
【题目】M、A、B、D、N、E五种短周期元素的原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在如图(周期表的一部分)占有相应的位置,它们的原子序数之和为37. 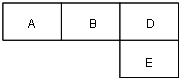
试回答:
(1)写出下列元素的符号: B:;N:
(2)D、E、N形成的简单离子的半径由大到小的关系是 . (写元素符号)
(3)由D、M形成的原子个数1:1的化合物所含的化学键类型是 , 写出该化合物的电子式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶质的物质的量浓度/molL﹣1 | 溶液的密度/gcm﹣3 | |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |

(1)表中硫酸的质量分数为(不写单位,用含c1、ρ1 , 的代数式表示).
(2)物质的量浓度为c1molL﹣1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为molL﹣1 .
(3)将物质的量浓度分别为c2molL﹣1和 ![]() c2molL﹣1的氨水等质量混合,所得溶液的密度(填“大于”、“小于”或“等于”,下同)ρ2gcm﹣3 , 所得溶液的物质的量浓度
c2molL﹣1的氨水等质量混合,所得溶液的密度(填“大于”、“小于”或“等于”,下同)ρ2gcm﹣3 , 所得溶液的物质的量浓度 ![]() c2molL﹣1(设混合后溶液的体积变化忽略不计)
c2molL﹣1(设混合后溶液的体积变化忽略不计)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应方程式书写正确的是( )
A.甲醛和足量银氨溶液充分反应:HCHO+2Ag(NH3)2++2O﹣ ![]() ?HCOO﹣+NH4++2Ag↓+H2O+3NH3
?HCOO﹣+NH4++2Ag↓+H2O+3NH3
B.往苯酚钠溶液中通入少量二氧化碳气体: ![]()
C.向盛有硫酸铜水溶液的试管里加入过量氨水:Cu2++4NH3?H2O═[Cu(NH3)4]2++4H2O
D.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br﹣+Ag+═AgBr↓
查看答案和解析>>
科目: 来源: 题型:
【题目】在标准状况下,m g A气体与n g B气体分子数相等,下列说法不正确的是( )
A.标准状况下,同体积的气体A和气体B的质量比m:n
B.25℃时,1kg气体A与1kg气体B的分子数之比为n:m
C.同温同压下,气体A与气体B的密度之比为m:n
D.标准状况下,等质量的A与B的体积比为m:n
查看答案和解析>>
科目: 来源: 题型:
【题目】在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.依图所示: 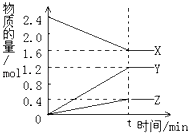
①该反应的化学方程式是 .
②反应起始至t分钟,时v(X)正v(X)逆(填“大于”、“小于”或“等于”),若t=3min,Y的平均反应速率是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2是重要的化工原料,也是应用广发的化工产品.CO2与过氧化钠或超氧化钾反应可产生氧气.
完成下列计算:
(1)CO2通入氨水生成NH4HCO3 , NH4HCO3很容易分解.2.00mol NH4HCO3完全分解,分解产物经干燥后的体积为L(标准状况).
(2)某H2中含有2.40molCO2 , 该混合气体通入2.00L NaOH溶液中,CO2被完全吸收.如果NaOH完全反应,该NaOH溶液的浓度为 .
(3)CO2和KO2有下列反应:
4KO2+2CO2→2K2CO3+3O2
4KO2+4CO2+2H2O→4KHCO3+3O2
若9mol CO2在密封舱内和KO2反应后生成9mol O2 , 则反应前密封舱内H2O的量应该是多少?列式计算.
(4)甲烷和水蒸气反应的产物是合成甲醇的原料:CH4+H2O ![]() CO+3H2 , 已知:CO+2H2
CO+3H2 , 已知:CO+2H2![]() CH3OH CO2+3H2
CH3OH CO2+3H2![]() CH3OH+H2O。300mol CH4完全反应后的产物中,加入100mol CO2后合成甲醇.若获得甲醇350mol,残留氢气120mol,计算CO2的转化率.
CH3OH+H2O。300mol CH4完全反应后的产物中,加入100mol CO2后合成甲醇.若获得甲醇350mol,残留氢气120mol,计算CO2的转化率.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com