
科目: 来源: 题型:
【题目】图为实验室制取和收集纯净干燥的氯气,并进行氯气的性质实验的装置图: 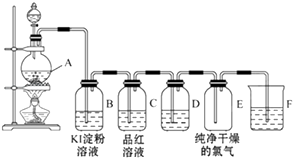
(1)反应前,在装置A中装浓盐酸(填写仪器名称)装MnO2(填写仪器名称)装置A中反应的化学方程式为 .
(2)装置B中的现象是反应的化学方程式为 .
(3)装置D中所装试剂是 , 作用是
(4)装置F中发生反应的化学方程式为
查看答案和解析>>
科目: 来源: 题型:
【题目】将4mol A气体和2mol B气体在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(g)+B(g)2C(g),若经2s后测得C的浓度为0.6molL﹣1 , 现有下列几种说法: ①用物质A表示的反应的平均速率为0.3molL﹣1s﹣1
②用物质B表示的反应的平均速率为0.6molL﹣1s﹣1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7molL﹣1
其中正确的是( )
A.①③
B.①④
C.②③
D.③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是( )
A.苯酚与碳酸氢钠溶液反应:C6H5OH+HCO3﹣→C6H5O﹣+CO2↑+H2O
B.溴乙烷转化成乙醇:C2H5Br+OH﹣ ![]() C2H5OH+Br﹣
C2H5OH+Br﹣
C.肥皂液加入醋酸:C17H35COO﹣+H+→C17H35COOH
D.甲醛溶液与足量的新制Cu(OH)2共热:HCHO+2Cu(OH)2+OH﹣ ![]() HCOO﹣+Cu2O↓+3H2O
HCOO﹣+Cu2O↓+3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】某混合物的水溶液中可能含有以下离子中的若干种:Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl﹣、SO42﹣ , 现分别取100mL的两份溶液进行如下实验.
①第一份加过量NaOH溶液后加热,收集到0.03mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2 , 生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到23.3g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
A.由①可知原溶液存在离子为NH4+ , 其浓度为0.03mol/L
B.原溶液肯定没有Fe3+、Mg2+ , 一定含有Na+
C.n(NH4+):n(Al3+):n(SO42﹣)=3:1:10
D.原溶液一定存在Cl﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( ) 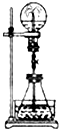
A.Cu与稀盐酸
B.NH4HCO3与稀盐酸
C.CaCO3与稀硫酸
D.NaHCO3与NaOH溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中化学键的类型相同的是( )
A. HCl MgCl2 NH4ClB. H2O Na2O CO2
C. NH3 H2O CO2D. CaCl2 NaOH H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学用语书写正确的是( )
A.氯离子的结构示意图: ![]()
B.作为相对原子质量测定标准的碳核素: ![]() C
C
C.氯化镁的电子式: ![]()
D.用电子式表示氯化氢分子的形成过程: ![]() +
+ ![]() →
→ ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】3,5二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:
甲醇、乙醚和3,5—二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) /g·cm—3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5—二甲氧基苯酚 |
| 33~36 |
| 易溶于甲醇、乙醚,微溶于水 |
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是。
②萃取时使用的主要仪器为。分离出该容器中的有机层的操作是。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是(填字母)。
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。减压过滤完成后应先拆去连接抽气泵和吸滤瓶的橡皮管再关闭抽气泵,其目的是。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol/L
B.V L Fe2(SO4)3溶液中含a g SO42﹣ , 取此溶液 ![]() ?L用水稀释成2V L,则稀释后溶液的c(Fe3+)为
?L用水稀释成2V L,则稀释后溶液的c(Fe3+)为 ![]() ?mol/L
?mol/L
C.已知某NaCl溶液的密度是1.17 g/cm3 , 可求出此溶液的物质的量浓度
D.把100mL20%的NaOH溶液跟100mL10%的NaOH 混合后,可判断NaOH混合溶液的质量分数等于15%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com