
科目: 来源: 题型:
【题目】铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO47H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如图: 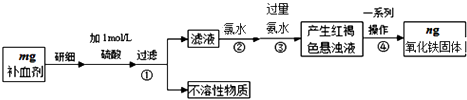
(1)实验中用已经准确量取的浓硫酸配制500mL 1molL﹣1的硫酸溶液,则配制时用到的仪器除烧杯、玻璃棒外,还有两种仪器是 , .
(2)步骤②加入过量氯水的作用是 , 反应的离子方程式为 .
(3)步骤④中一系列操作步骤为、洗涤、灼烧、冷却、称量.
(4)若实验无损耗,则该补血剂含铁元素的质量分数为 .
(5)下列操作会导致所测定的铁元素含量偏高的是 A.步骤③所加氨水量不足
B.步骤④洗涤不充分
C.步骤④灼烧不充分.
(6)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1molL﹣1的硫酸溶液,过滤.取滤液加溶液,若溶液变成色,说明该补血剂已变质.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关肥皂的叙述中错误的是:
A.肥皂与纯碱的去污原理相同B.肥皂可以加速油污在水中的分散C.肥皂是油脂在碱性条件下水解生成的D.肥皂主要成分的分子中含有亲油基团和亲水基团
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在通常条件下一步转化关系的组合只有( )
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③
B.①③④
C.②③
D.①④
查看答案和解析>>
科目: 来源: 题型:
【题目】应对雾霾污染、改善空气质量需要从多方面入手.
(1)研究发现,NOx是雾霾的主要成分之一,NOx主要来源于汽车尾气.
已知:N2(g)+O2(g)2NO(g)△H=+180.50kJmol﹣1
2CO(g)+O2(g)2CO2(g)△H=﹣566.00kJmol﹣1
为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环,写出该反应的热化学方程式 .
(2)开发利用清洁能源可减少污染,解决雾霾问题.甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景,一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2 , 在催化剂作用下充分反应.平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图1所示. 
(i)该反应的反应热△H0(填“>”或“<”),压强的相对大小与P1P2(填“>”或“<”).
(ii)该反应化学平衡常数表达式为 .
(iii)下列各项中,不能说明该反应已经达到平衡的是 .
A.容器内气体压强不再变化
B.v(CO):v(H2):v(CH3OH)=1:2:1
C.容器内的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
(iv)某温度下,在保证H2浓度不变的情况下,增大容器的体积,平衡(填字母).
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
作出此判断的依据是 .
(3)依据燃烧反应原理,合成的甲醇可以设计如图2所示的燃料电池装置.
(i)负极电极反应式为 .
(ii)电池工作时,若电流强度为I,1个电子所带电量为q,NA为阿伏伽德罗常数的值,则该装置每分钟消耗甲醇的物质的量为mol(假设化学能全部转化为电能).
查看答案和解析>>
科目: 来源: 题型:
【题目】石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),可由石墨剥离而成,具有极好的应用前景。下列说法正确的是
A.石墨烯与石墨互为同位素
B.0.12g石墨烯中含有6.02*1022个碳原子
C石墨烯是一种有机物
D.石墨烯中的碳原子间以共价键结合
查看答案和解析>>
科目: 来源: 题型:
【题目】亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,可溶于水,不溶于乙醇.在化学实验、电镀、食品添加剂、烧制青花瓷时可用于绘画等方面有广泛用途.已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下: 
(1)常温下,NaCN水溶液的pH7(填“>”、“<”、“=”),实验室用NaCN固体配制NaCN溶液时,应先将其溶于溶液,再用蒸馏水稀释.
(2)反应器中发生的主要反应的化学方程式为 .
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、 .
(4)转化器中生成K4[Fe(CN)6]的反应类型是 , 相同温度下,溶解度:K4[Fe(CN)6]Na4[Fe(CN)6](填“>”“=”“<”),过滤后洗涤K4[Fe(CN)6]使用的试剂是 .
(5)实验室常用K4[Fe(CN)6]检验Fe3+ , 生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为 .
(6)含有14.7kgNaCN的工业废水可生产出9.2kg的K4[Fe(CN)6],则K4[Fe(CN)6]的产率是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
J | ||||
R |
(1)M的离子结构示意图为;元素T基态原子的价电子排布式为 .
(2)J和氢组成的化合物分子有6个原子,其结构简式为
(3)M和R形成的化合物遇水会发生剧烈的反应,反应的化学方程式为 .
(4)L的最简单气态氢化物甲的水溶液显碱性. ①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,反应后的产物不污染环境,其化学方程式为 .
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是(选填序号).
选项 | a | b | c | d |
x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物总物质的量 |
③据报道,“L5+”是带正电荷的分子碎片,它的结构尚不清楚.其结构应该是对称的,5个L排成V形,且都达到8电子结构.则L5+可能的结构式是 , 其中可能含有个σ键,个π键,对孤电子对.
(5)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ. 该反应的热化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com