
科目: 来源: 题型:
【题目】如图为实验室某盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl﹣的数目
D.溶液的密度
(2)容量瓶上需标有以下五项中的
A.温度
B.浓度
C.规格
D.压强
E.刻度线
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400molL﹣1的稀盐酸.
将下列操作填写完整;
A.用量筒准确量取浓盐酸①mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀.
B.将已冷却的盐酸沿玻璃棒注入 ②中.
C.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡.
D.继续往容量瓶内小心加水,直到液面接近刻度线下1﹣2cm处.
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切.
F.将容量瓶盖紧,颠倒摇匀.
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏大”、“偏小”、“无影响”).
①用量筒量取浓盐酸时俯视观察凹液面
②溶液注入容量瓶前没有冷却至室温 .
查看答案和解析>>
科目: 来源: 题型:
【题目】把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.![]()
B.(2b﹣a)mol/L
C.![]()
D.(10b﹣5a)mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( ) 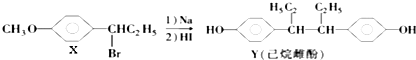
A.在NaOH水溶液中加热,化合物X可发生消去反应
B.在一定条件下,化合物Y可与Br2发生加成反应
C.用FeCl3溶液可鉴别化合物X和Y
D.化合物Y中不含有手性碳原子
查看答案和解析>>
科目: 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O.将12.4g该有机物的完全燃烧产物通过浓H2SO4 , 浓硫酸增重 10.8g,再通过碱石灰,碱石灰又增重了17.6g.下列说法正确的是( )
A.该有机物的最简式为 CH3O
B.该有机物的分子式可能为 CH3O
C.该有机物的分子式可能为 C2H6O
D.该有机物1H核磁共振谱中有两个峰
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A. 离子化合物一定不含共价键
B. 共价化合物中一定不含有离子键
C. 气态单质的分子中一定存在共价键
D. 非金属元素的化合物中一定不含离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇是一种优质的液体燃料,二甲醚与合成气制乙醇是目前合成乙醇的一种新途径,总反应为:CH3OCH3(g)+CO(g)+2H2 (g)CH3OH(g)+C2H5OH(g).向反应系统中同时通入二甲醚、一氧化碳和氢气,先生成中间产物乙酸甲酯后,继而生成乙醇.发生的主要化学反应有:
反应过程 | 化学方程式 | 不同温度下的K | ||
273.15K | 1000K | |||
Ⅰ | 二甲醚羰基化反应 | CH3OCH3(g)+CO(g)CH3COOCH3(g) | 1016.25 | 101.58 |
Ⅱ | 乙酸甲酯加氢反应 | CH3COOCH3(g)+2H2(g)CH3OH(g)+C2H5OH(g) | 103.97 | 10﹣0.35 |
回答下列问题:
(1)二甲醚碳基化反应的△H0 (填“>”“<”“=”).
(2)若反应在恒温恒容下进行,下列可说明反应已经达到平衡状态的是 .
A.2v(CH3COOCH3)=v(H2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度保持不变
D.密闭容器中C2H5OH的体积分数保持不变
(3)总反应CH3OCH3(g)+CO(g)+2H2 (g)CH3OH(g)+C2H5OH(g)的平衡常数表达式K= , 随温度的升高,总反应的K将(填“增大”、“不变”或“减小”).
(4)在压强为1Mpa条件下,温度对二甲醚和乙酸甲酯平衡转化率影响如图1所示,温度对平衡体系中乙酸甲酯的含量和乙醇含量的影响如图2所示.观察图2可知乙酸甲酯含量在 300K~600K范围内发生变化是 , 简要解释产生这种变化的原因 .
(5)将CH3OCH3(g)和CO(g)按物质的量之比1:1充入密闭容器中发生碳基化反应,在T K时,反应进行到不同时间测得各物质的浓度如下:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
CH3OCH3(g) | 2.00 | 1.80 | 1.70 | 1.00 | 0.50 | 0.50 |
CO(g) | 2.00 | 1.80 | 1.70 | 1.00 | 0.50 | 0.50 |
CH3COOCH3(g) | 0 | 0.20 | 0.30 | 1.00 | 1.50 | 1.50 |
①20min时,只改变了某一条件,根据上表中的数据判断改变的条件可能是(填字母).
A.通入一定量的CO B.移出一定量的CH3OCH3C.加入合适的催化剂
②在图3中画出TK,CH3COOCH3(g)的体积分数随反应时间的变化曲线 . 
查看答案和解析>>
科目: 来源: 题型:
【题目】肼(N2H4)是一种重要的液态火箭燃料,具有弱碱性和强还原性.工业上利用尿素[CO(NH2)2]、NaC1O在NaOH溶液中发生反应生成水合肼(N2H4H2O)、Na2CO3等产物.请回答:
(1)上述生成水合肼的反应中尿素是( 填“氧化剂”或“还原剂”),反应的化学方程式为 .
(2)肼与盐酸反应可生成N2H6C12 , N2H6C12的水溶液显性( 填“酸”或“碱”或“中”),用离子方程式表示其原因 .
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式 .
若要设计实验方案检验上述反应生成固体产物中的金属离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中;
②
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关叙述不正确的是
A.C、N、O、F原子半径逐渐减小B.Na、K、Rb、Cs失电子能力逐渐增强
C.P、S、Cl、Br的最高正价依次升高D.Na、Mg、Al、Si的最外层电子数依次增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com