
科目: 来源: 题型:
【题目】某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂.
用盐酸滴定待测液NaOH,滴定终点时的颜色变化是;若滴定前平视读数,滴定终点时俯视读数,则会使所测NaOH溶液的浓度值(填“无影响”、“偏高”或“偏低”).
查看答案和解析>>
科目: 来源: 题型:
【题目】空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
(1)一定温度下,向固定体积为2L的密闭容器中充入SO2和NO2各1mol,发生反应SO2(g)+NO2(g)SO3(g)+NO(g),测得上述反应5min末到达平衡,此时容器中NO与NO2的体积比为3:1,则这段时间内SO2的反应速率υ(SO2)= , 此反应在该温度下的平衡常数K= .
(2)甲醇日趋成为重要的有机燃料,通常利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示: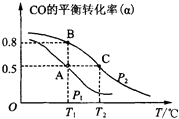
①上述合成甲醇的反应为反应(填“放热”或“吸热”).
②A、B、C三点的平衡常数KA、KB、KC的大小关系为 . A、B两点对应的压强大小关系是PAPB(填“大于”、“小于”或“等于”).
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为 , 理论上通过外电路的电子最多为 mol.
查看答案和解析>>
科目: 来源: 题型:
【题目】在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
A. p(Ne)>p(H2)>p(O2) B. p(O2)>p(Ne)>p(H2)
C. p(H2)>p(O2)>p(Ne) D. p(H2)>p(Ne)>p(O2)
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的是
①化合物 ②能与硝酸反应 ③钠盐 ④氧化物
A. ②④ B. ①②④ C. ①③ D. ①
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D是原子序数均小于20的四种元素.A与B同主族,且能形成BA2、BA3两种化合物.B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小.请回答下列问题:
①D元素在元素周期表中的位置是 .
②A与D所形成的化合物的电子式为 .
③将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:
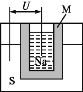
【题目】如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS![]() Na2Sx,正极的电极反应式为 。M(由Na2O和Al2O3制得)的两个作用是 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的 倍。
Na2Sx,正极的电极反应式为 。M(由Na2O和Al2O3制得)的两个作用是 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的 倍。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁及其化合物在国民经济的发展中起着重要作用.
(1)铁在潮湿的空气中易发生电化学腐蚀.某同学将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图1所示.液滴边缘是﹣﹣区(填“正极”或“负极”),其电极反应式为 . 
(2)铁钛合金是一种常用的不锈钢材料,某同学在探究该合金的性质时,往含有TiO2+、Fe3+溶液中加入铁屑至溶液显紫色,该过程中发生的反应有;
①2TiO2+(无色)+Fe+4H+═2Ti3+(紫色)+Fe2++2H2O
②Ti3+(紫色)+Fe3++H2O═TiO2+(无色)+Fe2++2H+
③ .
(3)高铁酸钠(Na2FeO4)是一种优良的水处理剂.
①FeO42﹣在水溶液中的存在形态如图2所示,纵坐标表示各存在形态的分数分布.下列说法不正确的是(填字母序号).
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4﹣的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO4﹣+OH﹣═FeO42﹣+H2O
②从环境保护的角度看,制备高铁酸盐的较好方法为电解法.用铁片作阳极,NaOH溶液为电解质溶液,电解制备高铁酸钠,其电流效率可达到40%.写出阳极的电极反应式
. 铁丝网电极是更理想的阳极材料,相同条件下,可将电流效率提高至70%以上,原因是 .
若维持电流强度为5.0A,电解20min,理论上可生成Na2FeO4g.(己知:F=96500C/mol,答案保留两位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”.引发雾霾天气的污染物中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气.
(1)已知反应N2O4(g)2NO2(g)△H,随温度升高,混合气体的颜色变深.将一定量N2O4气体充入绝热容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间变化情况.
下列说法能说明透光率不再发生改变的有 .
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变
(2)用NH3催化还原NOx可以消除氮氧化物的污染.如图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),反应原理为:NO(g)+NO2(g)+2NH3(g)2N2(g)+3H2O(g).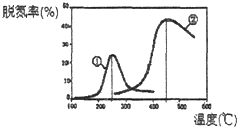
①该反应的△S0(填“>”、“=”或“<”).
②以下说法正确的是 .
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
(3)用CH4催化还原NOx也可以消除氮氧化物的污染.
已知:CH4(g)的燃烧热为890kJ/mol,蒸发1mol H2O(l)需要吸收44kJ热量.
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=﹣1114kJ/mol
2NO(g)+O2(g)═2NO2(g)△H=﹣114kJ/mol
写出CH4催化还原NO2(g)生成N2和H2O(g)的热化学方程式: .
(4)在温度为T1℃和T2℃时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 |
T1 | 1.2 | 0.9 | 0.7 | 0.4 | 0.4 |
T2 | 1.2 | 0.8 | 0.56 | … | 0.5 |
①温度为T1℃时,0~20min内,v(CH4)= .
②T1T2(填“>”或“<”,下空同);判断理由是 .
③T1℃时,反应CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g)平衡常数K=
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2 , 达新平衡时CH4的转化率将 (填“增大”、“减小”或“不变”).
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25%氨水的密度为0.91g.cm-3,5%氨水的密度为0.98g.cm-3,若将上述两溶液等体积混合,所得氨水溶液的质量分数是
A. 等于15% B. 大于15% C. 小于15% D. 无法估算
查看答案和解析>>
科目: 来源: 题型:
【题目】关于以下科技成果,下列说法正确的是( )
A.中国“人造太阳” | B.电磁炮成功装船 | C.“鲲龙”两栖飞机 | D.“墨子”通信卫星 |
利用氘和氚发生化学反应产生上亿度高温 | 电磁炮发射过程中电能转化为机械能 | 飞机大量使用熔点高、硬度大的铝锂合金 | 通讯中使用的光导纤维主要成分是单晶硅 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com