
科目: 来源: 题型:
【题目】已知有机物A、B、C、D、E有如图所示转化关系: 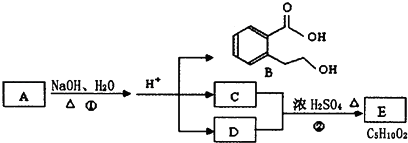
其中C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物.根据上图回答问题:
(1)B分子中的含氧官能团名称是;
写出一个同时符合下列四个条件的B的同分异构体的结构简式 .
a.含苯环结构,取代基位于间位 b.能发生水解反应
c.能发生银镜反应 d.与FeCl3溶液发生显色反应.
(2)写出②的反应方程式: .
(3)写出D与浓硫酸在加热条件下发生的反应 .
(4)A的结构筒式是 .
(5)若B分子(发生分子间脱水)发生酯化反应生成高分子的结构简式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:1 mol晶体硅中含有2 mol Si—Si键。工业上可通过下列反应制取高纯硅:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),根据下表列举的化学键的键能数据,判断该反应的反应热(ΔH)为( )
Si(s)+4HCl(g),根据下表列举的化学键的键能数据,判断该反应的反应热(ΔH)为( )
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
A.+412 kJ·mol-1 B.-412 kJ·mol-1
C.+236 kJ·mol-1 D.-236 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】三氧化铀是一种两性氧化物,它在溶液中可以以UO22+和U2O72-形式存在,按要求写出UO3与强酸、强碱反应的离子方程式:
(1)______________________________;(2)_________________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+![]() O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
③CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH3=-870.3 kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为( )
A.ΔH=+244.1 kJ/mol B.ΔH=-488.3 kJ/mol
C.ΔH=-996.6 kJ/mol D.ΔH=+996.6 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】硫及其化合物对人类的生产和生活有着重要的作用.
2SO2(g)+O2(g)2SO3(g)△H=﹣198kJmol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2 , 反应在不同条件下进行,反应体系总压强随时间的变化如下图所示.与实验a相比,实验b改变的条件是 , 判断的依据 . 
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)SO3(g)+NO(g)△H=﹣42kJmol﹣1 .
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
N(SO2) | N(NO2) | N(NO) | ||
甲 | T1 | 0.80 | 0.20 | 0.18 |
乙 | T2 | 0.20 | 0.80 | 0.16 |
丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= , 该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,TlT2(填“>”“<’’或“=”),判断的理由是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是对化学反应变化过程及结果的研究.按要求回答问题:
(1)已知:甲醇脱水反应2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=﹣23.9kJmol﹣1
甲醇制烯烃反应2CH3OH(g)=C2H4 (g)+2H2O(g)D△H2=﹣29.1kJmol﹣1
乙醇异构化反应C2H5OH(g)=CH3OCH3(g))D△H3=+50.7kJmol﹣1
则乙烯气相直接水合反应:C2H4 (g)+H2O(g)=C2H5OH(g)的△H= .
(2)在25℃下,将pH=a的氢氧化钠溶液与pH=b的醋酸溶液等体积混合,若两溶液恰好完全反应,则a+b14(填>、“<”或“=”);该温度下醋酸的电离常数K=(用含a、b的式子精确表示)
(3)用一个离子方程式表示反应:100ml 3molL﹣1NaOH溶液中通入标准状况下4.48LCO2;所得溶液中离子浓度大小排列顺序为:;
(4)废氨水可以转化成氨,氨再设计成碱性燃料电池.图是该燃料电池示意图,产生的X气体可直接排放到大气中.a电极电极反应式为;T℃下,某研究员测定NH3H2O的电离常数为1.8×10﹣5 , NH4+的水解平衡常数为1.5×10﹣8(水解平衡也是一种化学平衡,其平衡常数即水解常数),则该温度下水的离子积常数为 , 请判断T25℃(填“>”“<”“=”) 
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米氧化铝在陶瓷、电子、生物医药等方面有广泛的用途,它可通过硫酸铝铵晶体热分解得到[已知:硫酸铝铵晶体的化学式为Al2(NH4)2(SO4)424H2O,相对分子质量为906].制备硫酸铝铵晶体的实验流程如下: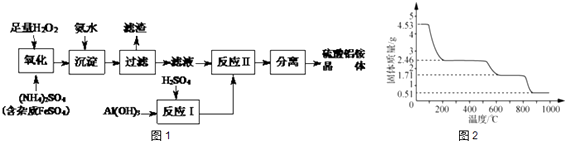
(1)H2O2氧化FeSO4的离子方程式为 .
(2)加入氨水的目的是 , 其化学反应方程式为 .
(3)若要保证产品的纯度,必须检验加入氨水后杂质是否除尽.其实验操作是:用试管取少量滤液, , 则说明杂质已除净.
(4)上述流程中,“分离”所包含的操作依次为:、、过滤、洗涤、干燥;请完成硫酸铝铵晶体高温分解的化学方程式:2Al2(NH4)2(SO4)424H2O═ Al2O3+NH3↑+SO3↑+ .
(5)取4.53g 硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图2所示.请计算确定400℃时(硫酸铵未分解)剩余固体成分的化学式为(H:1 N:14O:16 Al:27 S:32)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.食盐与石英熔化时,克服微粒间的作用力相同
B.SiHFBr2分子中所有原子的最外层均为8个稳定结构
C.重水在3.8℃时就变成了“热冰”,可能与重水分子间存在氢键有关
D.NaHSO4加热融化时破坏了该物质中的离子键和共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
请回答下列问题:
(1)若A为第三周期的金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,F的浓溶液与A、D反应都有红棕气体生成,则A的原子结构示意图为;反应④的化学方程式为: .
(2)若A为用量最大的金属,D、F是气态单质,反应②的离子方程式是: , A与水蒸气反应的化学方程式为: .
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,B常用作光导纤维,A、F所含元素同周期,则E的电子式为 , 反应①的化学方程式为 . 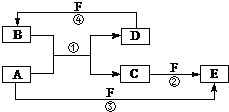
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计如图1所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
实验 | 药品 | 制取气体 | 量气管中的液体 |
Ⅰ | Cu、稀HNO3 | H2O | |
Ⅱ | NaOH固体、浓氨水 | NH3 | |
Ⅲ | Na2SO3固体、浓H2SO4 | SO2 | |
Ⅳ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
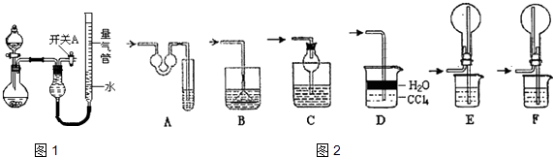
(1)实验过程中,使用分液漏斗滴加液体的操作是 .
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?(填“可行”或“不可行”).原因为
(3)实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中发生反应的离子方程式是 .
(4)实验Ⅱ中量气管中的液体最好是(填字母编号,下同).
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.如图2,以下各种尾气吸收装置中,适合于吸收NH3 , 而且能防止倒吸的有 .
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,② , ③视线与凹液面最低处相平.
(6)实验Ⅳ获得以下数据(所有气体体积已换算成标准状况,忽略滴入液体体积对气体体积的影响)
编号 | 镁铝合金度量 | 量气管第一次读数 | 量气管第二次读数 |
① | 1.0g | 10.0mL | 346.3mL |
② | 1.0g | 10.0mL | 335.0mL |
③ | 1.0g | 10.0mL | 345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为 . (H:1 Mg:24 Al:27)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com