
科目: 来源: 题型:
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA﹣ , Ⅲ代表A2﹣)所示.根据图示判断,下列说法正确的是( ) 
A.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA﹣)>c(A2﹣)>c(H+)>c(OH﹣)
B.等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水小
C.NaHA溶液中:c(OH﹣)+c(A2﹣)=c(H+)+c(H2A)
D.向上述加入20mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有机物在酸性催化条件下发生水解反应,生成两种不同的有机物,且这两种有机物的相对分子质量相等,该有机物是①蔗糖 ②麦芽糖 ③丙酸丙酯 ④甲酸乙酯( )
A.①②④
B.①
C.③
D.①④
查看答案和解析>>
科目: 来源: 题型:
【题目】制备氮化镁的装置示意图如下: 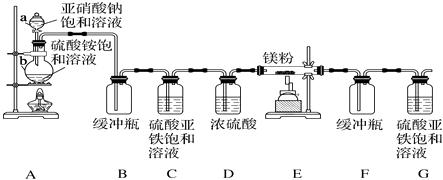
回答下列问题:
(1)仪器a的名称是 , b的名称是 .
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式: .
(3)C的作用是 .
(4)写出E中发生反应的化学方程式: .
(5)请用化学方法确定氮化镁是否含有未反应的镁,写出实验操作及现象 .
查看答案和解析>>
科目: 来源: 题型:
【题目】往1.0molL﹣1KI溶液中加入固体I2 , 发生反应:I2(aq)+I﹣ (aq)═I3﹣(aq)△H;I﹣的物质的量浓度c(I﹣)随温度T的变化曲线如图所示.已知反应第一次达到平衡时用时10s,则下列说法正确的是( ) 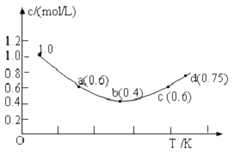
A.该反应的△H>0
B.a、c两点对应的I﹣反应速率相等
C.b点时0~10s I﹣的平均反应速率为0.04molL﹣1s﹣1
D.d点时该反应在对应温度下处于平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】高锰酸钾[KMnO4]是常用的氧化剂.工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体.中间产物为锰酸钾[K2MnO4].图1是实验室模拟制备的操作流程: 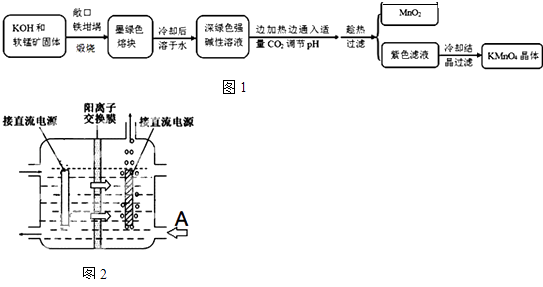
相关资料:
①物质溶解度
物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42﹣)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42﹣会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是;
(2)实验时,若CO2过量会生成KHCO3 , 导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:;
其中氧化还原反应中氧化剂和还原剂的质量比为 .
(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中 , 得到的产品纯度更高.
A.醋酸
B.浓盐酸
C.稀硫酸
(4)工业上采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图).图2中A口加入的溶液最好为 . 使用阳离子交换膜可以提高Mn元素利用率的原因为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】Zn还原SiCl4的反应如下:下列说法正确的是( )
SiCl4(g)+2Zn(l)Si(s)+2ZnCl2(g)△H1
SiCl4(g)+2Zn(g)Si(s)+2ZnCl2(g)△H2 .
A.Zn(l)=Zn(g)△H= ![]() (△H1﹣△H2 )
(△H1﹣△H2 )
B.用硅制作的太阳能电池是将化学能转化为电能
C.增加Zn(g)的量,△H2变大
D.以Zn片、铜片和稀硫酸构成的原电池,Zn片表面有气泡产生.
查看答案和解析>>
科目: 来源: 题型:
【题目】物质A﹣G有下图所示转化关系(部分反应物、生成物没有列出).其中A为某金属矿的主要成分,经过一系列反应可得到B和C.单质C可与E的浓溶液发生反应,G为砖红色沉淀. 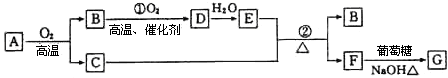
请回答下列问题:
(1)写出下列物质的化学式:B、G;
(2)C与硫磺在加热条件下的生成物与足量浓硝酸反应的离子方程式为: .
(3)反应②的化学方程式是;
(4)将0.23molB和0.11mol氧气放入容积为1L的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12molD,则反应的平衡常数K= . 若温度不变,再加入0.50mol氧气后重新达到平衡,D的体积分数(填“增大”、“不变”或“减小”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com