
科目: 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加过量NaOH溶液加热后,只收集到气体0.02mol,无沉淀生成,同时得到溶液甲。
②在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02g。
③第二份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65g。
根据上述实验回答:
(1)一定不存在的离子是______________,不能确定是否存在的离子是_______________。
(2)试确定溶液中肯定存在的离子及其浓度(可不填满):
离子符号______,浓度______;离子符号______,浓度______;离子符号______,浓度______.
(3)试确定K+是否存在______(填“是”或“否”),判断的理由是__________________________。
(4)设计简单实验验证原溶液中可能存在的离子____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁铝合金、铁合金、硅酸盐都是广泛应用的建筑材料。
(1)镁的原子结构示意图为_______________。镁是一种活泼的金属、但其在空气中不易腐蚀,原因是_____________________________,镁、铝、铁三种常见金属的活动性由强到弱的顺序是_________。
(2)钢是用途最广、用量最多的铁合金,某种钢由铁和另一种元素组成,将少量该钢样品与足量热的浓硫酸充分反应生成两种气体,写出生成两种气体的化学反应方程式:__________________________。
(3)滑石粉的主要成分是Mg3[Si4O10](OH)2用氧化物表示其组成:_______________________。二氧化硅能与一种酸反应,可根据此反应原理制雕花玻璃,写出反应的化学方程式: _________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙酸异戊酯( ![]() )是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图(有关的加热和夹持仪器略去)和有关数据如下:
)是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图(有关的加热和夹持仪器略去)和有关数据如下:
实验步骤:在烧瓶中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热烧瓶,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁晶体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯2.6g.回答下列问题:
相对分子质量 | 密度/(gcm﹣3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
(1)写出制取乙酸异戊酯的化学方程式 .
(2)冷凝管的作用是,碎瓷片的作用是 .
(3)若乙酸异戊酯产率偏低,其原因可能是(填序号).
A.原料没有充分反应
B.发生了副反应
C.在进行蒸馏纯化操作时,从143℃开始收集馏分
(4)在洗涤、分液操作中,应充分振荡,然后静置,待分层后(填序号).
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(5)实验中加入少量无水硫酸镁的目的是 .
(6)本实验的产率是(填序号)
A.30%
B.40%
C.50%
D.60%
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.【实验目的】制取乙酸乙酯
(1)【实验原理】甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,该反应的化学方程式为 .
(2)【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置: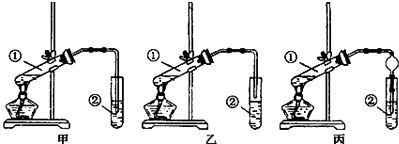
若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是(填“甲”或“乙”).丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是 .
(3)【实验步骤】A按所选择的装置组装仪器,在试管①中先加入3mL95%的乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸;
B将试管固定在铁架台上;
C在试管②中加入5mL X试剂;
D用酒精灯对试管①加热
E.当观察到试管②中有明显现象时停止实验.
【问题讨论】
①实验中浓硫酸的作用是 .
②试管2中加入的X试剂为 .
③步骤E试管②中观察到的现象是 .
④常用方法分离获得实验中的乙酸乙酯.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
B | 向无色溶液中加硝酸酸化的BaCl2溶液 | 有白色沉淀 | 原溶液中一定含SO |
C | 向Na2SiO3溶液中通入适量CO2气体 | 出现白色沉淀 | H2CO3的酸性比H2SiO3强 |
D | 向某溶液中先加氯水再加KSCN溶液 | 溶液呈血红色 | 原溶液中一定含Fe2+ |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物F是一种重要的有机合成中间体,它的合成路线如图: 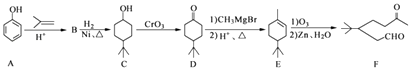
(1)化合物F中含氧官能团的名称是和 .
(2)通过实验可证明A物质具有极弱的酸性,写出有关的化学方程式 .
(3)化合物B的结构简式为 , A到B的反应类型为 .
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢.写出该化合物的结构简式(任写一种).
(5)请根据已有知识并结合相关信息,写出以苯酚( ![]() )和CH2=CH2为原料制备有机物 的
)和CH2=CH2为原料制备有机物 的 ![]() 合成路线流程图(无机试剂任用).
合成路线流程图(无机试剂任用).
合成路线流程图示例如下:CH3CH2OH ![]() CH2=CH2
CH2=CH2 ![]() Br﹣CH2CH2﹣Br.
Br﹣CH2CH2﹣Br.
查看答案和解析>>
科目: 来源: 题型:
【题目】物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有大。下列各组物质反应产物与物质的浓度有关的是
①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液
A. ①③ B. ③④ C. ①② D. ①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】绿矾是一种重要的化工原料.
(1)【问题1】绿矾晶体(FeSO47H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质.为探究绿矾样品的变质情况,某化学兴趣小组的同学设计了下列实验方案.实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液.
①方案1:取少量溶液,加入几滴试剂(写化学式),如果观察到的现象是溶液变血红色;实验结论:证明绿矾样品已被氧化.
②方案2:取少量溶液,加入几滴酸性KMnO4溶液,如果观察到的现象是 . 实验结论:证明绿矾样品完全被氧化.
③使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 .
④要从FeSO4溶液中得到绿矾晶体,必须进行的实验操作步骤:、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有(此空填序号)
A.蒸发皿 B.石棉网 C.烧杯 D.玻璃棒
(2)【问题2】灼烧绿矾的反应方程式:2(FeSO47H2O)═Fe2O3+SO2↑+SO3↑+14H2O工业上常通过高温分解FeSO4的方法制备Fe2O3 , 为检验FeSO4高温分解的气体产物中是否含有SO2和SO3 , 进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中.请回答以下问题: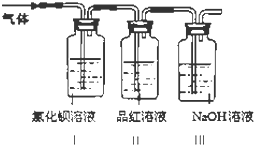
①装置I中氯化钡溶液中可观察到现象 . 若氯化钡溶液足量,将最后所得沉淀过滤、洗涤、烘干后称重为2.33克,则灼烧绿矾的过程中转移了mol的电子.
②装置II中试剂为品红溶液,其作用是
③装置III中试剂为NaOH溶液,其作用是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】中国古代文物不仅彰显了民族和文化自信,还蕴含许多化学知识。下列说法不正确的是
A.商代“四羊方尊”是青铜制品,青铜属于铜的合金
B.宋代《莲塘乳鸭图》所用宣纸,其主要成分是纤维素
C.清代“瓷母”是指各种釉彩大瓶,主要成分是二氧化硅
D.东晋《洛神赋图》中的颜料铜绿,主要成分属于盐类
查看答案和解析>>
科目: 来源: 题型:
【题目】
A. 点燃氢气前一定要检验氢气的纯度
B. 未使用完的白磷要随时收集起来,并与空气隔绝
C. 用氢气还原氧化铜时,要先通一会儿氢气,再加热氧化铜
D. 酒精灯不用时,必须盖上灯帽
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com