
科目: 来源: 题型:
【题目】将露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解)。试计算:

(1)盐酸的物质的量浓度为__________mol/L。
(2)该样品中NaOH与Na2CO3的物质的量之比(写出计算过程,只有答案不给分)。__________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)实验室制取、净化并收集氯气涉及以下几个主要阶段:

现有以下2种试剂: A.饱和食盐水 B.NaOH溶液
请在以上试剂中选择填空(填“A”或“B”):
①写出上述制取氯气的离子方程式_____________________,X溶液应选用______。
②尾气处理过程中,多余的氯气可用______吸收,写出该过程的离子方程式_____。

(2)FeSO47H2O受热分解的化学方程式为:2FeSO47H2O ![]() Fe2O3+SO2↑+SO3↑+14 H2O
Fe2O3+SO2↑+SO3↑+14 H2O
请回答:
① FeSO47H2O俗名叫________矾,将其受热产生的气体按图示装置进行实验,证实含有SO3和SO2。 能说明SO2存在的实验现象是________;为测定BaSO4沉淀的质量,后续的操作步骤依次为________、洗涤、干燥、称重。
②设计一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应)_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭体积不变的真空容器中加入一定量纯净的氨基甲酸铵固体,(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g),已知25℃时,平衡气体总浓度为2.4×10﹣3molL﹣1 , 下列说法中正确的是( )
A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态
B.20℃时,氨基甲酸铵的分解平衡常数为2.048×10﹣9mol3L﹣3
C.恒温下压缩体积,NH3的体积分数不变
D.再加入一定量氨基甲酸铵,可加快正反应反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】现有X(g)+Y(g)2Z(g);正反应放热.从反应开始经过t1后达到平衡状态,t2 时由于条件改变,平衡受到破坏,在t3时又达到平衡,据如图回答:从t2→t3的曲线变化是由哪种条件引起的( ) 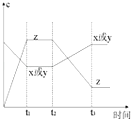
A.增大X或Y的浓度
B.增大压强
C.增大Z的浓度
D.升高温度
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应mA(固)+nB(气)cC(气)+fD(气)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(P)的关系如下图所示,下列叙述正确的是( ) 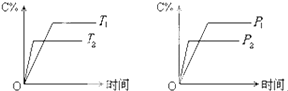
A.达到平衡后,若使用催化剂,C的体积分数增大
B.达到平衡后,若使温度升高,化学平衡向逆反应方向移动
C.化学方程式中n>c+f
D.达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,在某密闭容器内某一反应中M,N的物质的量随反应时间变化的曲线如图所示.下列叙述中,正确的是( ) 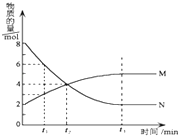
A.该反应的化学方程式为M═2N
B.若t1=1,则反应开始至t1时间段M 的反应速率为1mol﹒L﹣1﹒min﹣1
C.t2时正逆反应速率相等,反应达到平衡状态
D.t3时正反应速率等于逆反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.“液氯”因其具有强氧化性不能用钢瓶运输
B.氧化镁具有较高的熔点,常被用于耐高温材料
C.在医疗上,纯碱可用于治疗胃酸过多,但不能用于胃穿孔病人
D.硅是一种重要的半导体材料,常被用于制造光导纤维
查看答案和解析>>
科目: 来源: 题型:
【题目】氯气是一种重要的工业原料,工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气,下列说法错误的是( )
A. 氧化产物为N2
B. 该反应NH3被还原
C. 该反应HCl是还原产物
D. 生成1 mol N2有6 mol电子转移
查看答案和解析>>
科目: 来源: 题型:
【题目】将4molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)2C(g),
若经 2s后测得 C的浓度为 0.6molL﹣1 , 现有下列几种说法:
①用物质A 表示反应的平均速率为 0.3molL﹣1s﹣1
②物质 B的体积分数是40%
③2s 时物质 A 的转化率为30%
④2s 时物质 B 的浓度为 1.0molL﹣1
其中正确的是( )
A.①④
B.②③
C.①③
D.③④
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个密闭容器中,盛有N2和H2 , 它们的起始浓度分别是1.8molL﹣1和5.4molL﹣1 , 在一定的条件下它们反应生成NH3 , 10min后测得N2的浓度是0.8molL﹣1 , 则在这10min内NH3的平均反应速率是( )
A.0.1molL﹣1min﹣1
B.0.3molL﹣1min﹣1
C.0.2molL﹣1min﹣1
D.0.6molL﹣1min﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com