
科目: 来源: 题型:
【题目】[Cu(NH3)4]SO4H2O是一种杀虫剂.
(1)Cu元素基态原子的电子排布式为 , 根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Cu属于区.
(2)元素N、O、S的第一电离能由大到小排列的顺序为 .
(3)H元素可与O元素形成H2O和H2O2 , H2O2易溶于H2O,其主要原因为 .
(4)H元素与N元素可组成化合物N2H4 , 其中N原子的轨道杂化方式为 .
(5)SO42﹣的空间构型是 , 与SO42﹣互为等电子体的一种分子的化学式为 .
(6)Cu元素与H元素可形成一种红色晶体,其结构如图,则该化合物的化学式为 . 
查看答案和解析>>
科目: 来源: 题型:
【题目】Fe(OH)3胶体区别于FeCl3溶液最本质的特征是 ( )
A. Fe(OH)3胶体粒子的大小在1~100 nm之间 B. Fe(OH)3胶体具有丁达尔效应
C. Fe(OH)3胶体是均一、稳定的分散系 D. Fe(OH)3胶体的分散质能透过滤纸
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组对含有Al3+的未知溶液进行了如下分析:
(1)滴加少量NaOH溶液,无明显变化;
(2)继续滴加NaOH溶液,有白色胶状沉淀生成;
(3)滴加过量的NaOH溶液,白色胶状沉淀明显减少。
实验小组经定量分析,得出如图所示沉淀的物质的量与滴加NaOH溶液体积的关系。下列说法错误的是 ( )
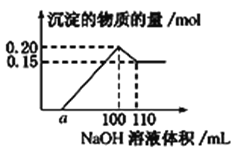
A. 该未知溶液中至少含有3种阳离子
B. NaOH溶液的物质的量浓度为5 mol·L-1
C. 若另一种离子为二价阳离子,则a=40
D. 若将最终沉淀过滤、洗涤、灼烧,其质量可能为6 g
查看答案和解析>>
科目: 来源: 题型:
【题目】图中曲线表示短周期元素的原子序数(按递增顺序连续排列)及其常见最高化合价的关系,下列叙述不正确的是 ( )

A. 单核简单离子半径大小为:②<③
B. ①、③可以按原子个数比1︰1形成化合物
C. ②、③形成的化合物是两性物质
D. ①、②形成的化合物的摩尔质量可能是44g/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学与技术]水处理技术在生产、生活中应用广泛.
(1)含有较多离子的水称为硬水.硬水加热后产生碳酸盐沉淀的离子方程式为(写出一个即可)
(2)将RH型阳离子交换树脂和ROH型阴离子交换树脂串接来软化天然硬水,应首先使硬水通过(填“RH”或“ROH”)型离子交换树脂,原因是 .
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为 . 电渗析法净化水时,使离子通过半透膜的推动力是 .
(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的 .
查看答案和解析>>
科目: 来源: 题型:
【题目】用右图所示实验装置(夹持仪器已略去)探索铜丝与过量浓硫酸反应的产物,下列有关说法不正确的是 ( )
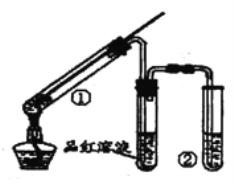
A. 品红溶液的作用是验证SO2的漂白性
B. 试管②中盛放的试剂可以是NaOH溶液或Na2SO3溶液
C. 停止反应后,立即向①中加水后溶液呈蓝色
D. 该反应中浓硫酸既表现了强氧化性,又表现了酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】现有三组溶液:①汽油和水溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液。分离以上各混合液的正确方法依次是( )
A. 分液、蒸馏、萃取B. 萃取、蒸发、分液
C. 分液、萃取、蒸馏D. 蒸馏、萃取、分液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
A.液溴和苯分别受热变为气体
B.干冰和氯化铵分别受热变为气体
C.二氧化硅和铁分别受热熔化
D.食盐和葡萄糖分别溶解在水中
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在VL密闭容器中,A、B、C三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析: 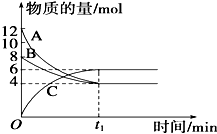
(1)反应的化学方程式为 .
(2)从开始到t1 min末时,用物质C表示的反应速率为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】研究NO2、SO2 . CO等大气污染气体的处理具有重要意义.
(1)NO2可用水吸收,相应的化学反应方程式为
利用反应6NO2+8NH3 ![]() 7N2+12H2O也可处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.
7N2+12H2O也可处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.
(2)已知:2SO2(g)+O2(g)![]()
![]() 2SO3(g)△H=﹣196.6kJmol﹣1
2SO3(g)△H=﹣196.6kJmol﹣1
2NO(g)+O2(g)═2NO2(g)△H=﹣113.0kJmol﹣1
则反应SO2(g)+NO2(g)=SO3(g)+NO(g)的△H=kJmol﹣1
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO2和NO的体积比保持不变 D.每消耗1molSO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应△H0(填“>”或“<”)实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 . 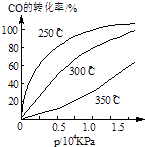
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com