
科目: 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积为2L的恒容密闭容器中发生反应xA (g) +yB (g) ![]() zC (g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n (A): n (B)的变化关系则下列结论正确的是
zC (g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n (A): n (B)的变化关系则下列结论正确的是
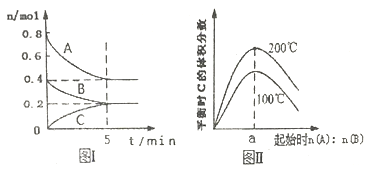
A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04 molL-1min-1
B. 图Ⅱ所知反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
C. 若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v正>v逆
D. 200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于50%
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温下,将a mol N2和b mol H2按一定比例混合,在相同状况下其密度是H2的 3.6倍,取5mol该混合气体通入密闭容器内,使之发生反应并在一定条件下达到平衡。已知反应达到平衡后容器内压强是相同条件下反应前压强的0.92倍,试求:
(1)反应前混合气体中N2和 H2的体积比a﹕b=__________;
(2)达到平衡时混合气体中的H2、NH3的物质的量分别是_____mol、_____mol;
(3)平衡时N2的转化率[n转化(N2)与n初始(N2)之比]________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用如图装置做相应实验,收集方法及所加试剂、现象、结论均正确的是
选项 | 气体 | 试剂 | 现象 | 结论 |
|
A | X | 酸性KMnO4溶液 | 溶液褪色 | X一定是SO2 气体 | |
B | NH3 | 酚酞溶液 | 溶液变红色 | 氨水呈碱性 | |
C | NO2 | 淀粉一KI溶液 | 溶液变蓝色 | NO2有还原性 | |
D | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | 氯水有酸性和漂白性 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子半径依次增大,且X、Y原子序数之和是W、Z原子序数之和的2 倍,m、n、p、r是由这些元素组成的元化合物,甲、乙是其中两种元素对应的单质,n 与乙均是淡黄色固体。上述物质的转化关系如图所示(部分反应物或生成物省略)。下列说法错误的是

A. 热稳定性: p<r
B. X 与Y组成的化合物一定有漂白性
C. 含Y 元素的盐溶液可能显酸性、中性或碱性
D. Z 与W、X、Y 可形成离子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】(i)燃料电池是目前正在探索的一种新型电池,目前已经使用的氢氧燃料电池的基本反应是正极:O2+2H2O+4e-=4OH-,回答下列问题:
(1)电解质溶液为____________。
(2)负极发生________反应(填“氧化”或“还原”)。写出其电极反应式___________。
(3)若反应后得到5.4 g液态水,此时氢氧燃料电池转移的电子数为________。
(ii)如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地往烧杯中央滴入CuSO4溶液。

(1)片刻后可观察到的现象是(指悬吊的金属圈)________。
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(2)产生上述现象的原因是___________________________________。
(iii)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:___________________________。
(2)若将(1)中的反应设计成原电池,并写出正、负极电极反应式。
正极反应:______________________,负极反应:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】H3BO3(一元弱酸) 可以通过电解NaB(OH)4溶液的方法制备,其工作原理如图,下列叙述错误的是

A. M室发生的电极反应式为:2H2O-4e- = O2↑+4H+
B. N室中:a% <b%
C. 理论上每生成1mol产品,阴极室可生成标准状况下5.6L气体
D. b膜为阴膜,产品室发生反应的化学原理为强酸制弱酸
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中:Fe2+、NO3﹣、SO42﹣、Na+
B.水电离出的c(H+)=10﹣12molL﹣1的溶液中:Ca2+、K+、Cl、HCO3﹣
C.![]() =1012的水溶液中:Al3+、NO3﹣、Cl﹣
=1012的水溶液中:Al3+、NO3﹣、Cl﹣
D.c(Fe3+)=0.1 molL﹣1的溶液中:K+、ClO﹣、SO42﹣、SCN﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com