
科目: 来源: 题型:
【题目】碘及其化合物在科研与生活中有很重要的作用。回答下列问题:
(1)碘可用作心脏起搏器电源——锂碘电池的材料,则碘电极是电池的______(填“正”或“负”)极。
(2)“加碘食盐”中含有少量的KIO3,向其中加入亚硫酸氢钠溶液,能产生使淀粉变蓝的物质,则该反应中氧化剂与还原剂的物质的量之比是_______________。
(3)碘单质与氢气反应的能量变化过程如图所示:

写出碘I2(s)转化成碘I2(g)的热化学方程式:__________________________________。
(4)在合成氨工业中用I2O5来测定CO的含量:5CO(g)+I2O5(s) ![]() 5CO2(g)+I2(s),在装有足量的I2O5固体的2L恒容密闭容器中通入2molCO发生上述反应,测得温度T1、T2下,一氧化碳的体积分数
5CO2(g)+I2(s),在装有足量的I2O5固体的2L恒容密闭容器中通入2molCO发生上述反应,测得温度T1、T2下,一氧化碳的体积分数![]() (CO)随时间t的变化曲线如图所示。回答下列问题:
(CO)随时间t的变化曲线如图所示。回答下列问题:
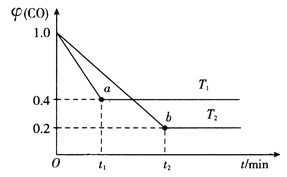
①温度T1下的平衡转化率![]() =________%,b点的平衡常数K2=__________。
=________%,b点的平衡常数K2=__________。
②在温度T2下,反应达到平衡后再充入适量的CO,重新达到平衡时;CO气体的转化率将_______(填“变大”“变小”或“不变”),该反应的△H_____(填“>”“<"或“=”)0。
③下列各种措施能提高该反应的CO转化率的是____________。
A.升温 B.加压 C.添加催化剂 D.移走部分CO2
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲把火扑灭,却被实验老师及时制止。原因是CO2可以支持镁燃烧,发生2Mg+CO2![]() 2MgO+C,下列关于该反应的判断正确的是( )
2MgO+C,下列关于该反应的判断正确的是( )
A. Mg元素化合价由0价升高到+2价,所以MgO是还原产物
B. 由此反应可以判断氧化性:CO2>MgO,还原性:Mg>C
C. CO2作氧化剂,表现氧化性,发生氧化反应
D. Mg原子失去的电子数目等于氧原子得到的电子数目
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸锶主要用于彩电显像管的荧屏玻璃和特种玻璃等的制造,通常由天青石矿(主要成分为SrSO4,还含有钡等杂质)制备,制备流程如图所示:
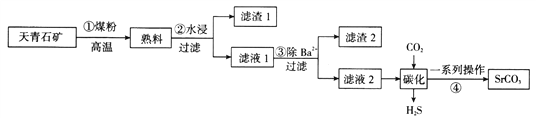
已知:i.锶在“滤液1”“滤液2”中均主要以Sr(HS)2、Sr(OH)2形式存在
ii.SrSO4、BaSO4的KSP分别是3.2×10-7、1.0×10-10
回答下列问题:
(1)步骤①反应:SrSO4+2C![]() SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为__________________。
SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为__________________。
(2)写出步骤②中“水浸”主要反应的化学方程式:________________________。步骤②“过滤”操作需要的主要玻璃仪器为________________________。
(3)上述生产工艺的优点是质量好、成本低,但从环保角度考虑该工艺生产存在明显的缺点是______________________________________________________。
(4)若向含有Sr2+、Ba2+的“滤液1”中滴加稀硫酸,当两种沉淀共存时,c(Sr2+):c(Ba2+)=________________。
(5)写出“碳化”过程中发生反应的化学方程式:_______________________________。
(6)某生产企业用a kg的天青石矿(含SrSO4:40%)制备,最终得到b kg碳酸锶产品,产率为______________(用含a、b的式子表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有下列三个反应:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列说法正确的是( )
A. 反应①②③中的氧化产物分别是I2、Fe3+、CoCl2
B. 根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C. 在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
D. 可以推理得到Cl2+FeBr2 =FeCl2+Br2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机化合物的叙述正确的是( )
A. 甲苯与氢气完全加成后产物的一氯代物的种类数是5种
B. 苯与液溴混合后加入铁粉可发生加成反应
C. 1 mol 苹果酸(HOOCCHOHCH2COOH)可与3 mol NaHCO3发生反应
D. 氟利昂-12的结构式为![]() ,该分子是平面型分子
,该分子是平面型分子
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸的组成用H2C2O4表示,为了测定某草酸溶液的浓度,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液,取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amolL﹣1的KMnO4溶液滴定到KMnO4不再褪色为止,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O.
试回答:
(1)实验中,标准液KMnO4溶液应装在_____式滴定管中,因为______________.
(2)实验中眼睛注视_____________________,直至滴定终点.判断到达终点的现象是_________.
(3)实验中,下列操作(其它操作均正确),会对所测草酸浓度有什么影响?(填偏大、偏小、无影响)
A. 滴定前仰视刻度,滴定后俯视刻度_________.
B. 锥形瓶在盛放待测液前未干燥,有少量蒸馏水_________.
C. 滴定过程中摇动锥形瓶,不慎将瓶内的溶液溅出一部分_________.
查看答案和解析>>
科目: 来源: 题型:
【题目】粗盐中含Ca2+、Mg2+、Fe3+、SO42—等杂质,需要提纯后才能综合利用。为除去粗盐中的杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
![]()
(1)提纯的步骤有:①加入过量的Na2CO3溶液②加入过量的BaCl2溶液③加入过量的NaOH溶液④调节溶液的pH等于7⑤溶解⑥过滤⑦蒸发,正确的操作顺序是________(填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(2)操作Z的名称是_____,蒸发操作用到的仪器有酒精灯,玻璃棒,三脚架,泥三角还有 ________。
(3)第Ⅱ步中,写出除去Ca2+和Fe3+相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2,Fe3+的主要存在形式为FeCl3)____________________、____________________。
(4)判断SO42—已沉淀完全的方法是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com