
科目: 来源: 题型:
【题目】二氧化硫和氯气都有漂白性,现把二者以等物质的量混合,让混合气体通入品红溶液,则其漂白性将( )
A.和氯气单独通过时相同B.和二氧化硫单独通过时相同
C.是二者作用效果之和D.可能失去漂白性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作中正确的是
A.分离溴苯与苯:用分液漏斗分液
B.萃取溴水中的溴:向溴水中加入己烷
C.制硝基苯:将苯、浓硝酸、浓硫酸的混合液用酒精灯加热
D.制取溴苯:将铁屑、溴水、苯混合加热
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. lL 1mol/LNa2CO3溶液中,CO32-离子总数为NA
B. 1LpH=2 的新制氯水中,阳离子总数为0.01NA
C. C与浓H2SO4加热生成4.48LCO2气体.转移的电子数为0.4NA.
D. 7.lg37Cl2中含有氯分子0.lNA
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米二氧化锆(ZrO2)是制备特种陶瓷(china)最重要的原料之一。由锆英石(主要成分为ZrSiO4)制备二氧化锆的工艺流程如图所示:
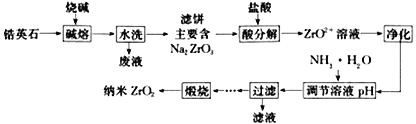
(1)写出“碱熔”时主要反应的化学方程式__________________________________。
(2)“水洗”所产生的“废液”主要成分为NaOH 和__________(填化学式),试写此成分的一种用途________________________________。
(3)写出“酸分解”生成ZrO2+反应的离子方程式__________________________________。
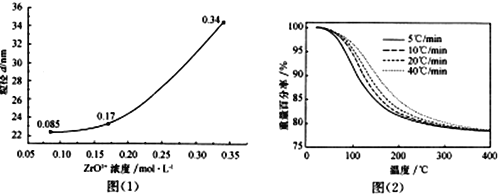
(4)根据图(1)分析ZrO2+浓度对ZrO2粒径的影响_____________________________________。
(5)ZrO2+溶液中常含有Fe3+(浓度为0.03mol·L-l),一般用草酸络合处理净化。若未净化处理直接加入氨水调节溶液pH,能否使ZrO2+完全转化为纯净的ZrO(OH)2沉淀,试通过计算说明。已知ZrO2+完全沉淀时浓度为1.0×10 -5 mol·L-l ,ZrO(OH)2、Fe(OH)3的Ksp分别为4.0×10-26、8.0×10-38, ![]() ≈3.16。__________________________________________________。
≈3.16。__________________________________________________。
(6)ZrO(OH)2煅烧制取纳米ZrO2时,升温速率与重量百分率之间的关系如图(2)所示。
煅烧时最佳升温速率为________________,理由是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,易挥发,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水;草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解(H2C2O4·2H2O ![]() 3H2O + CO↑ + CO2↑)。回答下列问题:
3H2O + CO↑ + CO2↑)。回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是有无色气泡且澄清石灰石变浑浊,由此可知草酸晶体分解的产物中有CO2,装置B的主要作用是____________________________________________________________________________。
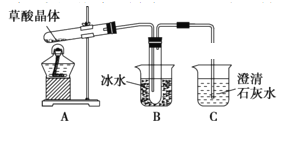
(2)乙组同学认为草酸晶体分解产物中还有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可重复选用)进行实验,装置H中装有的物质是CuO。
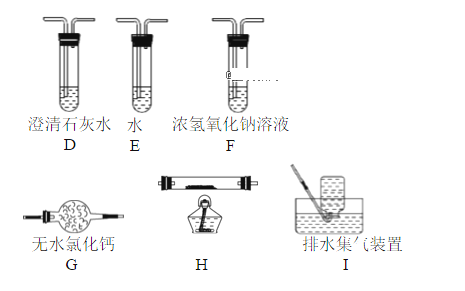
乙组同学的实验装置中,依次连接顺序为A、B、F、D、G、H、D、I。证明草酸晶体分解产物中有CO的现象是___________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列冶炼方法中,可制得相应金属单质的是 :
A. 工业上电解熔融MgO制镁 B. 加热分解Ag2O制银
C. 电解饱和食盐水制钠 D. 高温下分解CaCO3制钙
查看答案和解析>>
科目: 来源: 题型:
【题目】叠氮化钠(NaN3)是一种应用广泛的化工产品,可用于合成抗生素头孢菌素药物的中间体,汽车安全气囊等。回答下列问题:
Ⅰ.实验室制备NaN3
水合肼(N2H4·H2O) 与亚硝酸甲酯(CH3ONO)在氢氧化钠存在下制备NaN3,其反应装置如图所示:
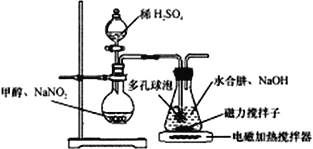
已知:2CH3OH+2NaNO2+H2SO4→2CH3ONO+ Na2SO4+2H2O; NaN3无色无味,微溶于醇、溶于水
(1)N2H4的电子式为_______________;NaN3晶体中阴离子与阳离子个数比为______________。
(2)装置中多孔球泡的作用是___________________。
(3)锥形瓶中水合肼与亚硝酸甲酯在30℃时可以反应生成叠氮酸钠、甲醇等物质,写出该反应的化学方程式_______________________________。
Ⅱ.回收甲醇
将制备反应后所得混合溶液加入烧瓶中,按照下图所示装置进行减压蒸馏。
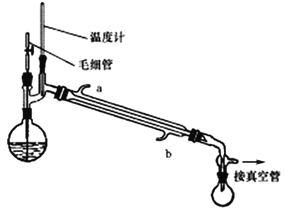
已知:
物质 | CH3OH | N2H4 | NaN3 |
沸点/℃ | 64.7 | 113.5 | 300 |
NaN3在40℃时分解
(4)实验时冷凝管中冷却水要“b进a出”原因是______________________。
(5)甲醇回收时需用减压蒸馏的原因是________________________。
(6)下列有关毛细管的作用说法正确的是_______________。
A.平衡圆底烧瓶内外压 B.作为气化中心,使蒸馏平稳
C.避免液体过热而暴沸 D.冷凝回流作用
Ⅲ.产品提取及纯度测定
将蒸馏后所得母液降温结晶,过滤得NaN3湿品;再用去离子水重结晶得NaN3产品并用碘量法测定产品纯度。取产品6.50g加入足量去离子水中溶解,并加入适量稀硫酸酸化;向混合液中加入20.00mL 1.00mol·L-lKMnO4溶液,溶液呈紫红色;再加入足量KI溶液消耗过量的KMnO4溶液;其后用0.100mol·L-lNa2S2O3标准溶液滴定所产生的I2,消耗Na2S2O3溶液30.00mL。
(7)实验所得产品的纯度为______________________。
已知:①产品中杂质不参与反应;
②测定过程中发生的反应:
10NaN3+2KMnO4+8H2SO4==2MnSO4+K2SO4+5Na2SO4+8H2O+15N2↑;
10KI+2KMnO4+8H2SO4==2MnSO4+6K2SO4+8H2O+5I2;
I2+2Na2S2O3==2NaI +Na2S4O6。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃某二元碱B(OH)2水溶液中,B2+、B(OH)+和B(OH)2三者各自的物质的量分数δ随溶液pH的变化曲线如图所示,下列说法错误的是(已知多元碱的电离是逐级进行的)
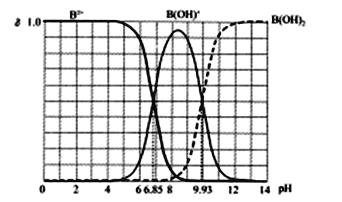
A. Kb2[B(OH)2]的数量级为10-8
B. 在B(OH)Cl溶液中c(OH-)>c(H+)
C. 等物质的量的BCl2和B(OH)Cl混合溶液中δ(B2+)<δ[B(OH)+]
D. B(OH)Cl溶液中,若c[B(OH)2]+2c(B2+)+c(H+)-c(OH-),则δ[B(OH)2]=δ[B(OH)+]
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:N2(g) + 3H2(g)![]() 2NH3(g) ΔH = 92 kJ·mol-1,下图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度。下列说法中,不正确的是
2NH3(g) ΔH = 92 kJ·mol-1,下图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度。下列说法中,不正确的是

A.X表示温度
B.L2>L1
C.反应速率 υ(M)>υ(N)
D.平衡常数 K(M)>K(N)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com