
【题目】二氧化硫和氯气都有漂白性,现把二者以等物质的量混合,让混合气体通入品红溶液,则其漂白性将( )
A.和氯气单独通过时相同B.和二氧化硫单独通过时相同
C.是二者作用效果之和D.可能失去漂白性
科目:高中化学 来源: 题型:
【题目】下列物质能使品红溶液褪色的是( )
①干燥的Cl2 ②Na2O2 ③NaClO ④活性炭 ⑤SO2
A. 除①外其它都可以 B. 只有②③⑤ C. 只有①④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,易挥发,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水;草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解(H2C2O4·2H2O ![]() 3H2O + CO↑ + CO2↑)。回答下列问题:
3H2O + CO↑ + CO2↑)。回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是有无色气泡且澄清石灰石变浑浊,由此可知草酸晶体分解的产物中有CO2,装置B的主要作用是____________________________________________________________________________。
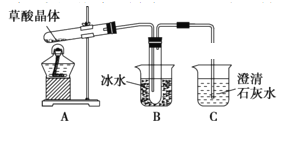
(2)乙组同学认为草酸晶体分解产物中还有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可重复选用)进行实验,装置H中装有的物质是CuO。
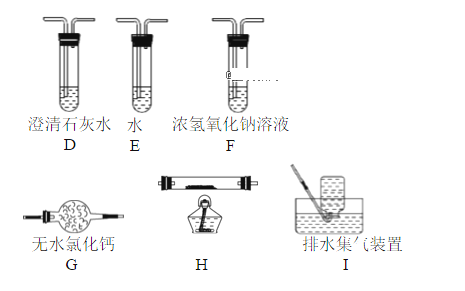
乙组同学的实验装置中,依次连接顺序为A、B、F、D、G、H、D、I。证明草酸晶体分解产物中有CO的现象是___________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:一定条件下,向A、B两个恒容密闭容器中分别加入等量的X(容器内所有物质均为气体),测得A、B容器中X的物质的量n(X)随时间t的变化如图所示。下列说法正确的是
A. A.B容积相同,但反应温度不同.且温度:A>B
B. A、B反应温度相同,但容积不同,且容积:A>B
C. a,b,c三点对应的平均相对分子质量:b>c>a
D. t2-t3时间段内,A、B两容器中平均反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图1、2、3为三套实验装置。
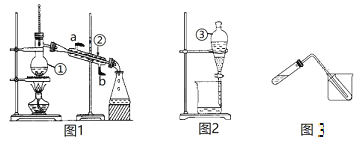
(1)图中所示仪器①和③的名称分别是_____________、_____________。
(2)图1装置可用于少量蒸馏水的制取,需要在仪器①中加入碎瓷片,目的是___________________;仪器②中冷却水的入口是__________(填“a”或“b”);图3装置也可用于少量蒸馏水的制取(加热及固定仪器略),该装置中使用的玻璃导管较长,其作用是____________。
(3)若用CCl4从碘水中萃取I2并用图2装置进行分离,振荡后静置观察到的现象是___________________________________________________________;在用图2装置进行分液操作时,为使液体顺利滴下,应进行的具体操作是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)图1表示电解饱和NaCl溶液的装置,X、Y是石墨棒。实验开始时,在两边溶液中同时各滴入几滴酚酞溶液,请回答以下问题:
①X极上的电极反应式是______________________________________________________。
②电解NaCl溶液的离子方程式是____________________________________________。
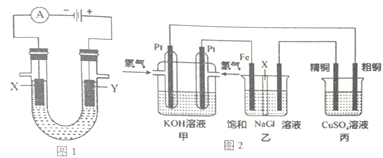
(2)图2是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
根据要求回答相关问题:
①通入氢气电极的反应式为______________________________________________________________。
②石墨电极(乙装置中右侧电极)为__________极(填“阳”或“阴”),反应一段时间后,在乙装置中滴入酚酞溶液,__________极区(填“铁”或“石墨”)的溶液变红。
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将__________(填“增大”、“减小”或“不变”)。
④若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为__________L;丙装置中阴极析出铜的质量为__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电石渣(主要成分为Ca(OH)2和CaCO3)为原料制备KClO3的流程如下:
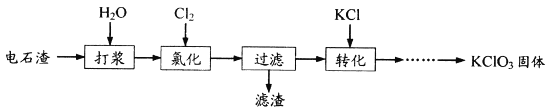
下列说法不正确的是
A. 氯化过程中主反应为:6Ca(OH)2+6Cl2= Ca(ClO3)2+5CaCl2+6H2O
B. 适当减缓通Cl2速率,充分搅拌浆料,加水使Ca(OH)2完全溶解,均有利于氯气的吸收
C. 滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2]:n[CaCl2]=1:5
D. 向滤液中加入稍过量KC1固体可将Ca(ClO3)2转化为KClO3,通过蒸发浓缩、冷却结晶的方法析出KClO3晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com