
科目: 来源: 题型:
【题目】对某难溶电解质AnBm的饱和溶液中,下列说法正确的是
A. 加同温度的水,其溶度积减小、溶解度增大
B. 升高温度,它的溶解度和溶度积都增大
C. 饱和溶液中c(Am+)=c(Bn﹣)
D. 加同温度的水,其溶度积、溶解度均不变
查看答案和解析>>
科目: 来源: 题型:
【题目】人教版高中化学选修4实验2-3中用到了硫代硫酸钠,某化学兴趣小组对这一物质展开了如下探究。

实验一.制备Na2S2O3·5H2O
通过查阅资料,该化学兴趣小组设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体。
已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l) ; S(s)+Na2SO3(aq) ![]() Na2S2O3(aq)
Na2S2O3(aq)
(1)写出A中的化学反应方程式___________________________________。
(2)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有_________________________(写一条)
(3)装置E的作用是____________________。
(4)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为_________________________。
实验二.性质探究
(5)常温下,用pH试纸测定0.1 mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是_______________________________________________________。
(6)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子化学方程式________________________________________。
实验三.Na2S2O3的应用
(7)用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00 mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解。此时CrO42-全部转化为Cr2O72-;再加过量KI溶液,充分反应后,加入淀粉溶液作指示剂,用0.0100 mol·L-1的Na2S2O3标准溶液进行滴定,反应完全时,相关数据记录如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗Na2S2O3标准溶液的体积/mL | 18.02 | 20.03 | 17.98 | 18.00 |
部分反应的离子方程式为:① Cr2O72-+6I-+14H+===3I2+2Cr3++7H2O
② I2+2S2O32-===S4O62-+2I-
滴定时Na2S2O3标准溶液应该用_____________________(填仪器名称)盛装,该废水中Ba2+的物质的量浓度为_______________________span>。
查看答案和解析>>
科目: 来源: 题型:
【题目】C、N、O、Si、P、Ge、As及其化合物在科研和生产中有许多重要用途。请回答下列问题:
(1)基态氮原子核外电子占据的原子轨道数目为_________________。
(2)图1表示碳、硅和磷三种元素的四级电离能变化趋势,其中表示磷的曲线是___(填标号)。

(3)NH3的沸点比PH3高,原因是___________________________。
(4)根据等电子原理,NO+电子式为______________。
(5)Na3AsO4中AsO43-的空间构型为______________,As4O6的分子结构如图2所示,则在该化合物中As的杂化方式是______________。
(6)锗的某种氧化物晶胞结构如图3所示,该物质的化学式为____________。已知该晶体密度为7.4g/cm3,晶胞边长为4.31×10-10m。则锗的相对原子质量为____________(保留小数点后一位)。(已知:O的相对原子质量为16,4.313=80,NA=6.02×1023mol-1)
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2O![]() H+ + OH-,下列叙述正确的是
H+ + OH-,下列叙述正确的是
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D. 将水加热,Kw增大,pH不变
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米级Cu2O既是航母舰艇底部的防腐蚀涂料,也是优良的催化剂。
(1)已知:1克碳粉燃烧全部生成CO气体时放出9.2kJ热量,2Cu2O(s)+O2(g)= 4CuO(s) ΔH =–292kJmol-1,则工业上用碳粉与CuO粉末混合在一定条件下反应制取Cu2O(s),同时生成CO气体的热化学方程式为________________________________________。
(2)用纳米级Cu2O作催化剂可实现甲醇脱氢可制取甲醛:
CH3OH(g)![]() HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。
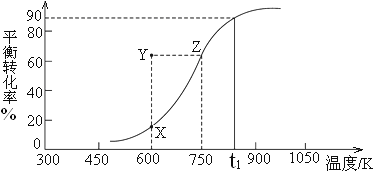
①该反应的ΔH___0 (填“>”或“<”);600K时,Y点甲醇的υ(正) ____υ(逆)(填“>”或“<”)。
②从Y点到X点可采取的措施是___________________________________。
③在t1K时,向固定体积为2L的密闭容器中充入1molCH3OH(g),温度保持不变,9分钟时达到平衡,则0~9min内用CH3OH(g)表示的反应速率v(CH3OH)=_____________, t1K时,该反应的平衡常数K=____________。
(3)研究表明,纳米级的Cu2O也可作为太阳光分解水的催化剂。
① 其他条件不变时,若水的分解反应使用Cu2O催化剂与不使用催化剂相比,使用催化剂会使该反应的活化能___________ (填“增大”、“减小”或“不变”),反应热(ΔH)______(填“增大”、“减小”或“不变”)。
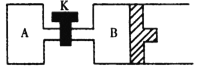
② 如图所示,当关闭K时,向容器A、B中分别充入0.04molH2O(g),起始时V(A) = V(B) = 2L。在一定条件下使水分解(反应过程中温度保持不变,B中活塞可以自由滑动),达到平衡时,V(B) = 2.4L。平衡时,两容器中H2O(g)的分解率A_____________B (填“<”、“=”或“>”)。打开K,过一段时间重新达平衡时,B的体积为____________L。(连通管中气体体积不计)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一透明溶液,可能含有Al3+、Fe3+、K+、NH4+、Mg2+和Cu2+等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。加入Na2O2的量与生成白色沉淀的量之间的关系用图来表示。
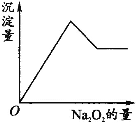
试推断:
(1)原溶液中一定含有________。
(2)一定不含有________。
(3)可能含有________。
(4)为了进一步确定可能含有的离子,应增加的实验方法为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A. CuCl2溶液蒸干灼烧后得到CuCl2固体
B. 火力发电的目的是使化学能转换为电能
C. 已知C(石墨,s)= C(金刚石,s)△H>0,无法比较二者的稳定性
D. 将FeCl3固体溶于适量蒸馏水来配制FeCl3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】将1.5 mol Cu2S和足量稀HNO3反应,生成Cu(NO3)2、H2SO4、NO和H2O。则参加反应的硝酸中被还原的硝酸的物质的量是
A. 5 mol B. 1.5 mol C. 6 mol D. 1mol
查看答案和解析>>
科目: 来源: 题型:
【题目】40℃时,在氨-水体系中不断通入CO2,各种离子变化趋势如图所示。下列说法不正确的是
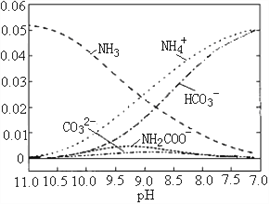
A. 当8.5<pH<10.5时,会有中间产物(NH2COOˉ)生成
B. 在pH=9.5时,溶液中存在关系:c(NH4+)>c(HCO3ˉ)>c(NH2COOˉ)>c(CO32ˉ)
C. 在pH=9.0时,溶液中存在关系:c(NH4+)+c(H+)=2c(CO32ˉ)+c(HCO3ˉ)+c(NH2COOˉ)+c(OHˉ)
D. 随着CO2的通入,![]() 不断减小
不断减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com