
科目: 来源: 题型:
【题目】(1)相同质量的下列各烃,完全燃烧后生成CO2最多的是____(填标号)
A.乙炔 B.乙烯 C.乙烷 D.甲烷
(2)某烃的一种同分异构体,核磁共振氢谱测得分子中只有一个吸收峰,则该烃的分子式可能为______(填标号)
A.C6H14 B.C7H16 C.C8H18 D.C9H20
(3)乙烯和丙烯属于同系物。下列叙述正确的是_____上(填标号)
A.等质量的乙烯和丙烯完全燃烧耗氧量相同
B.丙烯分子中三个碳原子处于同一直线上
C.乙烯和丙烯与HCl加成均有两种产物
D.以丙烯为单体加聚可以生成![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:
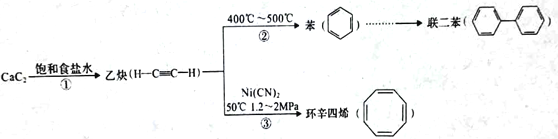
(1)反应①类似盐的水解,写出CaC2的电子式_________。
(2)苯是由哪位科学家首先发现的________,苯分子中有三个氢原子被-Br、-Br、-OH取代得到的芳香族化合物有_____种。将苯分子中的一个碳原子换成一个氮原子,得到一种类似苯环结构的稳定有机物,则此有机物的相对分子质量为________。
(3)写出反应③的化学反应方程式并注明反应类型__________。
(4)联二苯的化学式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
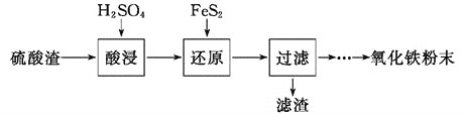
(1)“酸浸”中硫酸要适当过量,目的是___________。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为___________。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定。有关反应的化学方程式如下:
2Fe3++Sn2++6Cl—=2Fe2++SnCl62—
Sn2++4Cl—+2HgCl2=SnCl62-+Hg2Cl2↓
6Fe2++Cr2O72—+14H+=6Fe3++2Cr3++7H2O
滴定时,K2Cr2O7标准溶液应盛放在滴定管中___________ (填“酸式”、“碱式”);若不加HgCl2,则测定的Fe3+量___________ (填“偏高”、“偏低”或“不变”)。
(4)①可选用___________ (填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是___________ (用离子方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
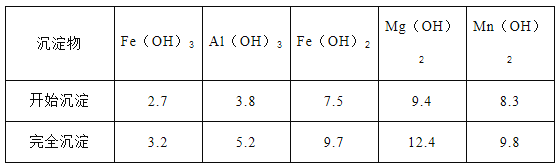
实验可选用的试剂有:稀硝酸、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:___________
a.氧化:。 b.沉淀:。 c.分离,洗涤。 d.烘干,研磨。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列装置图中的实验方案能达到实验目的的是
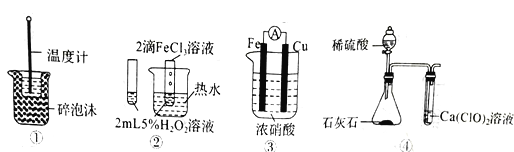
A. 图①可用于中和热的测定
B. 图②可验证FeCl3对H2O2分解反应有催化作用
C. 图③可用于探究铁作负极的原电池原理
D. 图④可用于验证酸性:H2SO4>H2CO3>HClO
查看答案和解析>>
科目: 来源: 题型:
【题目】下列所得溶液中,其物质的量浓度为1.0 mol/L的是( )
A. 将20 g NaOH溶解在500 mL水中
B. 将22.4 L HCl气体溶于水配成1 L溶液
C. 将62.5 g胆矾(CuSO4·5H2O)溶解在适量水中,再加蒸馏水直到溶液的体积为250 mL
D. 将100 mL 10 mol/L的硫酸加入到900 mL水中
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(1)用双线桥表示出电子转移的方向和数目________,题干中反应改写成离子方程式是____。
(2)电解食盐水的过程中,被还原的元素是____________,氧化产物是______。
Ⅱ.四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是:3Fe2++2S2O32-+O2+xOH-=Fe3O4↓+S4O62-+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是__________。
(2)反应的化学方程式中x=______。
(3)每生成1 mol Fe3O4,反应转移的电子为____mol,被Fe2+还原的O2的物质的量为_____mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)Na2O2与CO2的反应化学方程式____________________________________________;7.8gNa2O2固体与足量的CO2反应转移的电子数为_______________个
(2)向硫酸氢钠溶液中逐滴加入氢氧化钡溶液到中性,请写出发生反应的离子方程式________。
(3)写出铁与水反应蒸气反应的化学方程式__________________;
(4)等体积、等浓度的碳酸氢钙溶液和氢氧化钠溶液混合的离子方程式____________;
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组按如图所示实验流程比较浓硝酸和稀硝酸的氧化性强弱,其中B为一种紫红色金属,C为红棕色气体。
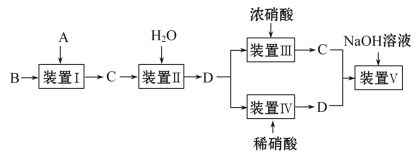
请回答下列问题:
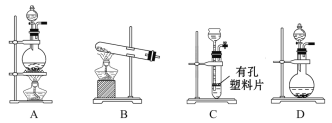
(1)A与B反应的化学方程式是___________________________________;A与B反应迅速,实验中需要采取措施控制气体放出的快慢及多少,则装置Ⅰ可以选择的装置为________。
(2)实验时在装置Ⅰ中加入B后,在加入A之前需向整套装置中通入足量的CO2气体,该操作的目的是______。
(3)装置Ⅱ中发生反应的化学方程式是_________________________。
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸______(填“强”或“弱”),判断的依据是_________。
(5)小组内有同学指出该流程中装置Ⅴ可有可无,你认为装置Ⅴ是否需要___ (填“是”或“否”),理由是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:

(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入________(填“A”或“B”),再滴加另一反应物。
(2)如下图所示,过滤操作中的一处错误是________________________________________。

(3)判断流程中沉淀是否洗净所用的试剂是__________________________________________。高温焙烧时,用于盛放固体的仪器名称是___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NaH与水反应化学方程式为NaH+H2O=NaOH+H2↑ 在该反应中H20是
A、是氧化剂
B、是还原剂
C、既是氧化剂又是还原剂
D、 既不是氧化剂又不是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com