
科目: 来源: 题型:
【题目】化学家们合成了一种新物质——五星烷,其键线式如图所示。下列有关五星烷的说法正确的是( )

A. 五星烷与乙烷互为同系物 B. 五星烷的化学式为C15H20
C. 五星烷的分子中含有7个五元环 D. 五星烷的一氯代物有3种
查看答案和解析>>
科目: 来源: 题型:
【题目】某Cr2O3样品中含有少量Al2O3、MgO等杂质。实验室以此样品为主要原料制取重铭酸钾(K2Cr2O7)的流程如下:

已知:2CrO42-+2H+![]() Cr2O72-+H2O。
Cr2O72-+H2O。
(1)上述氧化过程中,若将1 mol Cr2O3转化成Na2CrO4,消耗氧气的体积(标准状况)是__________。
(2)称取重铬酸钾试样2.40g配成250 mL溶液,取出25.00 mL于碘量瓶中,加入稀硫酸和足量碘化钾(铬被还原为Cr3+)并放于暗处6 min左右,然后加入适量水和数滴淀粉指示剂,用0.24 mol·L-1Na2S2O3标准溶液滴定至终点(发生反应:I2+2S2O32-=2I-+S4O62-,杂质不参与反应),共用去Na2S2O3标准溶液20.00 mL。求所得产品中重铬酸钾的质量分数(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】中草药秦皮中含有的七叶树内酯(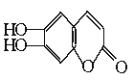 碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
A. 3mol Br22mol NaOH B. 3mol Br24mol NaOH
C. 2mol Br23mol NaOH D. 4mol Br24mol NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
元素 | Al | B | Be | C | Cl | F | Li |
X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
元素 | Mg | Na | O | P | S | Si | |
X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
试结合元素周期律知识完成下列问题:
(1)请预测K与Rb元素的X数值的大小关系:K ______ Rb (填“>”、“=”或“<”)。
(2)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键,试推断AlBr3中的化学键类型是____。
(3)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于____原子(填元素符号).
(4)简述第二周期元素(除稀有气体外)的X的数值大小与原子半径之间的关系:________。
Ⅱ.(1)
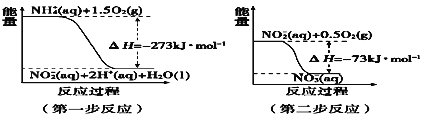
①第一步反应是____反应(选填“放热”或“吸热”),判断依据_____。
②1 molNH4+(aq)全部氧化成NO3- (aq)的热化学方程式_______。
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:
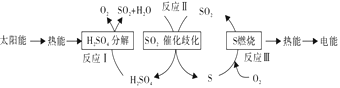
反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ/mol
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=297 kJ/mol
反应Ⅱ的热化学方程式:_______________。
(3)一定条件下,不同量的CO2与不同量的NaOH充分反应放出的热量如下表所示:
CO2的量 | NaOH的量 | 放出的热量 |
22.0 g | 750 mL 1.0 mol/L | x kJ |
1.0 mol | 2.0 L 1.0 mol/L | y kJ |
写出该条件下,CO2与NaOH反应生成NaHCO3的热化学方__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是________________。当1 mol O2发生反应时,还原剂所失电子的物质的量为_________mol。
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S===2K2SO4+2Al2O3+9SO2+48H2O,在该反应中,还原剂是_____________。
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:________________________。
(4)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
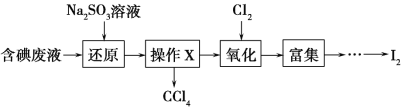
向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_________________;该操作将I2还原为I-的目的是________________________。
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是________________。
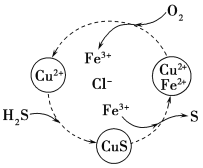
(6)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为________________,反应消耗1 mol NaBH4时转移的电子数目为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示装置,烧杯中盛有200mL1 mol/L的CuSO4溶液。

(1)正极材料为______,电池工作时SO42-向______移动(填Zn或Cu)。
(2)正极电极反应式为_______。
(3)若初始时Zn片与Cu片质量相等,实验结束后,称得两极质量差为12.9g,则反应中转移电子的物质的量为____,反应后溶液中溶质的物质的量浓度为________(忽略溶液体积的变化)。
查看答案和解析>>
科目: 来源: 题型:
【题目】1999年4月,比利时查出污染鸡的根源是生产鸡饲料的油脂被二恶英所污染,二恶英是两大芳香族化合物的总称。其中四氯代二苯并二恶英毒性最大,其结构简式为:
下列有关该化合物的说法中正确的是( )
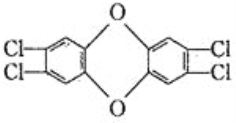
A. 分子式为C12H8O2Cl4
B. 是一种可溶于水的气体
C. 是最危险的致癌物之一
D. 是一种多卤代烃
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是( )
A.NaHCO3受热易分解,可用于制胃酸中和剂
B.SiO2熔点高、硬度大,可用于制光导纤维
C.Al2O3是两性氧化物,可用作耐高温材料
D.硅胶多孔能吸水,可用作食品干燥剂
查看答案和解析>>
科目: 来源: 题型:
【题目】配制100 mL 1.0 ![]()
![]() 的NaOH溶液,下列情况会导致溶液浓度偏低的是( )
的NaOH溶液,下列情况会导致溶液浓度偏低的是( )
A. 容量瓶使用前经蒸馏水清洗后没有干燥
B. 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C. 俯视确定凹液面与刻度线相切
D. 用敞口容器称量NaOH且时间过长
查看答案和解析>>
科目: 来源: 题型:
【题目】已知歧化反应:3NO2+H2O===2HNO3+NO,下列说法正确的是( )
A. 氧化产物与还原产物的物质的量之比为1∶2
B. 氧化剂与还原剂的物质的量之比为1∶2
C. 1 mol NO2与足量水反应转移电子个数为2NA
D. 每生成22.4 L NO,有2 mol NO2被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com