
科目: 来源: 题型:
【题目】下列实验过程中产生的现象与对应的图形相符的是( )
A.  NaHSO3 粉末加入HNO3溶液中B.
NaHSO3 粉末加入HNO3溶液中B. 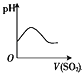 SO2气体通入新制氯水中
SO2气体通入新制氯水中
C. 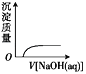 NaOH溶液滴入 Ba(HCO3)2溶液中D.
NaOH溶液滴入 Ba(HCO3)2溶液中D.  CO2气体通入澄清石灰水中
CO2气体通入澄清石灰水中
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于SO2的说法中,不正确的是
A.SO2不能用来漂白食品
B.SO2具有漂白性,可以使品红溶液褪色
C.SO2与水反应生成H2SO4
D.SO2是一种大气污染物,它主要来自于化石燃料的燃烧
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G是短周期元素,周期表中B与C相邻,C与E同主族;A中L层是K层的2倍,B的电子数比C的电子数少1个;F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的气体单质,且溶液使酚酞溶液变红。G是第三周期原子半径最小的主族元素。
(1)B在元素周期表中的位置_____;D的最高价氧化物的水化物的电子式____,用电子式表示FGC的形成过程为_______;
(2)B与F元素可形成18电子分子的电子式为_____。
(3)A、B、C的氢化物稳定性顺序为_______(用分子式表示);G的阴离子的还原性_____(大于或小于)E的阴离子。
(4)F2C和F2E中,沸点较高的是____(填化学式),其主要原因是_____。
(5)锡(Sn)是古代五金之一,在第五周期第ⅣA,锡能和浓硫酸反应生成Sn(SO4)2和刺激性气味气体,反应的化学方程式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积为2L的密闭容器中发生2SO2+O2 ![]() 2SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;②在400℃时,20molSO2与5molO2反应;③在300℃时,10molSO2与5molO2反应;
2SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;②在400℃时,20molSO2与5molO2反应;③在300℃时,10molSO2与5molO2反应;
(1)开始时正反应速率最快的是_________。
(2)若10min内测得第①组的平均反应速率为:V(SO2)=0.4mol/(L·min),则10min时,生成的SO3浓度为_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I. 已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,下列叙述中正确的是

(1)a、b分别代表的意思是_______________、___________________。
(2)该反应ΔH_______________________
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器A的名称为________________,干燥管D的作用为___________________。
(4)若要证明非金属性:Cl>I,C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为________,观察到C中溶液____________ (填现象),即可证明。从环境保护的观点考虑,此装置缺点 __________。
(5)若要证明非金属性:S>C>Si,则在A中__________B中加_________、C中加__________,写出C中反应的化学方程式______________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】在无色透明的溶液中可以大量共存的离子组是()
A.OH-、K+、Al3+、SO42-B.OH-、NH4+、Cl-、Na+
C.Cu2+、NO3-、Cl-、SO42-D.Mg2+、K+、Cl-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,可逆反应:mA+nB![]() pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则m+n和p的关系是
(2)A、C是气体,增加B的量,平衡不移动,则B为 态。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(4)加热后,可使C的质量增加,则正反应是 反应(放热或吸热)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:
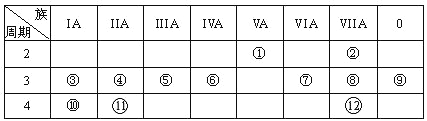
(1)画出原子的结构示意图:④______________
(2)在①~12元素中,金属性最强的元素是______,非金属性最强的元素是____,最不活泼的元素是_____。(均填元素符号)
(3)元素⑦与元素⑧相比,非金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)元素⑤的最高价氧化物的水化物分别与元素③⑧的最高价氧化物的水化物反应的离子方程式_________, _________
(5)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程:__________。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:______________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应在210℃达到平衡:
PCl5(g)![]() PCl3(g)+Cl2(g) △H >0 K=1 ①
PCl3(g)+Cl2(g) △H >0 K=1 ①
CO(g)+Cl2(g)![]() COCl2(g) △H <0 K=5×104 ②
COCl2(g) △H <0 K=5×104 ②
COCl2(g)![]() CO(g)+ Cl2(g) △H >0 ③
CO(g)+ Cl2(g) △H >0 ③
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示____________,K值大小与温度的关系是:温度升高,K值___________________(填一定增大、一定减小、或可能增大也可能减小)。
(2)根据反应①的平衡常数K的表达式,平衡时,下列等式必定成立的是___________
A.c(PCl5) = c(PCl3)= c(Cl2)=1
B.c(PCl5)= c(PCl3)·c(Cl2)=1
C.c(PCl5)= c(PCl3)·c(Cl2)
(3)降低Cl2浓度,反应③的K值___________(填“增大”、“减少”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com