
科目: 来源: 题型:
【题目】乙二酸通常以二水合物的形式存在,俗称草酸晶体.已知草酸晶体在101℃时熔化并开始升华,157℃时大量升华,继续升温会分解生成CO、CO2和H2O。
(1)下列关于乙二酸的叙述正确的是(填编号)_____________
①能和乙二醇发生酯化反应
②能使酸性高锰酸钾溶液褪色
③其溶液能使蓝色石蕊试纸变红
④能和碳酸氢钠溶液反应生成气体
(2)乙二酸的工业生产方法之一是以乙二醇为原料,在一定条件下,用空气氧化得到.写出该反应的化学反应方程式:__________________________________
(3)欲检验草酸晶体受热分解的产物中是否有CO2,甲、乙两位同学分别设计了装置1、装置2来完成实验.
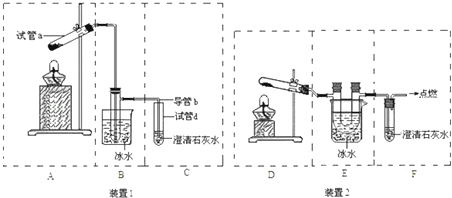
(Ⅰ)简述检验装置1气密性的操作方法:______________________________________
(Ⅱ)B和E两个装置中更合理的是______________
(Ⅲ)请从A~F中选择合适的仪器,组装一套可更好达到实验目的装置,按照气流由左到右的顺序依次为(用字母表示):________________.
(Ⅳ)一定条件下草酸氢铵分解生成NH3、CO、CO2和H2O,110℃时将该混合气体先通过Na2O2,再通过浓硫酸分别增重Ag和Bg; 若将混合气体先通过浓硫酸,再通过Na2O2分别增重Cg和Dg(能反应的气体均可吸收完全,且该条件下CO与Na2O2不反应),则A、B、C、D的大小关系为:______________
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①﹣⑩在表中的位置,回答下列问题:
IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
3 | ⑧ | ⑨ | ⑩ |
(1)自然界物质种类最多的元素在周期表中的位置是______
(2)⑧⑨⑩的离子半径由大到小的顺序为______(填化学用语).
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式______
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式____________
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式______.
查看答案和解析>>
科目: 来源: 题型:
【题目】H是一种新型香料的主要成分之一,其合成路线如下(部分产物和部分反应条件略去):
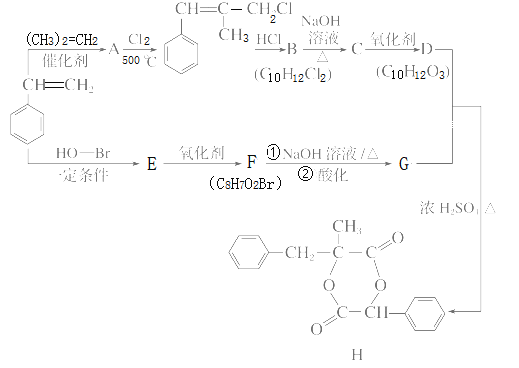
已知:①RCH==CH2+CH2==CHR′![]() CH2==CH2+RCH==CHR′;
CH2==CH2+RCH==CHR′;
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子。
请回答下列问题:
(1)(CH3)2C==CH2的同分异构体中存在顺反异构的有机物的名称为________________。
(2)A的核磁共振氢谱除苯环上的H外,还显示______组峰,峰面积比为____。
(3)D分子中含有的含氧官能团名称是____________________________, E的结构简式为____________________________________________。
(4) D和G反应生成H的化学方程式为_____________________________________。
(5)G的同分异构体中,同时满足下列条件的有种(不包括立体异构)_____________。
①苯的二取代物 ②与FeCl3溶液发生显色反应 ③含“-O-”结构
(6)参照上述合成路线,以丙烯为原料(无机试剂任选),设计制备2,3--丁二醇的合成路线________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某无机化合物的二聚分子结构如图,该分子中A、B两种元素都是第三周期的元素,分子中所有原子最外层都达到8电子稳定结构。关于该化合物的说法不正确的是( )

A. 化学式是Al2Cl6
B. 不存在离子键和非极性共价键
C. 在固态时所形成的晶体是分子晶体
D. 是离子化合物,在熔融状态下能导电
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸;在空气中迅速被氧化成绿色;见光则分解,变成褐色.如图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl﹣)生产CuCl的流程:
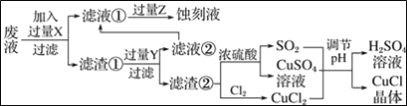
根据以上信息回答下列问题:
(1)写出生产过程中所加试剂:X_______,Y________
(2)生产中为了提高CuCl产品的质量,采用抽滤法快速过滤,析出的CuCl晶体不用水而用无水乙醇洗涤的目的是_________________;生产过程中调节溶液的pH不能过大的原因是__
(3)写出产生CuCl的化学方程式:__________________________________
(4)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A.氯气的性质很活泼,它与氢气混合后立即发生爆炸
B.实验室制取氯气时,为了防止污染环境,多余的氯气可以用氢氧化钙溶液吸收
C.新制氯水的漂白性强于久置氯水的漂白性
D.检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下面关于硅的叙述中,正确的是( )
A. 二氧化硅可用于光导纤维,利用了它的导电性
B. 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C. 硅的化学性质不活泼,在自然界中可以以游离态形式存在
D. 硅在电子工业中是重要的半导体材料
查看答案和解析>>
科目: 来源: 题型:
【题目】研究含氮化合物对能源、环保和生产具有重要的意义。请回答下列问题:
(1)在2 L密闭容器内, 800 ℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①如图所示A点处v正___(填“>”、“<”或“=”,下同)v逆,A点处v正___B点处v正。
②如图所示的曲线,其中表示NO2的变化的曲线是________(填a、b、c、d等字母)。用O2表示2 s内该反应的速率v=________。
(2)已知化学反应N2+3H2![]() 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,
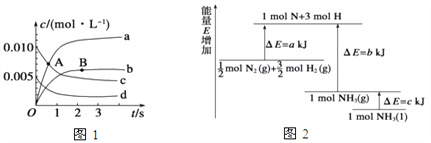
则,1 mol N和3 mol H生成1 mol NH3(g)是______能量的过程(填“吸收”或“释放”),由![]() mol N2(g)和
mol N2(g)和![]() mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。
mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:
Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后获得试样溶液,设计并完成了如下的实验:

已知:3NO3-+8Al+5OH—+2H2O ![]() 3NH3↑+8A1O2—
3NH3↑+8A1O2—
根据以上的实验操作与现象,该同学得出的结论正确的是
A. 不能确定试样中是否含Al3+
B. 试样中肯定存在NH4+、Mg2+和SO42-,其他离子都不能确定
C. 要确定试样中是否有Na+存在,可做焰色反应实验,若焰色为紫色,则存在Na+
D. 沉淀2只可能是碳酸钡
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
A. 放电时负极反应为Zn-2e-+2OH-===Zn(OH)2
B. 放电时正极反应为FeO42-+4H2O+3e-===Fe(OH)3+5OH-
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com