
科目: 来源: 题型:
【题目】半富马酸喹硫平可用于精神疾病的治疗,下图所示是其多条合成路线中的一条:
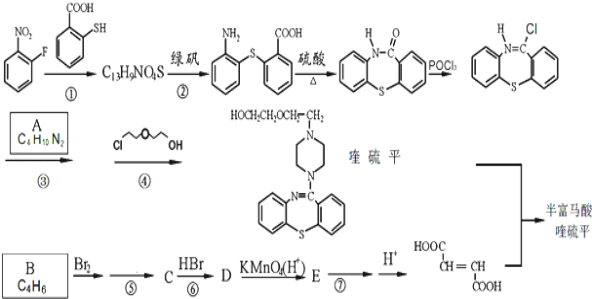
完成下列填空:
(1)反应①的反应类型是___________,反应⑤的试剂及反应条件是___________。
(2)写出结构简式:A___________; B___________。
(3)写出反应⑦的化学方程式_______________________________________________。
(4)写出反应③和④中生成的相同产物的化学式_________。反应⑤和⑦的目的是______________。
(5)化合物![]() 消去HCl后的产物记为F,写出两种F的能发生银镜反应、且只含3种不同化学环境氢原子的同分异构体的结构简式_____________________________。
消去HCl后的产物记为F,写出两种F的能发生银镜反应、且只含3种不同化学环境氢原子的同分异构体的结构简式_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学中常借助于图像这一表现手段以清晰地突出实验装置的要点,形象地阐述化学过程的原理。 下列有关化学图像表现的内容正确的是
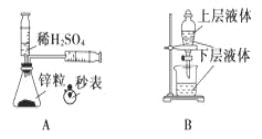
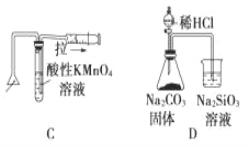
A. 测定一定时间内生成 H2 的反应速率 B. 提取海带中的碘
C. 检验火柴燃烧产生的 SO2 D. 证明非金属性:Cl>C>Si
查看答案和解析>>
科目: 来源: 题型:
【题目】在2A(g)+3B(g)![]() 2C(g)+D(g)中,下列表示反应速率最快的是
2C(g)+D(g)中,下列表示反应速率最快的是
A. v(A)=0.5 mol/(L·min)B. v(B)=0.6 mol/(L·min)
C. v(C)=0.4 mol/(L·min)D. v(D)=0.3 mol/(L·min)
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组设计不同实验方案比较Cu2+、Ag+ 的氧化性。
查阅资料:Ag+ + I- = AgI↓ K1 =1.2×1016;2Ag+ + 2I- = 2Ag↓+ I2 K2 = 8.7×108
(1)方案1:通过置换反应比较
向酸化的AgNO3溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性Ag+>Cu2+。反应的离子方程式是___________________________________________________。
(2)方案2:通过Cu2+、Ag+ 分别与同一物质反应进行比较
实验 | 试 剂 | 编号及现象 | |
试 管 | 滴 管 | ||
| 1.0 mol/L KI溶液 | 1.0 mol/L AgNO3溶液 | Ⅰ.产生黄色沉淀,溶液无色 |
1.0 mol/L CuSO4溶液 | Ⅱ.产生白色沉淀A,溶液变黄 | ||
①经检验,Ⅰ中溶液不含I2,黄色沉淀是________。
②经检验,Ⅱ中溶液含I2。推测Cu2+做氧化剂,白色沉淀A是CuI。确认A的实验如下:
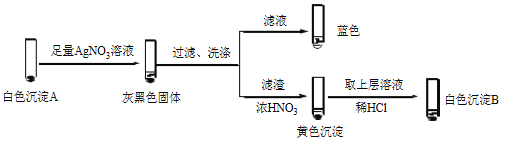
a.检验滤液无I2。溶液呈蓝色说明溶液含有________(填离子符号)。
b.白色沉淀B是________。
c.白色沉淀A与AgNO3溶液反应的离子方程式是___________,说明氧化性Ag+>Cu2+。
(3)分析方案2中Ag+ 未能氧化I- ,但Cu2+氧化了I-的原因,设计实验如下:
编号 | 实验1 | 实验2 | 实验3 |
实验 |
KI溶液 |
KI溶液 AgNO3溶液 a b |
KI溶液 CuSO4溶液 c d |
现象 | 无明显变化 | a中溶液较快变棕黄色,b中电极上析出银;电流计指针偏转 | c中溶液较慢变浅黄色; 电流计指针偏转 |
(电极均为石墨,溶液浓度均为 1 mol/L,b、d中溶液pH≈4)
①a中溶液呈棕黄色的原因是___________________________(用电极反应式表示)。
②“实验3”不能说明Cu2+氧化了I-。依据是空气中的氧气也有氧化作用,设计实验证实了该依据,实验方案及现象是_____________________________。
③方案2中,Cu2+能氧化I-,而Ag+未能氧化I-。其原因一是从K值______;二是从Cu2+的反应特点______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】简单原子的原子结构可用下图形象地表示:
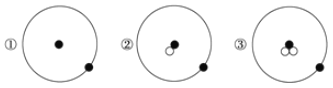
其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是
a.①②③互为同位素 b.①②③互为同素异形体 c.①②③具有相同的质量数
d.①②③是三种化学性质不同的粒子 e.①②③具有相同的质量 f.①②③是三种不同的原子
A. e、fB. b、cC. d、eD. a、f
查看答案和解析>>
科目: 来源: 题型:
【题目】铅精矿可用于冶炼金属铅,其主要成分为PbS。
(1)火法炼铅将铅精矿在空气中焙烧,生成PbO和SO2。
①用铅精矿火法炼铅的反应的化学方程式为____________________________。
②火法炼铅的废气中含低浓度SO2,可将废气通入过量氨水中进行处理,反应的离子方程式为_____________________________________________________。
(2)湿法炼铅在制备金属铅的同时,还可制得硫磺,相对于火法炼铅更为环保。湿法炼铅的工艺流程如下:

已知:PbCl2为能溶于水的弱电解质,在Cl-浓度较大的溶液中,存在平衡:PbCl2(aq) + 2Cl-(aq) ![]() PbCl42-(aq)。不同温度下PbCl2的溶解度如下表所示:
PbCl42-(aq)。不同温度下PbCl2的溶解度如下表所示:
温度(℃) | 20 | 40 | 60 | 80 | 100 |
溶解度(g) | 1.00 | 1.42 | 1.94 | 2.88 | 3.20 |
①浸取液中FeCl3的作用是________________________________。
②操作a为加适量水稀释并冷却,该操作有利于滤液1中PbCl2的析出,分析可能的原因是___________________________________________________________________。
③将溶液3和滤液2分别置于如图所示电解装置的两个极室中,可制取金属铅并使浸取液中的FeCl3再生。

ⅰ.溶液3应置于_________ (填“阴极室”或“阳极室”)中。
ⅱ.简述滤液2电解后再生为FeCl3的原理______________________________________。
ⅲ.若铅精矿的质量为a g,铅浸出率为b ,当电解池中通过c mol电子时,金属铅全部析出,铅精矿中PbS的质量分数为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:
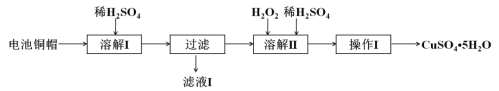
(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是___________、____________。
(2) 从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为__________、__________、过滤、冰水洗涤、低温干燥。
(3)在“溶解II”步骤中,发生反应的离子方程式为____________________________。
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol·L-1Na2S2O3溶液至刚好完全反应,消耗Na2S2O3溶液25.00mL。已知:2Cu2++4I-===2CuI(白色)↓+I2, 2S2O32-+I2===2I-+S4O62- 请依据实验数据计算样品中CuSO4·5H2O的质量分数(写出计算过程)_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用镁和硝基苯制取反式偶氮苯(溶解性:不溶于水,溶于醇、醚)。实验原理如下:
2![]() +4Mg+8CH3OH→
+4Mg+8CH3OH→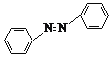 +4Mg(OCH3)2+4H2O
+4Mg(OCH3)2+4H2O
已知:①Mg(OCH3)2在水中极易水解。
②反式偶氮苯产品在紫外线照射后部分转化为顺式偶氮苯。
(1)反应中,硝基苯变为反式偶氮苯的反应属于_______________
A、取代反应 B、消去反应 C、还原反应 D、氧化反应
(2)在反应装置中,加入原料及溶剂,搅拌下加热回流。反应加入的镁条应用砂纸打磨干净的原因是_____________________________________。
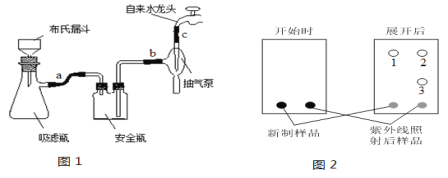
(3)反应结束后将反应液倒入冰水中,用乙酸中和至中性,即有反式偶氮苯粗产品析出,抽滤(抽滤装置如图1),滤渣用95%乙醇水溶液重结晶提纯。
①为了得到较大颗粒的晶体,加入乙酸时需要____________(填“缓慢加入”、“快速加入”)。
②抽滤过程中要洗涤粗产品,下列液体最合适的是___________。
A.乙醚 B.蒸馏水 C.95%乙醇水溶液 D.饱和NaCl溶液
③重结晶操作包括“加热溶解、趁热过滤、冷却结晶、抽滤、洗涤、干燥”。上述重结晶过程中的___________操作除去了不溶性杂质,____________操作除去了可溶性杂质。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)⑦的离子结构示意图是__________;
(2)表中最活泼的金属是________(填写元素符号),能形成的最稳定气态氢化物的化学式是_______;
(3)
(4)⑤、⑧形成化合物中含有的化学键是________(填“离子键”或“共价键”);
(5)1mol④的单质与足量②的氢化物完全反应产生的气体在标准状况下的体积为_____;
(6)写出⑥的单质与④的最高价氧化物的水化物溶液反应的化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】萜类化合物a、b、c广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )
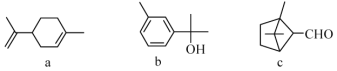
A. b和c互为同分异构体
B. a、b、c分子中所有碳原子不可能处于同一平面上
C. a和c均能使溴的四氯化碳溶液因反应褪色
D. b和c均能与新制的Cu(OH)2反应生成红色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com