
科目: 来源: 题型:
【题目】在2A + B![]() 3C + 4D 反应中(各物质均为气体),表示该反应速率最快的是
3C + 4D 反应中(各物质均为气体),表示该反应速率最快的是
A. v(A)= 0.5 mol·L-1·s-1
B. v(B)= 0.3 mol·L-1·s-1
C. v(C)= 0.8 mol·L-1·s-1
D. v(D)= 30 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的2L密闭容器中,发生反应:X(g)+Y(g)![]() 2Z(g),达到平衡时,各物质的平衡浓度为:c(X)=0.8mol/L;c(Y)=0.1mol/L;c (Z)=1.6mol/L。若用a、b、c分别表示X、Y、Z的起始的物质的量,回答下列问题:
2Z(g),达到平衡时,各物质的平衡浓度为:c(X)=0.8mol/L;c(Y)=0.1mol/L;c (Z)=1.6mol/L。若用a、b、c分别表示X、Y、Z的起始的物质的量,回答下列问题:
(1)若在恒温恒容条件下进行反应X(g)+Y(g)![]() 2Z(g),可判断该反应达到化学平衡状态的是_____
2Z(g),可判断该反应达到化学平衡状态的是_____
A.单位时间内生成n molX的同时生成2nmolZ
B.密闭容器中密度不再改变的状态
C.用X、Y、Z的物质的量浓度变化表示反应速率的比为1∶1∶2的状态
D.反应容器中Y的物质的量分数不再改变的状态
E.密闭容器中压强不再改变的状态
F.混合气体的平均相对分子质量不再改变的状态
(2)a、b应满足的关系是_________。
(3)a的取值范围是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】键能的大小可用于计算化学反应的反应热(△H)。
化学键 | Cl-Cl | H—H | H—Cl | N≡N |
键能/kJ·mol-1 | 243 | 436 | 431 | 946 |
(1)利用上表中的数据判断发生反应H2(g) + Cl2(g)= 2HCl(g)过程中,当生成1molHCl气体时需要___(填“吸收”或“放出” )____kJ能量。
(2)已知N2 (g)+3H2(g) = 2NH3(g) ΔH=-92 kJ/mol,则N—H键的键能是___kJ·mol-1。
(3)1molNO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化如下图,请写出NO2和CO反应的热化学方程式:____。

(4)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1
②2CO(g)+O2(g)=2CO2(g) ΔH2
③H2O(g)=H2O(l) ΔH3
则CH3OH(l)+O2(g)= CO(g) + 2H2O(l) ΔH=_______(用含ΔH1、ΔH2、ΔH3的式子表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关Cl2的说法中,不正确的是
A. Cl2是一种黄绿色的有毒气体 B. 干燥的Cl2可保存在钢瓶中
C. 铁丝在Cl2中燃烧生成FeCl3 D. 氯气和液氯是两种不同的物质
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计实验探究同主族碳、硅两元素的非金属性的强弱,根据要求完成下列问题:
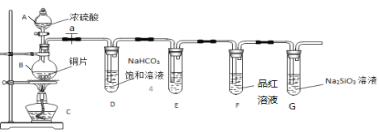
(1)填写所示仪器名称:A _______,B ______。
(2)铜与浓硫酸反应的化学方程式是____________________。
(3)装置E中足量酸性KMnO4溶液的作用是_________________。
(4)能说明碳元素的非金属性比硅元素非金属性强的实验现象是_________。
(5)依据试管D中实验现象,能否证明硫元素的非金属性强于碳元素的非金属性___(填“能”或“否”),试管D中发生反应的离子方程式是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关从海带中提取碘的实验原理和装置能达到实验目的的是

A. 用装置甲灼烧碎海带
B. 用装置乙过滤海带灰的浸泡液
C. 用装置丙制备用于氧化浸泡液中I的Cl2
D. 用装置丁吸收氧化浸泡液中I后的Cl2尾气
查看答案和解析>>
科目: 来源: 题型:
【题目】随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。下列说法正确的是( )
A.H2 和 H3 属于同素异形体B.C60 的摩尔质量为 720 g
C.O2 和 O4 属于同位素D.N5+离子中含有 36 个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com