
科目: 来源: 题型:
【题目】25 ℃,c(HCN)+c(CN) =0.1 mol·L-1的一组HCN和NaCN的混合溶液,溶液中c (HCN)、c(CN-)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是

A. 将0.1 mol·L-1的HCN溶液和0.1 mol·L-1NaCN溶液等体积混合(忽略溶液体积变化):c(CN-)>c(Na+)>c(HCN)>c(OH-)>c(H+)
B. W点表示溶液中:c(Na+) + c(H+) = c(HCN)
C. pH = 8的溶液中:c(Na+) + c(H+) + c(HCN) = 0.1 mol·L-1 + c(OH-)
D. 将0.3 mol·L-1 HCN溶液和0.2 mol·L-1NaOH溶液等体积混合(忽略溶液体积变化):c(CN-) + 3c(OH-) = 2c(HCN)+ 3c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上冶炼铝的原料是铝土矿(主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等),某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量盐酸后过滤出的滤渣中含有____________________,加入过量的NaOH溶液,过滤后的滤液中含有的溶质有_______________________(均填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,则每消耗0.1mol氧气有多少_____mol Fe(OH)2被氧化。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为___________________,沉淀A加热得到Al2O3的化学方程式为____________________。
(4)假设铝土矿中含杂质49%,则1吨铝土矿理论上可生产多少__________mol铝。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,用化学用语回答下列问题:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑧的原子结构示意图为______________________________________________。
(2)③⑧⑩的最高价含氧酸的酸性最强的是__________(填化学式)。
(3)③的气态氢化物与③的最高价氧化物对应的水化物反应生成盐的化学方程式是_______。
(4)①④⑩三种元素的原子能形成原子数目比为1∶1∶1的共价化合物,它的电子式为_____________,②④两种元素形成原子数目比为1∶2的共价化合物的结构式为___________________________。
(5)⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为_________,⑨的最高价氧化物的水化物的浓溶液与铜反应的化学方程式为:____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下:

查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
III.Sn(OH)2的性质与Al(OH)3性质相似。请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,这样操作的原因是____________________。
(2)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子方程式是____________________。
(3)滤液I溶质的成分是____________________。
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是____________________。
(5)称取SnSO4·x H2O晶体50.2g,在隔绝空气的情况下小火加热至结晶水全部失去,冷却称量固体质量为43g,则该晶体的化学式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X是某药物的中间体,其结构简式如图所示。下列有关X的说法正确的是
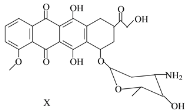
A. 每个X分子中含有5个手性碳原子
B. 一定条件下,X能与乙醇发生酯化反应
C. 一定条件下,X能发生消去反应
D. X既能与盐酸反应,又能与NaOH溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】由铁、锌、镁、铝四种金属中的两种组成的10g混合物与足量的盐酸反应,反应后生成的氢气在标准状况下体积为11.2L.则混合物中一定含有的金属是( )
A.锌B.铁C.镁D.铝
查看答案和解析>>
科目: 来源: 题型:
【题目】已知电导率越大导电能力越强。常温下用0.100 mol·L-1NaOH溶液分别滴定10.00mL浓度均为0.100 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线①代表滴定盐酸的曲线
B. a点溶液中: c(OH-)+c(CH3COO-)-c(H+) =0.1 mol/L
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
科目: 来源: 题型:
【题目】选择下列化学用语,用序号完成下列问题①O2②Na2O2③18O④CH3—CH2—CH2—CH2—CH3⑤O2-⑥CaCl2 ⑦O3 ⑧16O ⑨NH4Cl ⑩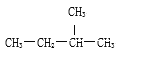
(1)只含共价键的是___________________。
(2)既含共价键又含离子键的是___________________。
(3)属于离子晶体的是______________,属于共价化合物的是_________________。
(4)互为同素异形体的是______,互为同分异构体的是______,互为同位素的是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com