
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮяжЪЕФСПЯрЭЌЕФ Mg2+ЁЂF-ЁЂH2O Ш§жжЮЂСЃЃЌвЛЖЈКЌгаЯрЭЌЕФЃЈ ЃЉ
A.ЕчзгЪ§B.жЪзгЪ§C.жазгЪ§D.жЪСПЪ§
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЬМЫсЧтФЦЙуЗКЕигІгУгкЩњВњЁЂЪЕбщКЭШеГЃЩњЛюжаЁЃФГПЮЭтаЁзщЭЌбЇЭЈЙ§ВщдФзЪСЯЖдЬМЫсЧтФЦЕФаджЪКЭжЦЗЈНјааСЫЯЕСаЪЕбщЃЌЧыФуВЮгыЬНОПЁЃ
ЃЈ1ЃЉЯђNaHCO3ШмвКЕЮМгMnCl2ШмвКЩњГЩГСЕэMnCO3ЃЌРызгЗНГЬЪНЮЊ______ЁЃ
ЃЈ2ЃЉЯђNaHCO3ШмвКМгШыЩйСПЕФУОЗлЃЌЙлВьЕНгаЦјЬхКЭАзЩЋГСЕэЩњГЩЃЌдђИУЦјЬхвЛЖЈЪЧ______ЃЈЬюЛЏбЇЪНЃЉЃЌАзЩЋГСЕэПЩФмЪЧЃКЂйMgCO3ЃЛЂкMg(OH)2ЃЛЂлMg2(OH)2CO3ЁЃгћжЄУїАзЩЋГСЕэЮЊЂкЃЌМђЕЅЕФЪЕбщЗНЗЈЮЊ______ЃЈВйзїЁЂЯжЯѓКЭНсТлЃЉЁЃ
ЃЈ3ЃЉЕчНтNa2CO3ШмвКжЦNaHCO3ЕФдРэШчЭМЁЊ1ЫљЪОЃЎ
ЂйЕчНтГѕЦкЃЌЕчНтГижазмЗДгІЗНГЬЪНЮЊ______ЁЃ
ЂкШєЕчНтЙ§ГЬжаЭИЙ§НЛЛЛФЄЕФNa+ЮЊ 0.4 molЃЌдђбєМЋЪеМЏЕН O2_____LЃЈБъПіЃЉЁЃ
ЂлЕчНтКѓЦкШмвКжаЕФКЌЬМЮЂСЃж№НЅМѕЩйЃЌДЫНзЖЮбєМЋЗДгІЪНЮЊ______ЁЃ
ЃЈ4ЃЉ ЁАКюЪЯжЦМюЗЈЁБЕФдРэЪЧЃК NaCl+NH3+ CO2+H2O= NaHCO3+NH4ClЃЌФЃФтИУжЦЗЈЕФВПЗжзАжУШчЭМЁЊ2ЫљЪОЃЎ
Ђй е§ШЗЕФВйзїЪЧ______ЃЈЬюађКХЃЉЁЃ
AЃЎaЭЈШыCO2ЃЌШЛКѓbЭЈШыNH3ЃЌcжаЗХМюЪЏЛв
BЃЎaЭЈШыNH3ЃЌШЛКѓbЭЈШыCO2ЃЌcжаЗХеКЯЁСђЫсЕФЭбжЌУо
CЃЎbЭЈШыNH3ЃЌШЛКѓaЭЈШыCO2ЃЌcжаЗХМюЪЏЛв
DЃЎbЭЈШыCO2ЃЌШЛКѓaЭЈШыNH3ЃЌcжаЗХеКЯЁСђЫсЕФЭбжЌУо
Ђк ЫЎВлжаЕФРфЫЎЦ№НЕЮТзїгУЃЌетбљгаРћгк______ЁЃ

ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкбѕЛЏТСКЭЧтбѕЛЏТСЕФа№ЪіДэЮѓЕФЪЧЃЈ ЃЉ
A. Al(OH)3ЪмШШФмЗжНт
B. Al2O3МШФмШмгкЧПЫсШмвКгжФмШмгкЧПМюШмвК
C. Al(OH)3НКЬхФмЮќИНЫЎжаЕФаќИЁЮя
D. Al(OH)3гыЙ§СПЕФХЈАБЫЎЗДгІЩњГЩNH4[Al(OH)4]
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЪЧЪЕбщЪвжЦШЁSO2ВЂбщжЄSO2ЕФФГаЉаджЪЕФзАжУЃЌЪдЛиД№

ЪдЛиД№ЃК
ЃЈ1ЃЉЂкжаЕФЪЕбщЯжЯѓЮЊ______________ЁЃ
ЃЈ2ЃЉЂмжаЕФЪЕбщЯжЯѓЮЊ______________ЃЌДЫЪЕбщЫЕУїSO2га____________адЃЎ
ЃЈ3ЃЉЂнжаЕФЪЕбщЯжЯѓЮЊ____________ЃЌДЫЪЕбщЫЕУїSO2га________адЃЎ
ЃЈ4ЃЉЂоЕФзїгУЪЧ___________ЃЌЗДгІЗНГЬЪНЪЧ_____________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈжае§ШЗЕФЪЧ![]() ЁЁЁЁ
ЁЁЁЁ![]()
![]() дгЛЏЙьЕРЪЧгЩЭЌвЛИідзгжаФмСПзюНќЕФsЙьЕРКЭpЙьЕРЛьКЯЦ№РДаЮГЩЕФвЛзщФмСПЯрЭЌЕФаТЙьЕР
дгЛЏЙьЕРЪЧгЩЭЌвЛИідзгжаФмСПзюНќЕФsЙьЕРКЭpЙьЕРЛьКЯЦ№РДаЮГЩЕФвЛзщФмСПЯрЭЌЕФаТЙьЕР
![]() ЭЌвЛжмЦкДгзѓЕНгвЃЌдЊЫиЕФЕквЛЕчРыФмЁЂЕчИКадЖМЪЧдНРДдНДѓ
ЭЌвЛжмЦкДгзѓЕНгвЃЌдЊЫиЕФЕквЛЕчРыФмЁЂЕчИКадЖМЪЧдНРДдНДѓ
![]() ЗжзгжаМќФмдНДѓЃЌБэЪОЗжзггЕгаЕФФмСПдНИп
ЗжзгжаМќФмдНДѓЃЌБэЪОЗжзггЕгаЕФФмСПдНИп
![]() ЫљгаЕФХфКЯЮяЖМДцдкХфЮЛМќ
ЫљгаЕФХфКЯЮяЖМДцдкХфЮЛМќ
![]() ЫљгаКЌМЋадМќЕФЗжзгЖМЪЧМЋадЗжзг
ЫљгаКЌМЋадМќЕФЗжзгЖМЪЧМЋадЗжзг
![]() ШлШкзДЬЌЯТФмЕМЕчЕФЛЏКЯЮявЛЖЈЪЧРызгЛЏКЯЮя
ШлШкзДЬЌЯТФмЕМЕчЕФЛЏКЯЮявЛЖЈЪЧРызгЛЏКЯЮя
![]() ЫљгаЕФдзгОЇЬхЖМВЛЕМЕч
ЫљгаЕФдзгОЇЬхЖМВЛЕМЕч
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИљОнвЊЧѓЭъГЩЯТСаЮЪЬт
ЃЈ1ЃЉЕЅжЪТСКЭЧтбѕЛЏФЦШмвКЗДгІЕФЛЏбЇЗНГЬЪН_________________ЃЌБОЗДгІжаЕФбѕЛЏМСЪЧ_______ЁЃ
ЃЈ2ЃЉЪЕбщЪвгУЖўбѕЛЏУЬКЭХЈбЮЫсжЦШЁТШЦјЕФРызгЗНГЬЪН_____________________ЁЃБОЗДгІжаЕФбѕЛЏМСКЭЛЙдМСЕФЮяжЪЕФСПБШЮЊ_____________________ЁЃ
ЃЈ3ЃЉЖўбѕЛЏСђКЭТШЦјАДЕШЮяжЪЕФСПЭЈШызуСПЫЎжаЕФЛЏбЇЗНГЬЪН_______________ЃЌБОЗДгІжаШєга1molбѕЛЏМСВЮМгЗДгІдђзЊвЦЕчзгЪ§ФПЮЊ_____________________ЁЃ
ЃЈ4ЃЉХЈЯѕЫсвЛАуЯдЛЦЩЋЃЌгУЗНГЬЪННтЪЭдвђЃК______________ЃЌПЩЯђХЈЯѕЫсжаЭЈШы_______ЯћГ§ЛЦЩЋЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗлУКЛвЃЈжївЊКЌга SiO2ЁЂFe2O3ЁЂAl2O3 ЕШЃЉЪЧШМУКЗЂЕчЙ§ГЬжаВњЩњЕФЗЯдќЃЌЗлУКЛвЕФзлКЯРћгУОпга КмДѓЕФМлжЕЁЃ
ЂёЃЎбаОПШЫдБЭЈЙ§ЪЕбщЖдЗлУКЛвжаТСКЭЬњдЊЫиЕФЗжРыЙЄвеНјааСЫбаОПЁЃ
ЃЈ1ЃЉвдСђЫсШмвКЗжНтЗлУКЛвЃЌЪЙЦфжаЕФТСЁЂЬњдЊЫиШмГіЃЌЙ§ТЫЪЕЯжГѕВНЗжРыЁЃ
ЂйаДГіСђЫсШмвКгы Fe2O3 ЗДгІЕФРызгЗНГЬЪН_____ЁЃ
ЂкГѕВНЗжРыЕУЕНЕФТЫдќжївЊГЩЗжЪЧ_____ЁЃ
ЃЈ2ЃЉЯђЃЈ1ЃЉЗжРыЫљЕУЕФТЫвКжаМгШыЛЙдМСЪЙ Fe3+зЊЛЏЮЊ Fe2+ЃЌНсКЯЯТБэЗжЮіЦфдвђ____ЁЃ
ЮяжЪ | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
ГСЕэЧјМфЃЈpHЃЉ | 7.06~8.95 | 1.94~3.20 | 3.69~4.8 |
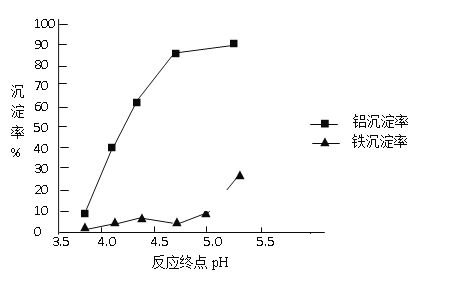
ЃЈ3ЃЉЪЙгУМюадНЯШѕЕФАБЫЎЮЊpHЕїНкМСЃЌНјааЗжРыЪЕбщЁЃ
ЂйАБЫЎЪЙТЫвКжаТСРызгГСЕэЕФРызгЗНГЬЪНЮЊ_____ЁЃ
ЂкЗДгІжеЕуЕФpHЖдТСКЭЬњЗжРыаЇЙћЕФгАЯьШчЯТЭМЁЃИљОнЪЕбщНсЙћЃЌЮЊДяЕНКУЕФЗжРыаЇЙћЃЌЗДгІЙ§ГЬжаПижЦpHЕФ ЗЖЮЇЪЧ______________ЃЌбЁдёИУЗЖЮЇЕФРэгЩЪЧ___________________ЁЃ
ЂђЃЎNH4HSO4КЭH2SO4АДЮяжЪЕФСПБШ1ЁУ1ЛьКЯХфжЦГЩНўШЁвКЃЌ220ЁцЪБЃЌПЩНЋИпТСЗлУКЛвжаAl2O3зЊЛЏЮЊСђЫсТСяЇ [NH4Al(SO4)2]ЃЌШЛКѓЗжРыЁЂьбЩеЛёЕУДПAl2O3ЁЃ вбжЊСђЫсТСяЇЃКЂйШмНтЖШЃК0ЁцЪБЃЌSЃН5.2gЃЛ100ЁцЪБЃЌSЃН421.9gЁЃЂк280ЁцЪБЗжНтЁЃ
ЃЈ1ЃЉвРОнзЪСЯПЩжЊЃЌНЋСђЫсТСяЇгыЦфЫћШмжЪЗжРыЕФЗНЗЈЪЧ_____ЁЃ
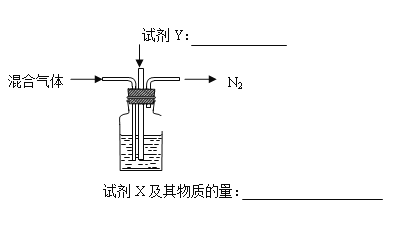
ЃЈ2ЃЉьбЩе NH4Al(SO4)2 ЭЌЪБЕУЕНЛьКЯЦјЬхЃЈNH3ЁЂN2ЁЂSO2ЁЂSO3ЁЂH2OЃЉЁЃШє 16 mol ЛьКЯЦјЬхАДШчЯТзАжУБЛЭъШЋЮќЪежЦЕУНўШЁвКЃЌЧыНЋЯТЭМжаЪдМСЃЈЛЏбЇЪНЃЉМАЦфЮяжЪЕФСПВЙГфЭъећЁЃ____________ЃЌ___________
4NH4AlЃЈSO4ЃЉ2 ![]() 2Al2O3+5SO3Ёќ+3SO2Ёќ+2NH3Ёќ+N2Ёќ+5H2OЁќ
2Al2O3+5SO3Ёќ+3SO2Ёќ+2NH3Ёќ+N2Ёќ+5H2OЁќ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙигкдЊЫижмЦкБэЕФЫЕЗЈе§ШЗЕФЪЧ
A.дЊЫижмЦкБэжага8ИіжїзхB.дЊЫижмЦкБэжага7ИіжмЦк
C.жмЦкБэжаЕФжїзхЖМгаН№ЪєдЊЫиD.IAзхжаЕФдЊЫиШЋВПЪЧН№ЪєдЊЫи
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙигкЩњЮяЬхФкдЊЫиЕФа№ЪіЃЌе§ШЗЕФЪЧЃЈ ЃЉ

A. ИїжждЊЫидкЯИАћгыЗЧЩњЮяНчЕФКЌСПВювьВЛДѓ
B. ЯИАћФкКЌСПзюЖрЕФдЊЫиЪЧC,вђДЫCЪЧЩњУќЕФКЫаФдЊЫи
C. ЯИАћФкКЌгаFeЁЂCuЁЂMnЁЂZnЁЂBЁЂMoЕШзїгУВЛживЊЕФЮЂСПдЊЫи
D. КцИЩЕФжВЮяЯИАћжаКЌСПзюЖрЕФдЊЫиЪЧC
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЧтЛЏТСяЎ(LiAlH4)ЪЧгаЛњКЯГЩжаЕФживЊЛЙдМСЁЃФГПЮЬтзщЩшМЦЪЕбщжЦБИЧтЛЏТСяЎВЂВтЖЈЦфДПЖШЁЃвбжЊЃКЧтЛЏТСяЎЁЂЧтЛЏяЎгіЫЎЖМОчСвЗДгІВЂВњЩњЭЌвЛжжЦјЬхЁЃЛюЦУН№ЪєСђЛЏЮягыЫсЗДгІВњЩњH2SЦјЬхЁЃ
ЂёЁЂжЦБИЧтЛЏяЎЃКбЁдёЯТЭМжаЕФзАжУжЦБИЧтЛЏяЎ(гааЉзАжУПЩжиИДЪЙгУ)ЃК
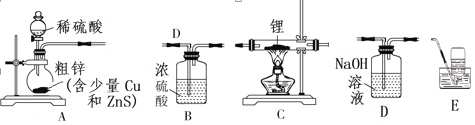
ЃЈ1ЃЉзАжУЕФСЌНгЫГађ(ДгзѓжСгв)ЮЊAЁњ___________________________________ЁЃ
ЃЈ2ЃЉМьВщКУзАжУЕФЦјУмадЃЌДђПЊзАжУAжаЗжвКТЉЖЗЕФЛюШћКѓЃЌЕуШМОЦОЋЕЦЧАашНјааЕФЪЕбщВйзїЪЧ________ЁЃ
ЂђЁЂжЦБИЧтЛЏТСяЎ
1947ФъЃЌSchlesingerЁЂBondКЭFinholtЪзДЮжЦЕУЧтЛЏТСяЎЃЌЦфЗНЗЈЪЧЪЙЧтЛЏяЎгыЮоЫЎШ§ТШЛЏТСАДвЛЖЈБШР§дкввУбжаЛьКЯЃЌНСАшЃЌГфЗжЗДгІКѓЃЌОвЛЯЕСаВйзїЕУЕНLiAlH4ОЇЬхЁЃ
ЃЈ3ЃЉаДГіЧтЛЏяЎгыЮоЫЎШ§ТШЛЏТСЗДгІЕФЛЏбЇЗНГЬЪН_________________________ЁЃ
Ђѓ.ВтЖЈЧтЛЏТСяЎВњЦЗ(ВЛКЌЧтЛЏяЎ)ЕФДПЖШ
ЃЈ4ЃЉАДЯТЭМСЌНгКУзАжУКѓЃЌМьВщзАжУЦјУмадЕФВйзїЪЧЃК_____________________ЁЃзАКУвЉЦЗ(YаЮЙмжаЕФеєСѓЫЎзуСПЃЌЮЊСЫБмУтЧтЛЏТСяЎгіЫЎЗЂЩњБЌеЈЃЌеєСѓЫЎжаашВєШыЫФЧтпЛрЋзїЯЁЪЭМС)ЃЌЦєЖЏЗДгІЕФВйзїЪЧ__________________ЁЃ
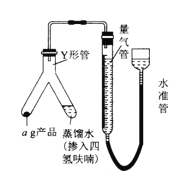
ЃЈ5ЃЉдкБъзМзДПіЯТЃЌЗДгІЧАСПЦјЙм(гЩМюЪНЕЮЖЈЙмИФзАЖјГЩ)ЖСЪ§ЮЊV1 mLЃЌЗДгІЭъБЯВЂРфШДжЎКѓЃЌСПЦјЙмЖСЪ§ЮЊV2 mLЁЃИУбљЦЗЕФДПЖШЮЊ_________(гУКЌaЁЂV1ЁЂV2ЕФДњЪ§ЪНБэЪО)ЁЃШчЙћЦ№ЪМЖСЪ§ЪБИЉЪгПЬЖШЯпЃЌВтЕУЕФНсЙћНЋ_________(ЬюЁАЦЋИпЁБЁАЦЋЕЭЁБЛђЁАЮогАЯьЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com