
科目: 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如图:根据要求填空:
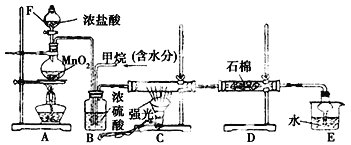
(1)实验室制取Cl2的化学方程式为:____________________。
(2)写出CH4与Cl2生成一氯代物的化学方程式____________________。
(3)B装置有三种功能:①控制气体流速;②将气体混合均匀;③________。
(4)D装置中的石棉上吸附着KI饱和溶液及KI粉末,其作用是________________________。
(5)E装置的作用是________。
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(6)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法为__________。
(7)该装置还有缺陷,原因是没有进行尾气处理,尾气的主要成分是(双选,填编号)________。
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
查看答案和解析>>
科目: 来源: 题型:
【题目】无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如下:

已知:AlCl3、FeCl3分别在183 ℃、315 ℃时升华
(1)铝原子的结构示意图为________,实验室配制氯化铝溶液时加入盐酸的目的是________________________。
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为______________________炉气中残余有少量Cl2,请画出吸收Cl2的尾气装置图_____。

(3)700 ℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围________________。
a.低于183 ℃ b.介于183 ℃和315 ℃之间 c.高于315 ℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
m克样品![]() NaAlO2溶液
NaAlO2溶液![]() Al(OH)3
Al(OH)3![]() n克Al2O3
n克Al2O3
NaAlO2溶液与过量二氧化碳反应的离子方程式为:______________________。计算该样品中Al的质量分数________(结果用m、n表示,不必化简)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物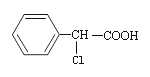 有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )
A. 6种 B. 9种 C. 15种 D. 19种
查看答案和解析>>
科目: 来源: 题型:
【题目】一种化学名为 2,4,4—三氯—2— 羟基—二苯醚的物质(如下图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用。则下列有关说法中正确的是 ( )

A. 该物质与 FeCl3溶液混合后不显色
B. 该物质中所有原子一定处于同一平面
C. 该物质苯环上的一溴取代物有 6 种
D. 物质的分子式为 C12H6Cl3O2
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬烯(柠檬烯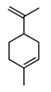 )。提取柠檬烯的实验操作步骤如下:
)。提取柠檬烯的实验操作步骤如下:
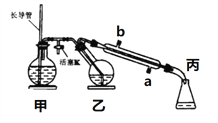
(1)将1~2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30 mL水
(2)松开活塞K。加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧,打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。
下列说法不正确的是( )
A. 当馏出液无明显油珠,澄清透明时,说明蒸馏完成
B. 蒸馏结束后,为防止倒吸,立即停止加热
C. 长玻管作安全管,平衡气压,防止由于导管堵塞引起爆炸
D. 要得到纯精油,还需要用到以下分离提纯方法:萃取、分液、蒸馏
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学反应速率的说法中,正确的是( )
A. 反应C(s)+H2O(g)![]() CO(g)+H2(g),增加碳的用量可加快反应速率
CO(g)+H2(g),增加碳的用量可加快反应速率
B. 用铁片与稀硫酸反应制H2,改用98%的浓硫酸可加快生成H2的速率
C. 用锌片与稀盐酸反应,加入适量的NaCl溶液,反应速率不变
D. 反应2SO2(s)+O2(g)![]() 2SO3(g)在密闭容器中进行,压缩容器体积,反应速率增大
2SO3(g)在密闭容器中进行,压缩容器体积,反应速率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】电池有广泛的用途。
Ⅰ.依据氧化还原反应:Cu+2Ag+===Cu2++2Ag设计的原电池如图所示。请回答下列问题:
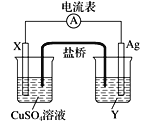
(1)电极X的材料是________________,电解质溶液Y是____________。
(2)银电极的电极反应式是______________________________。
(3)外电路中的电子是从_____极流向_____极。(填“正”或“负”)
(4)该原电池的正极是____________,还可以选用__________________等材料。
Ⅱ.铅蓄电池是化学电源,它工作时的电池总反应为:PbO2+Pb+2H2SO4===2PbSO4+2H2O。试回答:
(5)蓄电池负极的电极材料是_____________________(填“PbO2”或“Pb”)。
(6)工作时该蓄电池正极的电极反应式是___________。
(7)铅蓄电池工作时,电解质溶液的密度________(填“增大”、“减小”或“不变”),负极质量____ (填“增大”、“减小”或“不变”)。
Ⅲ.某研究性学习小组根据反应2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
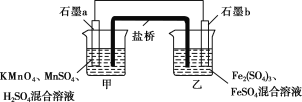
回答下列问题:
(8)此原电池的正极是石墨________(填“a”或“b”),发生________反应。
(9)电池工作时,盐桥中的SO![]() 移向________(填“甲”或“乙”)烧杯。
移向________(填“甲”或“乙”)烧杯。
(10)甲烧杯中的电极反应式为________________________________。
(11)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学反应表达正确的是 ( )
A. 1—丙醇与浓氢溴酸反应:CH3CH2CH2OH + HBr ![]() CH3CH2CH2Br + H2O
CH3CH2CH2Br + H2O
B. 硬脂酸与乙醇的酯化反应:C17H35COOH + C2H518OH ![]() C17H35COOC2H5 + H218O
C17H35COOC2H5 + H218O
C. 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH + OH— ![]() CH2BrCOO— + H2O
CH2BrCOO— + H2O
D. 向丙氨酸钠中加入足量盐酸: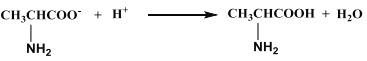
查看答案和解析>>
科目: 来源: 题型:
【题目】关于下图所示的原电池,下列说法正确的是( )
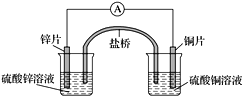
A. 电子从锌电极通过电流表流向铜电极
B. 盐桥中的阴离子向硫酸铜溶液中迁移
C. 铜电极发生还原反应,其电极反应是2H++2e-===H2↑
D. 取出盐桥后,电流表仍会偏转,铜电极在反应前后质量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com