
科目: 来源: 题型:
【题目】在2L密闭容器内,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
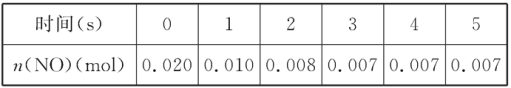
(1)上述反应____(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为________。
(2)如图中表示NO2变化曲线的是____。用O2表示从0s~2s内该反应的平均速率v=_______。
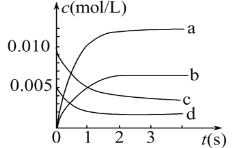
(3)能说明该反应已达到平衡状态的是_______。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v[(NO)逆]=2v[(O2)正] d.容器内密度保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于药物的使用说法正确的是
A.阿司匹林是一种治感冒药,具有解热镇痛作用
B.使用青霉素时,不用进行皮试可直接静脉注射
C.服用阿司匹林出现胃肠道反应是中毒的表现,应立即停药并静脉注射NaHCO3溶液
D.胃酸过多的病人都可以服用氢氧化钠、氢氧化铝、碳酸钠等中和胃酸的药
查看答案和解析>>
科目: 来源: 题型:
【题目】NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H=?
2N2(g) +6H2O(g) △H=?
(1)
化学键 | H—O | O===O | N≡N | N—H |
键能kJ·molˉ1 | a | b | c | d |
△H=__________________ 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是__________________。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内n(NO)/n(NH3)=1时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:
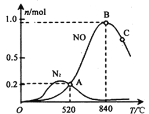
①该催化剂在高温时选择反应____________ (填“ I ”或“ II”)。
②520℃时,4NH3(g)+5O2![]() 4NO(g) +6H2O(g)的平衡常数K=___________________ (不要求得出计算结果,只需列出数字计算式)。
4NO(g) +6H2O(g)的平衡常数K=___________________ (不要求得出计算结果,只需列出数字计算式)。
③有利于提高NH3转化为N2平衡转化率的措施有_______________
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
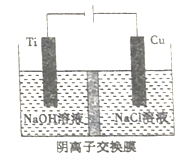
(4)纳米级Cu2O 由于具有优良的催化性能而受到关注,工业上常用电解法Cu2O,其反应为2Cu+H2O![]() Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为___________________,当生成_______克Cu2O时,就会有NA个阴离子通过离子交换膜。
Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为___________________,当生成_______克Cu2O时,就会有NA个阴离子通过离子交换膜。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料,某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
(方案1)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
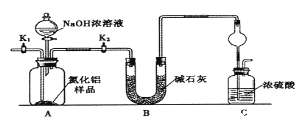
(1)如图C装置中球形干燥管的作用是______________。
(2)完成以下实验步骤:组装好实验装置,首先______;再加入实验药品。接下来的实验操作是____,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是______________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见_________。
(方案2)用如下图装置测定m g样品中A1N的纯度(部分夹持装置已略去)。
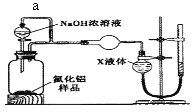
(4)导管a的主要作用是______________。
(5)为测定生成气体的体积,量气装置中的X液体可以是____________。(填选项序号)
a.CCl4 b.H2O c.NH4Cl溶液 d.![]()
(6)若mg样品完全反应,测得生成气体的体积为VmL,(已转换为标准状况),则A1N的质量分数为___(用含V、m的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
【制备FeBr2固体】
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将干燥、纯净的CO2气流通入D中,再将铁粉加热至600—700℃,E管中铁粉开始反应。不断将d中液溴滴入温度为100—120℃的D中,经过一段时间的连续反应,在不锈钢管内产生黄绿色鳞片状溴化亚铁。

(1)若在A中盛固体CaCO3,a中盛有6 mol/L的盐酸。为使导入D中的CO2为干燥纯净的气体,则图中B、C处的洗气瓶中装有的试剂分别是:B中为____________,C中为_________________。
若进入E装置中的CO2未干燥,则可能发生的副反应的化学方程式为_____________________。
(2)E管中的反应开始前通入CO2的主要作用是__________________________________;
E管中的反应开后持续通入CO2的主要作用是______________________________________。
【探究FeBr2的还原性】
(3)现实验需要90 mL 0.1 mol/L FeBr2溶液,取上述反应制得的FeBr2固体配制该溶液,所需仪器除烧杯、量筒、玻璃棒外,还需要的玻璃仪器是_______________________________。
(4)已知:Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色。Cl2既能氧化Br-,也能氧化Fe2+。
取10 mL上述FeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为血红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。
以上实验结论表明还原性:Fe2+__________Br-(填“>”或“<”)。
(5)若在40 mL上述FeBr2溶液中通入标准状况下67.2 mL的 C12,取少量反应后的溶液加入CCl4,振荡后下层液体呈______色,写出该反应的离子方程式________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】储氢材料是当前新能源领域研究的一类热门材料。在一定条件下,以Cu-Zn原电池作电源,利用图所示装置可实现有机物的储氢,下列有关说法正确的是( )
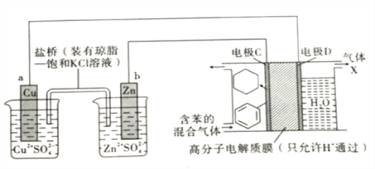
A.在Cu-Zn原电池装置工作时,盐桥内的Cl-向铜电极一端移动
B.电极C为阳极,在电极D上发生还原反应
C.气体X的主要成分是H2
D.H+透过高分子膜从右室进入左室,在电极C上发生还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在实验室中发现了一瓶无色、有刺激性气味的气体,根据气味判断可能是氨气,但不能确定一定是氨气。下列提供的方法中,你认为能够帮他检验是否为氨气的是
A. 将湿润的红色石蕊试纸放在打开的瓶口
B. 将湿润的蓝色石蕊试纸放在打开的瓶口
C. 用蘸有浓硫酸的玻璃棒靠近打开的瓶口
D. 用干燥的红色石蕊试纸放在打开的瓶口
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

(1)MgCO3 与稀硫酸反应的化学方程式为__________________________。
(2)加入H2O2 氧化时,发生反应的离子方程式为__________________________。
(3)滤渣2 的成分是____________(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C![]() 2MgO+2SO2↑+CO2↑ MgSO4+C
2MgO+2SO2↑+CO2↑ MgSO4+C![]() MgO+SO2↑+CO↑ MgSO4+3C
MgO+SO2↑+CO↑ MgSO4+3C![]() MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。

①D中通过排水法收集的气体可以是___________(填化学式)。
②C中溶液用于吸收CO2,B中盛放的溶液可以是___________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com