
科目: 来源: 题型:
【题目】H2S是严重危害环境的气体,采取多种方法减少H2S的排放并加以资源利用。
(1) 用Fe2(SO4)3吸收H2S。在配制硫酸铁溶液时需要向溶液中加入一定量的硫酸,其目的是:________________。吸收时发生反应的离子方程式为_____________________。反应后的溶液在硫杆菌作用下进行再生,反应为:4FeSO4+O2+2H2SO4==2Fe2(SO4)3+2H2O。
图1、图2为再生时Fe2+的转化速率与反应条件的关系。再生的最佳条件为_______________。若反应温度过高,反应速率下降,其原因是_____________________。

(2) 在一定条件下,用H2O2氧化H2S。
随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的化学式为________________。
(3) H2S与CO2在高温下反应可生成氧硫化碳(COS),其结构式为________________。
(4)加热条件下用O2氧化H2S,使硫元素转化为硫单质并回收,写出氧气氧化硫化氢的反应方程式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.据报道,日常生活中,将洁厕液与84消毒液混合使用会发生中毒的事故。
(1)84消毒液的主要成分是次氯酸钠,次氯酸钠与空气中CO2反应生成次氯酸,写出次氯酸钠的电子式:__________;若将84消毒液长期露置于空气中,溶液中的主要成分将变为__________(填化学式)。
(2)洁厕灵的主要成分是HCl。洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式:______________________________。
(3)下列氧化还原反应中,与上述反应类型不同的是________。
A.Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O B.2FeCl3+Fe===3FeCl2
C.S+2H2SO4(浓)![]() 3SO2↑+2H2O D.KClO3+5KCl+3H2SO4===3K2SO4+3Cl2↑+3H2O
3SO2↑+2H2O D.KClO3+5KCl+3H2SO4===3K2SO4+3Cl2↑+3H2O
II.已知高锰酸钾(硫酸酸化)溶液和草酸(H2C2O4)溶液可以发生氧化还原反应。请回答下列问题:
(1)该反应中的还原剂是________(填化学式)。
(2)写出该反应的离子方程式:____________________________________________。
(3)若生成1molCO2则转移电子_______mol
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下反应A(g)+B(g)C(g)△H<0达到平衡后,据下列图象判断:

达到新的平衡对应的图象 (填写字母) | 平衡移动方向 (正反应、逆反应,不移动) | |
(i)使用催化剂 | _________ | ________ |
(ii)升温 | _________ | _________ |
(iii)降压 | _________ | _________ |
(iv)增加A的量 | __________ | _________ |
(v)减少C的量 | __________ | ________ |
查看答案和解析>>
科目: 来源: 题型:
【题目】某不饱和烃与氢气加成后的产物为 ,请按要求回答下列问题:
,请按要求回答下列问题:
(1)请用系统命名法对该物质进行命名:_________________________。
(2)若该不饱和烃为炔烃,则该炔烃的结构简式为___________________________。
(3)若该不饱和烃为一单烯烃,则可能有________种结构,结构简式分别为__________。
(4)由(2)中炔烃的最简单同系物可以合成聚氯乙烯塑料。试写出该过程中的化学方程式,并注明反应类型:
①______________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2OH++OH-△H>0,下列叙述正确的是( )
A. 向平衡体系中加入水,平衡正向移动,c (H+)增大
B. 将水加热,Kw增大,pH不变
C. 向水中加入少量硫酸氢钠固体, 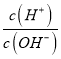 增大
增大
D. 向水中加入少量NaOH固体,平衡正向移动,c(H+)降低
查看答案和解析>>
科目: 来源: 题型:
【题目】0.10mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆向移动
B. 加入少量NaOH固体,平衡向正向移动
C. 加入少量0.10mol/LHCl溶液,溶液中C(H+)减少
D. 加入少量CH3COONa固体,平衡向正向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】
半导体材料磷化硼(BP)可由BBr3和PBr3在高温下合成。回答下列问题:
(1)基态P原子的价电子排布式为__________,同周期中第一电离能比P 小的元素有______种。
(2)在水中的溶解度BBr3_______PBr3(填“ >”或“ <”),原因是_____________。
(3)一定温度下PBr5能形成阴、阳离子个数比为1:1的导电熔体,经测定其中P—Br键键长均相等。写出该导电熔体中阳离子的电子式:_________,其中P原子的杂化轨道类型是_______。
(4)已知磷化硼晶体中P原子作A1型最密堆积,B原子填入四面体空隙中,相邻P原子和B原子核间距为d cm,则该晶体中每个B原子周围有_____个B原子与它距离最近,晶体密度为____g·cm-3(NA表示阿伏加德罗常数的值),若某个P原子的坐标为(0,0,0),则晶胞中其余P原子的坐标为__________(写出一个即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】将4molA气体和2molB气体在2 L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g) ![]() 2C(g)。若经2 s后测得C的浓度为0.6mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1 ;
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1;
③2s时物质A的转化率为30% ;
④2s时物质B的浓度为1.4mol·L-1。
其中正确的是( )
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH4+完全转化为N2,该反应可表示为2NH![]() +3ClO-===N2↑+3Cl-+2H++3H2O。下列说法中不正确
+3ClO-===N2↑+3Cl-+2H++3H2O。下列说法中不正确
A. 反应中氮元素被氧化,氯元素被还原
B. 还原性:NH4+>Cl-
C. 反应中每生成1 mol N2,转移6 mol电子
D. 经此法处理过的废水可以直接排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com