
科目: 来源: 题型:
【题目】(1)在NaCl溶液中滴加AgNO3溶液,现象为_____________________________ , 离子方程式为:_________________________________________________
(2)在CH3CH2CH2Cl中滴加AgNO3溶液,现象为_____________________________,原因是__________________________
(3)若先将CH3CH2CH2Cl与NaOH溶液共热,然后用硝酸酸化,再滴加AgNO3溶液,现象为_______________________________________________________,反应的化学方程式为:________________________,______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】三峡工程是目前世界上最大的水利枢纽,它所提供的清洁、廉价、再生的水电,相当于每年燃烧5 000万吨原煤的火力发电厂产生的电能,因此三峡工程的建成和使用有助于控制( )。
①氮氧化物的排放 ②酸雨的形成 ③臭氧层空洞扩大
④温室效应 ⑤白色污染
A.①②B.②④C.③④D.①②⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)普鲁士蓝的化学式为Fe4[Fe(CN)6]3,该物质中存在的化学键有离子键、_______和_______;含有的Fe3+的核外电子样布式为_______________。
(2)KCN 可被H2O2 氧化为KOCN
①KOCN 可作为制药原料,其晶体类型是__________;碳原子采取sp杂化,1mol该物质中含有的π键数目为___________。含有的三种非金属元素的电负性由大到小的顺序是________。(2)H2O2常温下是液体,沸点较高(150℃),其主要原因是____________。
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下左图,As 原子的杂化方式为____,雌黄和SnCl2 在盐酸中反应转化为雌黄(As4S4) 和SnCl4,SnCl4 分子的空间构型为_______。
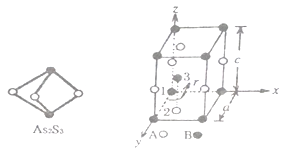
(4)某晶体的晶胞结构如上右图所示,该晶体的化学式为______________,该晶胞参数分别为apm,cpm,γ=120°如图示;1号原子坐标为(0,0,0),2 号原子坐标为(1/3,2/3,0),则3号原子坐标为____________,计算上述晶体中A和B 两原子间的最小核间距为________pm。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列推断正确的是
A. SiO2是酸性氧化物,能与NaOH溶液反应
B. Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C. CO、NO、NO2都是大气污染物气体,在空气中都能温室存在
D. 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液显红色
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年冬季全国大部分地区出现雾霾现象,汽车尾气是造成雾霾的原因之一,汽车尾气含CO、NO等有毒气体。为了减少CO 对大气的污染,某研究性学习小组拟研究CO和H2O 反应转化为绿色能源H2。己如:
2CO(g)+O2(g)=2CO2(g); △H= -566kJ·moL-1
2H2(g)+O2(g)=2H2O(g); △H=-483.6kJ·moL-1
H2O(g)=H2O(l) △H= -44.0kJ·moL-1
(1)氢气燃烧热△H=_____________________。
(2)写出CO 和H2O(g)作用生成CO2 和H2的热化学方程式______________________。
(3)往1L 体积不变的容器中加入0.200molCO和1.00molH2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1(方程式中各物质前化学计量数为最简整数比),则t℃时CO的转化率为____________;反应达到平衡后,升高温度,此时平衡常数将____________(填“变大”、“ 不变”或“变 小”)。
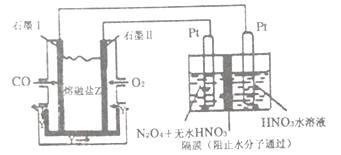
(4)从汽车尾气中分离出CO 与O2、与熔融盐Na2CO3组成燃料电池,同时采用电解法制备N2O5,装置如下图所示,其中Y为CO2。写出石墨Ⅰ电极上发生反应的电极反应式________________。在电解池中生成N2O5的电极反应式为______________________。
(5)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。下图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线,则:
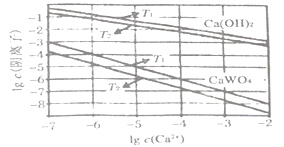
T1___________T2 (填“>”或“<”),T1时Ksp (CaWO4)=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铜及其化合物应用广泛。
Ⅰ.氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下:

已知:CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易氧化。回答下列问题:
(1)步骤①中N元素被还原为最低价,则Cu溶解的离子方程式为_______________。
(2)步骤③中(NH4)SO3要适当过量,目的是使Cu2+充分还原,并保证Cu2+的还原速率和_____,其主要反应的离子方程式________________。已知NH4Cl、Cu2+的物质的量之比[n(NH4Cl]/n(Cu2+)]与Cu2+沉淀率的关系如下图所示,当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,原因是_____________________。

(3)步骤⑥中醇洗的目的是____________________________。
Ⅱ.以氧缺位铁酸铜(CuFe2O4-x)作催化剂,可利太阳能热化学循环法分解H2O制H2,其物质转化如图所示。
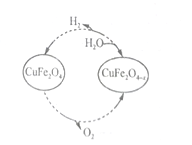
(4)氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_______________。
(5)若x=0.15,则1mol CuFe2O4-x参与一次该循环,理论上能制得的H2体积为_______L(标准状况下)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】用0.1mol/LNaOH溶液滴定40mL0.1mol/LH2SO3溶液,所得滴定曲线如下图所示(忽略混合时溶液体积的变化)。下列叙述不正确的是

A. H2SO3的Ka1=1×10-2
B. 0.05mol/L NaHSO3溶液的PH=4.25
C. 图中Y点对应的溶液中,3c(SO32-)=c(Na+)+c(H+)-c(OH-)
D. 图中Z点对应的溶液中:c(Na+)> c(SO32-)> c(HSO32-)> c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
B.图2表示压强对可逆反应2A(g)+2 B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图3表示等质量的钾、钠分别与足量水反应,则甲为钠
D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com