
科目: 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是()
3C+4D反应中,表示该反应速率最快的是()
A.v(A)=0.5 mol/(L·min) B.v(B)=0.3 mol/(L·min)
C.v(C)=0.8 mol/(L·min) D.v(D)=1 mol/(L·min)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于CH4和CO2的说法不正确的是
A. 固态CO2属于分子晶体,其晶体中每个CO2分子周围有12个分子紧邻
B. CH4、CO2分子中均含有极性共价键,均是非极性分子
C. 因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
D. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如下图。下列有关该物质的说法正确的是:
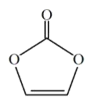
A. 该分子与水分子之间可形成氢键
B. 分子中含6个σ键
C. 分子中氧原子和碳原子的杂化类型相同
D. 该分子为非极性分子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列无色溶液中的离子能大量共存的是( )
A.H+、K+、OH-、Cl-B.Na+、Cu2+、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl-D.Ba2+、K+、CO32-、NO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,撒盐可以起到凝血作用,其化学原理是( )
A.丁达尔效应B.胶体聚沉
C.发生复分解反应D.发生氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的脱氧剂,其制备方法是向Na2CO3溶液中通入SO2,生成NaHSO3和CO2,一定条件下NaHSO3转化为Na2S2O5。完成下列填空:
(1)碳原子的原子结构示意图是_____________;CO2中所含共价键的类型_____________。
(2)从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。_______________。
(3)SO2 与Na2CO3溶液反应生成NaHSO3和CO2,其化学方程式为_______________________,证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是_________________。
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+ H2O→Na2SO4+H2SO4,该反应中,氧化产物是______;若反应中转移了0.04mol的电子,有________g Na2S2O5参加反应。
(5)连二亚硫酸钠Na2S2O4俗称保险粉,广泛用于纺织工业的还原性染色、清洗、印花、脱色以及织物的漂白等。Na2S2O4属于强还原剂,暴露于空气中易被氧气氧化。Na2S2O4遇KMnO4酸性溶液发生反应:5Na2S2O4+6KMnO4+4H2SO4=5Na2SO4+3K2SO4+6MnSO4+4H2O。
为了测定保险粉纯度。称取5.0g Na2S2O4样品溶于冷水中,配成100mL溶液,取出10mL 该溶液于锥形瓶中,用0.1000mol/L的KMnO4 溶液滴定。重复上述操作2 次,平均消耗KMnO4 溶液21.00mL。则该样品中Na2S2O4的质量分数为__________(杂质不参与反应)。(保留至0.1%)
(6)“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。请写出金属钒与浓硝酸反应的离子方程式:_______________________________________。
(7)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:__________、_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按图1所示工艺流程制备氯化铜晶体(CuCl2·2H2O):
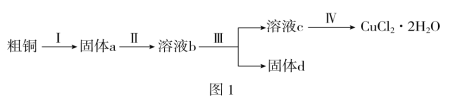
请回答下列问题:
(1)为了完成步骤Ⅰ,可采用图2所示的装置将粗铜完全转化为固体a:
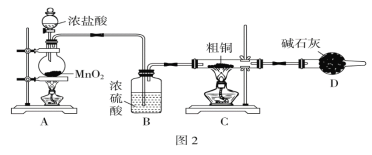
①A装置中发生反应的离子方程式是___________________________________________。
②在该实验中,点燃A、C装置中的酒精灯时,应该先点燃________装置的酒精灯,D装置的作用是_____________________________,C装置中生成的产物是________________。
③有同学认为应在B装置前增加吸收HCl的装置,你认为是否必要____(填“是”或“否”)。
(2)步骤Ⅱ的操作:将固体a置于烧杯中,然后加入_________,至固体完全溶解。
(3)步骤Ⅲ中应先加入某试剂调节溶液b的pH以除去杂质,该试剂可选用下列试剂中的________(填序号)。
a.NaOH溶液 b.氨水 c.CuO d.Cu2(OH)2CO3 e.CuSO4溶液
(4)步骤Ⅳ中,将溶液c蒸发浓缩、冷却结晶、过滤得到CuCl2·2H2O。现欲得到无水CuCl2,在实验室也可以采用图2所示装置使CuCl2·2H2O脱水得到无水CuCl2,则A装置中的两种化学试剂是___________________________(填名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com