
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎΝΘΉ”NH3D+÷–Θ§ΒγΉ” ΐΓΔ÷ Ή” ΐΚΆ÷–Ή” ΐ÷°±»ΈΣ
A.10ΘΚ7ΘΚ11B.11ΘΚ11ΘΚ8C.10ΘΚ11ΘΚ8D.11ΘΚ8ΘΚ10
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Έ¬Ε»œ¬Θ§ΫΪ≈®Ε»ΕΦ «0.1molΓΛL-1ΒΡX2ΓΔY2ΝΫ÷÷ΤχΧε≥δ»κ÷ΝΟή±’»ίΤς÷–Θ§ Ι÷°ΖΔ…ζΖ¥”Π…ζ≥…ΤχΧεZΘ§¥οΒΫΤΫΚβ ±c(X2)=0.04molΓΛL-1ΓΔc(Y2)=0.08molΓΛL-1ΓΔc(Z)=0.04molΓΛL-1Θ§‘ρΗΟΖ¥”ΠΒΡΖ¥”Π Ϋ «
A. X2+2Y2![]() XY2 B. 3X2+Y2
XY2 B. 3X2+Y2![]() 2X3Y
2X3Y
C. 2X2+Y2![]() 2X2Y D. X2+3Y2
2X2Y D. X2+3Y2![]() 2XY3
2XY3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®ΧβΈΡΘ©≥ΘΈ¬œ¬Θ§Ρ≥Υ°»ή“ΚM÷–¥φ‘ΎΒΡάκΉ””–NaΘΪΓΔA2Θ≠ΓΔHAΘ≠ΓΔHΘΪΓΔOHΘ≠Θ§¥φ‘ΎΒΡΖ÷Ή””–H2OΓΔH2AΓΘΗυΨίΧβ“βΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)–¥≥ωΥαH2AΒΡΒγάκΖΫ≥Χ Ϋ_________________________ΓΘ
(2)»τ»ή“ΚM”…10 mL 2 molΓΛLΘ≠1NaHA»ή“Κ”κ10 mL 2 molΓΛLΘ≠1 NaOH»ή“ΚΒ»ΧεΜΐΜλΚœΕχ≥…Θ§‘ρ»ή“ΚMΒΡpH________(ΧνΓΑ<Γ±ΓΑ>Γ±ΜρΓΑΘΫΓ±)7Θ§»ή“Κ÷–άκΉ”≈®Ε»”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ______________ΓΘ“―÷ΣKsp(BaA)ΘΫ1.8ΓΝ10Θ≠10Θ§œρΗΟ»ή“Κ÷–Φ”»κ10 mL 1 molΓΛLΘ≠1BaCl2»ή“ΚΘ§ΜλΚœΚσ»ή“Κ÷–ΒΡBa2ΘΪ≈®Ε»ΈΣ________molΓΛLΘ≠1ΓΘ
(3)»τ”–œ¬Ν–»ΐ÷÷»ή“ΚΘΚΔΌ0.01 molΓΛLΘ≠1ΒΡH2A»ή“ΚΘΜΔΎ0.01 molΓΛLΘ≠1ΒΡNaHA»ή“ΚΘΜΔέ0.02 molΓΛLΘ≠1ΒΡHCl”κ0.04 molΓΛLΘ≠1ΒΡNaHA»ή“ΚΒ»ΧεΜΐΜλΚœΘ§‘ρ»ΐ÷÷«ιΩωœ¬Θ§»ή“Κ÷–c(H2A)Ήν¥σΒΡ «____________ΘΜpH”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ______________ΓΘ
(4)»τ»ή“ΚM”…pHΘΫ3ΒΡH2A»ή“ΚV1 mL”κpHΘΫ11ΒΡNaOH»ή“ΚV2 mLΜλΚœΖ¥”ΠΕχΒΟΘ§ΜλΚœ»ή“Κ÷–![]() ΘΫ104Θ§V1”κV2ΒΡ¥σ–ΓΙΊœΒΈΣ________(ΧνΓΑV1¥σ”ΎV2Γ±ΓΑV1Β»”ΎV2Γ±ΓΑV1–Γ”ΎV2Γ±ΜρΓΑΨυ”–Ω…ΡήΓ±)ΓΘ
ΘΫ104Θ§V1”κV2ΒΡ¥σ–ΓΙΊœΒΈΣ________(ΧνΓΑV1¥σ”ΎV2Γ±ΓΑV1Β»”ΎV2Γ±ΓΑV1–Γ”ΎV2Γ±ΜρΓΑΨυ”–Ω…ΡήΓ±)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΗςΉιΈΔΝΘ÷–Θ§ΜΞΈΣΒ»ΒγΉ”ΧεΒΡ «(ΓΓΓΓ)
A.N2OΚΆCO2B.COΚΆCO2
C.Na+ΚΆF-D.H3O+ ΚΆPCl3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎΕ®Έ¬ΓΔΕ®»ίΧθΦΰœ¬Θ§≤ΜΡή±ξ÷ΨH2(g)ΘΪI2(g)![]() 2HI(g)¥οΜ·―ßΤΫΚβΒΡ «Θ® Θ©
2HI(g)¥οΜ·―ßΤΫΚβΒΡ «Θ® Θ©
A. ΒΞΈΜ ±ΦδΡΎœϊΚΡa mol H2Ά§ ±œϊΚΡ2a mol HI
B. »ίΤςΡΎΒΡΉή―Ι«Ω≤ΜΥφ ±Φδ±δΜ·Εχ±δΜ·
C. »ίΤςΡΎH2ΓΔI2≤Μ‘ΌΦθ…ΌΘ§HI≤Μ‘Ό‘ωΦ”
D. ΒΞΈΜ ±ΦδΡΎΟΩ…ζ≥…a mol HIΘ§Ά§ ±”–aNAΗωHIΖ÷Ή”Ζ÷Ϋβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎΟή±’»ίΤς÷–ΖΔ…ζΖ¥”ΠX(g)ΘΪ3Y(g)![]() 2Z(g)Θ§»τXΓΔYΓΔZΒΡΤπ Φ≈®Ε»Ζ÷±πΈΣ0.1 molΓΛLΘ≠1ΓΔ0.3molΓΛLΘ≠1ΚΆ0.2molΓΛLΘ≠1Θ§‘ρΤΫΚβ ±ΗςΈο÷ ΒΡ≈®Ε»≤ΜΩ…Ρή «Θ® Θ©
2Z(g)Θ§»τXΓΔYΓΔZΒΡΤπ Φ≈®Ε»Ζ÷±πΈΣ0.1 molΓΛLΘ≠1ΓΔ0.3molΓΛLΘ≠1ΚΆ0.2molΓΛLΘ≠1Θ§‘ρΤΫΚβ ±ΗςΈο÷ ΒΡ≈®Ε»≤ΜΩ…Ρή «Θ® Θ©
A. XΈΣ0.2 molΓΛLΘ≠1
B. YΈΣ0.1 molΓΛLΘ≠1
C. ZΈΣ0.3 molΓΛLΘ≠1
D. ZΈΣ0.1 molΓΛLΘ≠1 ±Θ§YΈΣ0.45 molΓΛLΘ≠1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γΆΦΉΑ÷ΟΘ§ΫΪ»ή“ΚA÷πΒΈΦ”»κΙΧΧεB÷–Θ§œ¬Ν––π ω’ΐ»ΖΒΡ «

A. »τAΈΣ≈®―ΈΥαΘ§BΈΣMnO2Θ§C÷– ΔΤΖΚλ»ή“ΚΘ§‘ρC÷–»ή“ΚΆ …Ϊ
B. »τAΈΣ¥ΉΥαΘ§BΈΣ±¥Ω«Θ§C÷– ΔΙΐΝΩ≥Έ«ε ·Μ“Υ°Θ§‘ρC÷–»ή“Κ±δΜκΉ«
C. »τAΈΣ≈®Α±Υ°Θ§BΈΣ…ζ ·Μ“Θ§C÷– ΔAlCl3»ή“ΚΘ§‘ρC÷–œ»≤ζ…ζΑΉ…Ϊ≥ΝΒμΚσ≥ΝΒμ”÷»ήΫβ
D. »τAΈΣ≈®ΝρΥαΘ§BΈΣNa2SO3ΙΧΧεΘ§C÷– Δ ·»ο ‘“ΚΘ§‘ρC÷–»ή“Κœ»±δΚλΚσΆ …Ϊ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»τœ¬ΆΦ±μ ΨœρΚ§Mg2ΘΪΓΔAl3ΘΪΓΔNH4ΘΪΒΡ―Έ»ή“Κ÷–ΒΈΦ”NaOH»ή“Κ ±Θ§≥ΝΒμΒΡΝΩ”κNaOHΒΡΧεΜΐΒΡΙΊœΒΆΦΓΘ
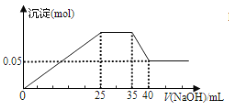
ΔΌ ΔΎ
œ¬Ν–Ης±μ ω”κ Ψ“βΆΦ“Μ÷¬ΒΡ «Θ® Θ©
A. ΆΦΔΌ»ΐ÷÷άκΉ”ΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ:n(Mg2ΘΪ):n(Al3ΘΪ):n(NH4ΘΪ)ΘΫ2:3:2
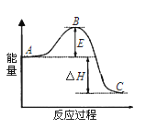
B. ΆΦΔΎ÷–«ζœΏ±μ ΨΡ≥Ζ¥”ΠΙΐ≥ΧΒΡΡήΝΩ±δΜ·Θ§ »τ Ι”Ο¥ΏΜ·ΦΝΘ§BΒψΜαΫΒΒΆ
C. ΆΦΔΌ÷– Ι”ΟΒΡNaOHΒΡ≈®Ε»ΈΣ2 mol/L
D. ΆΦΔΎ÷–Έο÷ AΖ¥”Π…ζ≥…Έο÷ CΘ§ΠΛH>0
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΦΉ¥Φ «“Μ÷÷ΚήΚΟΒΡ»ΦΝœΘ§ΙΛ“Β…œ”ΟCH4ΚΆH2OΈΣ‘≠ΝœΘ§Ά®ΙΐΖ¥”ΠΔώΚΆΔρά¥÷Τ±ΗΦΉ¥ΦΓΘ
(1)ΫΪ1.0 mol CH4ΚΆ2.0 mol H2O(g)Ά®»κΖ¥”Π “(»ίΜΐΈΣ100 L)Θ§‘Ύ“ΜΕ®ΧθΦΰœ¬ΖΔ…ζΖ¥”ΠΘΚ
CH4(g)ΘΪH2O(g)![]() CO(g)ΘΪ3H2(g)Γ≠Γ≠ΔώΓΘCH4 ΒΡΉΣΜ·¬ ”κΈ¬Ε»ΓΔ―Ι«ΩΒΡΙΊœΒ»γΆΦΓΘ
CO(g)ΘΪ3H2(g)Γ≠Γ≠ΔώΓΘCH4 ΒΡΉΣΜ·¬ ”κΈ¬Ε»ΓΔ―Ι«ΩΒΡΙΊœΒ»γΆΦΓΘ
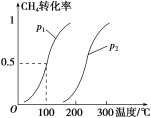
ΔΌ“―÷Σ100 Γφ ±¥οΒΫΤΫΚβΥυ–ηΒΡ ±ΦδΈΣ5 minΘ§‘ρ”ΟH2±μ ΨΒΡΤΫΨυΖ¥”ΠΥΌ¬ ΈΣ_______ΓΘ
ΔΎΆΦ÷–ΒΡp1________p2(ΧνΓΑ<Γ±ΓΑ>Γ±ΜρΓΑΘΫΓ±)ΓΘ
ΔέΗΟΖ¥”ΠΒΡΠΛH________0(ΧνΓΑ<Γ±ΓΑ>Γ±ΜρΓΑΘΫΓ±)ΓΘ
(2)‘Ύ―Ι«ΩΈΣ0.1 MPaΧθΦΰœ¬Θ§a mol CO”κ 3a mol H2ΒΡΜλΚœΤχΧε‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬ΡήΉ‘ΖΔΖ¥”Π…ζ≥…ΦΉ¥ΦΘΚ
CO(g)ΘΪ2H2(g)![]() CH3OH(g)ΓΓΠΛH<0Γ≠Γ≠ΔρΓΘ
CH3OH(g)ΓΓΠΛH<0Γ≠Γ≠ΔρΓΘ
ΔΌ»τ»ίΤς»ίΜΐ≤Μ±δΘ§œ¬Ν–¥κ ©Ω…‘ωΦ”ΦΉ¥Φ≤ζ¬ ΒΡ «________ΓΘ
AΘ°…ΐΗΏΈ¬Ε»
BΘ°ΫΪCH3OH(g)¥”ΧεœΒ÷–Ζ÷άκ
CΘ°≥δ»κHeΘ§ ΙΧεœΒΉή―Ι«Ω‘ω¥σ
DΘ°‘Ό≥δ»κ1 mol COΚΆ3 mol H2
ΔΎΈΣΝΥ―Α’“Κœ≥…ΦΉ¥ΦΒΡΈ¬Ε»ΚΆ―Ι«ΩΒΡ “ΥΧθΦΰΘ§Ρ≥Ά§―ß…ηΦΤΝΥ»ΐΉι Β―ιΘ§≤ΩΖ÷ Β―ιΧθΦΰ“―Ψ≠Χν‘Ύœ¬Οφ Β―ι…ηΦΤ±μ÷–ΓΘ
Β―ι±ύΚ≈ | T(Γφ) | n(CO)/n(H2) | p(MPa) |
1 | 150 | 1/3 | 0.1 |
2 | a | 1/3 | 5 |
3 | 350 | b | 5 |
A.‘ρ…œ±μ÷– Θ”ύΒΡ Β―ιΧθΦΰ ΐΨίΘΚaΘΫ________Θ§bΘΫ________ΓΘ
BΘ°ΗυΨίΖ¥”ΠΔρΒΡΧΊΒψΘ§»γΆΦ «‘Ύ―Ι«ΩΖ÷±πΈΣ0.1 MPaΚΆ5 MPaœ¬COΒΡΉΣΜ·¬ ΥφΈ¬Ε»±δΜ·ΒΡ«ζœΏΆΦΘ§«κ÷ΗΟςΆΦ÷–ΒΡ―Ι«ΩpxΘΫ________MPaΓΘ

(3)“‘ΦΉ¥ΦΉςΈΣ»ΦΝœ÷Τ≥…ΒΡ»ΦΝœΒγ≥ΊΫαΙΙ Ψ“βΆΦ»γΆΦΥυ ΨΓΘ
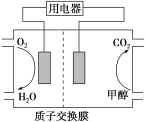
ΙΊ”ΎΗΟΒγ≥ΊΒΡ–π ω’ΐ»ΖΒΡ «________ΓΘ
AΘ°Β±Βγ≥ΊΖ¥”ΠœϊΚΡΝΥ1 molΦΉ¥Φ ±Θ§»ή“Κ÷–ΉΣ“ΤΝΥ12NAΗωeΘ≠
BΘ°Βγ≥ΊΒΡΗΚΦΪΖ¥”ΠΈΣCH3OHΘΪH2OΘ≠6eΘ≠===CO2ΓϋΘΪ6HΘΪ
CΘ°Ζ≈ΒγΙΐ≥Χ÷–Θ§HΘΪ¥”’ΐΦΪ«χœρΗΚΦΪ«χ«®“Τ
DΘ°‘ΎΒγ≥ΊΖ¥”Π÷–Θ§ΟΩœϊΚΡ1 mol―θΤχΘ§άμ¬έ…œΡή…ζ≥…±ξΉΦΉ¥Ωωœ¬CO2ΤχΧε22.4/3 L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com